
科目:高中化学 来源: 题型:
| A | ①能使溴的四氯化碳溶液褪色;②比例模型为; ③能与水在一定条件下反应生成C ③能与水在一定条件下反应生成C |
| B | ①由C、H两种元素组成;②球棍模型为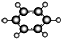 |
| C | ①由C、H、O三种元素组成;②能与Na反应,但不能与NaOH溶液反应;③能与E反应生成相对分子质量为100的酯 |
| D | ①相对分子质量比C少2;②能由C氧化而成 |
| E | ①由C、H、O三种元素组成;②球棍模型为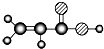 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2:3 | B、1:3 |
| C、1:4 | D、1:7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
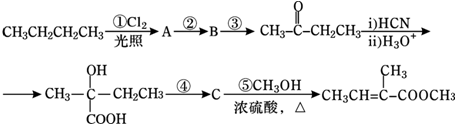
| H3O+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
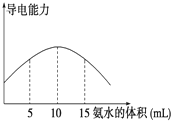 电离度是描述弱电解质电离程度的物理量,电离度=(已电离的电解质的物质的量/原来总的物质的量)×100%.现取20mL pH=3的 CH3COOH溶液,加入0.2mol?L-1的氨水,测得溶液导电性变化如图,则加入氨水前CH3COOH的电离度为( )
电离度是描述弱电解质电离程度的物理量,电离度=(已电离的电解质的物质的量/原来总的物质的量)×100%.现取20mL pH=3的 CH3COOH溶液,加入0.2mol?L-1的氨水,测得溶液导电性变化如图,则加入氨水前CH3COOH的电离度为( )| A、0.5% | B、1.5% |
| C、0.1% | D、1% |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cu2+和SO42- |
| B、Cu2+和Cl- |
| C、K+和SO42- |
| D、Ag+和NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、摩尔是用来衡量微观粒子多少的一种物理量 |
| B、在一定的温度和压强下,各种气体的摩尔体积相等 |
| C、阿伏加德罗常数的数值是0.012 kg碳所含的原子个数 |
| D、若气体摩尔体积为22.4 L?mol-1,则所处条件为标准状况 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com