
A、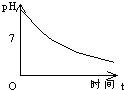 |
B、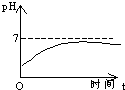 |
C、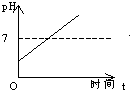 |
D、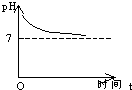 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
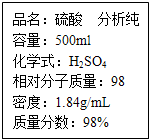 如图是某校实验室中一瓶硫酸试剂标签上的部分内容.下列说法中正确的是( )
如图是某校实验室中一瓶硫酸试剂标签上的部分内容.下列说法中正确的是( )| A、该硫酸的物质的量浓度为9.2mol/L |
| B、取该硫酸与等质量的水混合后,硫酸的物质的量浓度为9.2mol/L |
| C、配制250mL 4.6mol?L-1的稀硫酸需取该硫酸62.5ml |
| D、配制250ml 4.6mol?L-1硫酸,某同学在定容时俯视刻度线,则所配浓度偏小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、实验室用MnO2、浓盐酸制备Cl2:MnO2+4H++2Cl-
| ||||
| B、氧化铁可溶于氢碘酸(HI):Fe2O3+6H+═2Fe3++3H2O | ||||
| C、少量金属钠放入冷水中:Na+2H2O═Na++2OH-+H2↑ | ||||
| D、碳酸氢钙溶液和少量氢氧化钠溶液混合:HCO3-+OH-═CO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碘遇淀粉变蓝色这一现象发生了化学变化 |
| B、质子数为53的碘-131的质量数为184 |
| C、碘盐中碘元素存在的形态是化合态(KI) |
| D、碘-131的化学元素符号为 I |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②④ | B、④⑤ |
| C、①③④ | D、①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com