
����Ŀ���±�ΪԪ�����ڱ���һ���֣��û�ѧ����ش��������⣺
���� ���ڡ� | ��A | ��A | ��A | ��A | ��A | ��A | ��A |
1 | �� | ||||||
2 | �� | �� | �� | ||||
3 | �� | �� | �� | �� | �� | �� |
��1�����ԭ�ӽṹʾ��ͼΪ________________________________��
��2���ں͢���̬�⻯���ȶ��ԵĴ�С˳��___________(�ѧʽ)��
��3���ۢ�����ۺ������������ǿ����__________(�ѧʽ)��
��4���۵���̬�⻯����۵�����������Ӧ��ˮ���ﷴӦ���ɵ�����________(�ѧʽ)��������________(�������ۻ��������������ӻ�������)��
��5���٢ܢ�����Ԫ�ص�ԭ�����γ�ԭ����Ŀ��Ϊ1��1��1�Ĺ��ۻ�������ĵ���ʽΪ________��
��6�����ȽϢܺ͢�����Ԫ�صķǽ�����ǿ����������Ϊ��֤��֤����________(����ĸ)��
A���Ƚ�������Ԫ�ص��ʵķе�
B���Ƚ�������Ԫ�ص������������ϵ�����
C���Ƚ�������Ԫ�ص�����������Ӧˮ����������
D���Ƚ�������Ԫ�ص��������Ӧ��������
���𰸡�  NH3>CH4 HClO4 NH4NO3 ���ӻ�����
NH3>CH4 HClO4 NH4NO3 ���ӻ����� ![]() B
B
������������Ԫ�������ڱ��е����λ�ÿ�֪�١���ֱ���H��C��N��O��Na��Mg��Al��P��S��Cl��
��1��P��ԭ�ӽṹʾ��ͼΪ��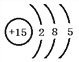 ����2���ں͢�����ͬ���ڣ��������ҷǽ�������ǿ������̬�⻯���ȶ��Դ�С˳����NH3��CH4����3���ۡ��ࡢ��ķǽ�������ǿ����Cl������ۺ������������ǿ����HClO4����4���۵���̬�⻯���ǰ������۵�����������Ӧ��ˮ���������ᣬ���߷�Ӧ����ʽNH3+HNO3=NH4NO3��������������ӻ������5���١��ܡ�������Ԫ�ص�ԭ�����γ�ԭ����Ŀ��Ϊ1:1:1�Ĺ��ۻ�������HClO������ʽΪ
����2���ں͢�����ͬ���ڣ��������ҷǽ�������ǿ������̬�⻯���ȶ��Դ�С˳����NH3��CH4����3���ۡ��ࡢ��ķǽ�������ǿ����Cl������ۺ������������ǿ����HClO4����4���۵���̬�⻯���ǰ������۵�����������Ӧ��ˮ���������ᣬ���߷�Ӧ����ʽNH3+HNO3=NH4NO3��������������ӻ������5���١��ܡ�������Ԫ�ص�ԭ�����γ�ԭ����Ŀ��Ϊ1:1:1�Ĺ��ۻ�������HClO������ʽΪ![]() ����6��A��Ԫ�ص��ʵķе㲻�������ȽϷǽ�����ǿ����A����B��Ԫ�ص�������������Խ���ף��ǽ�����Խǿ��B��ȷ��C����Ԫ��û�����������ˮ���C����D��Ԫ�ص��������Ӧ�������ԣ����������ȽϷǽ�����ǿ����D����ѡB��
����6��A��Ԫ�ص��ʵķе㲻�������ȽϷǽ�����ǿ����A����B��Ԫ�ص�������������Խ���ף��ǽ�����Խǿ��B��ȷ��C����Ԫ��û�����������ˮ���C����D��Ԫ�ص��������Ӧ�������ԣ����������ȽϷǽ�����ǿ����D����ѡB��


 ����ѧҵ���Ե�����ϵ�д�
����ѧҵ���Ե�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��ʵ��װ���У�A��F�ֱ�ΪNH3��Cl2�ķ���װ�ã� 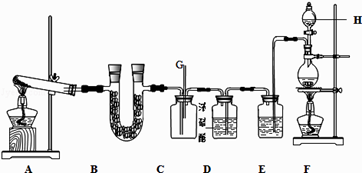
��ش��������⣺
��1��װ��F�з�����Ӧ�����ӷ���ʽΪ ��
��2���ס�����ͬѧ�ֱ�����������ַ�����ȡC12���ף��ú�HCl 146g��Ũ������������MnO2��Ӧ���ң���87g MnO2������Ũ���ᷴӦ������������������ĸ���� a���ױ��Ҷ�b���ұȼ�c��һ����
��3������H���������������ƣ���װ��E�������� ��
��4��װ��C�ĵ���G���ݳ���β���п��ܺ��л���ɫ���ж����壬��������β����������ѡ���Լ������ƣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�仯�У����ܷ����ı����(����)
A.������B.������C.���������D.ԭ�Ӻ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�ص�ͬλ��![]() X�������Ȼ���XCl2 1.11 g����ˮ�Ƴ���Һ����1 mol��L��1��AgNO3��Һ20 mLǡ����ȫ��Ӧ��������ͬλ������20�����ӣ���
X�������Ȼ���XCl2 1.11 g����ˮ�Ƴ���Һ����1 mol��L��1��AgNO3��Һ20 mLǡ����ȫ��Ӧ��������ͬλ������20�����ӣ���
��1��Z��A��ֵ��Z��________��A��________��
��2��XԪ�������ڱ��е�λ�ã�________��
��3��д��XCl2��AgNO3��Ӧ�Ļ�ѧ����ʽ ____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ������ ��
A. 1 mol ���ʵ��������ڸ����ʵ���Է������������ԭ������
B. Ħ���������ʵ�����������λ���������ʵ�����������λ
C. �����ӵ�������12 kg 12C�к��е�̼ԭ����
D. ���ʵ������������������ӵ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȫ��̬����������ܶȸߡ��ɱ��ͣ��乤��ԭ����ͼ��ʾ�����е缫a���ò���ʯīϩ��S8���ϣ���ط�ӦΪ��16Li+xS8=8Li2Sx��2��x��8��������˵��������ǣ�������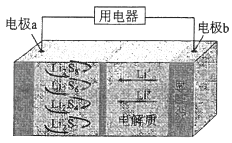
A.��ع���ʱ�������ɷ�����Ӧ��2Li2S6+2Li++2e��=3Li2S4
B.��ع���ʱ�����·������0.02 mol���ӣ��������ϼ���0.14 g
C.ʯīϩ��������Ҫ����ߵ缫a�ĵ�����
D.��س��ʱ��Խ��������е�Li2S2��Խ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ɱ��۵�ܵ������ڣ� ��
A.CO2�ǷǼ��Է���
B.C=O���ļ��ܺ�С
C.CO2��ѧ���ʲ�����
D.CO2���Ӽ������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ˮ�ķе�Ϊ100�棬����ķ��ӽṹ��ˮ���ƣ������ķе�ȴ�ܵͣ��ǩ�60.7�棬�������ֲ������Ҫԭ���ǣ� ��
A.���»���
B.���ۼ�
C.���
D.��Է�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯�У���Ҫ���뻹ԭ�����ǣ� ��
A. Cl-��Cl2 B. FeCl3��FeCl2
C. C��CO2 D. KMnO4��K2MnO4
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com