
【题目】光气(COC12熔点为-118℃,沸点为8.2℃,微溶于水,易溶于甲苯等有机溶剂)可作为化学武器的成分,其制备实验装置如图所示(夹持装置已省略)。
已知:3CCl4+2H2SO4(浓)![]() 3COCl2↑+4HCl+S2O5Cl2。下列说法正确的是
3COCl2↑+4HCl+S2O5Cl2。下列说法正确的是
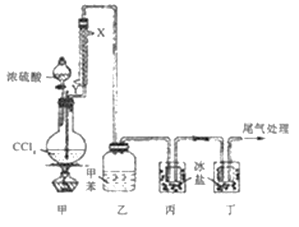
A. 装置组装连接后,第一步操作通入冷凝水,然后才能加热
B. 自来水从冷凝管的X口通入,且被冷凝的物质是CCl4
C. 装置乙中可收集到光气的甲苯溶液,装置丙、丁均可收集到液态光气
D. 可将装置丁的尾气通过导管直接通入NaOH溶液中进行尾气处理
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.浓硫酸具有强氧化性,不能干燥二氧化硫气体
B.相同条件下的![]() 和
和![]() 以1:1的体积比混合,在光照条件下充分反应,生成物中物质的量最多的为
以1:1的体积比混合,在光照条件下充分反应,生成物中物质的量最多的为![]()
C.由粗硅制高纯硅的过程中涉及:粗硅![]() 高纯硅,高纯硅可用来做光导纤维
高纯硅,高纯硅可用来做光导纤维
D.![]() 是引起酸雨的主要原因,燃煤中加入生石灰有利于减少
是引起酸雨的主要原因,燃煤中加入生石灰有利于减少![]() 的排放
的排放
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家最近发现一种只有六个中子构成的粒子,这种粒子称为“六中子”,也有人称之为“零号元素”。下列有关“六中子”粒子的说法不正确的是
A.该粒子不显电性B.该粒子质量数为6
C.在周期表中与氢元素占同一位置D.该粒子质量比氢原子的大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在一容积为2L的密闭容器中,发生如图所示的反应。已知X、Y、Z均为气体,请回答下列问题:
(1)物质Z在0~10min的平均反应速率______。
(2)物质X和Y在反应中的转化率之比为______。
(3)写出该反应的化学方程式:______。(物质用X、Y、Z表达)。
(4)若已知该反应体系达到平衡状态时,共放出热量76.8kJ,则该反应的△H=______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是人体细胞中三种重要有机物A、C、E的元素组成及相互关系图,请据图回答:

(1)图中X所指的元素为________。
(2)A的中文名称为____________,其彻底水解的产物有___种。
(3)细胞结构Ⅱ的名称为________,在细胞中分布场所为________,主要作用有__________、______。
(4)过程②叫做________,若b的平均相对分子质量为r,通过②反应过程形成m条肽链,经盘曲折叠构成相对分子质量为e的E,则E分子中肽键的数目是________。E具有多样性,其原因由b分析为____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向0.1mol·L-1的 NH4HCO3溶液中逐渐加入0.1mol·L-1NaOH溶液时,含氮、含碳粒子的分布情况如图所示(纵坐标是各粒子的分布系数,即物质的量与起始物质的量比值)。根据图像,下列说法不正确的是
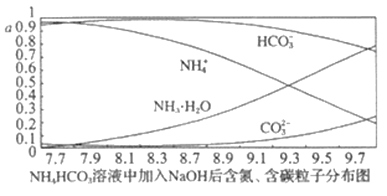
A. 开始阶段,HCO3-反而略有增加,可能是因为NH4HCO3溶液中存在H2CO3发生的主要反应是H2CO3+OH-=HCO3-+H2O
B. 当pH大于8.7以后,碳酸氢根离子和铵根离子同时与氢氧根离子反应
C. pH=9.5时,溶液中c(HCO3-)>c(NH3·H2O)>c(NH4+)>c(CO32-)
D. 滴加氢氧化钠溶液时,首先发生的反应为2NH4HCO3+2NaOH===(NH4)2CO3+Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅蓄电池是常用的化学电源,其电极材料分别是Pb和PbO2,电解液为稀硫酸。放电时,该电池总反应式为:Pb+PbO2+2H2SO4 ![]() 2PbSO4+2H2O。请根据上述情况判断:
2PbSO4+2H2O。请根据上述情况判断:
(1)该蓄电池的负极材料是_________,放电时发生_________(填“氧化”或“还原”)反应。
(2)该蓄电池放电时,电解质溶液的酸性_________(填“增大”、“减小”或“不变”),电解质溶液中阴离子移向_________(填“正”或“负”)极。
(3)已知硫酸铅为不溶于水的白色固体,生成时附着在电极上。试写出该电池放电时,正极的电极反应_______________________________________(用离子方程式表示)。
(4)氢氧燃料电池具有启动快、效率高等优点,其能量密度高于铅蓄电池。若电解质为H2SO4溶液,则氢氧燃料电池的正极反应式为__________________________________。该电池工作时,外电路每流过1×103 mol e-,消耗标况下氧气_________m3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于反应过程中能量变化的说法正确的是

A. 图中a、b曲线可分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g) ΔH<0使用和未使用催化剂时,反应过程中的能量变化
B. 己知2C(s)+2O2(g)=2CO2(g) ΔH1;2C(s)+O2(g)=2CO(g) ΔH2。则ΔH1>ΔH2
C. 同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH不同
D. 在一定条件下,某可逆反应的ΔH=+100kJ·mol-1,则该反应正反应活化能比逆反应活化能大100kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷是一种理想的洁净燃料,利用甲烷与水反应制备氢气,因原料廉价,具有推广价值。该反应为CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H>0
CO(g)+3H2(g) △H>0
(1)800℃时,反应的化学平衡常数K=l.0,某时刻测得该温度下密闭容器中各物质的物质的量浓度如表。则此时正、逆反应速率的关系是____。
CH4 | H2O | CO | H2 |
3.0molL-1 | 8.5molL-1 | 2.0molL-1 | 2.0molL-1 |
(2)为了探究温度、压强对上述化学反应速率的影响,某同学设计了以下三组对比实验(温度为360℃或480℃、压强为101 kPa或303 kPa,其余实验条件见下表)。
实验序号 | 温度/℃ | 压强/kPa | CH4初始浓度/ molL1 | H2O初始浓度/ molL1 |
1 | 360 | p | 2.00 | 6.80 |
2 | t | 101 | 2.00 | 6.80 |
3 | 360 | 101 | 2.00 | 6.80 |
表中t=____,P=_____;设计实验2、3的目的是________________;
实验l、2、3中反应的化学平衡常数的大小关系是____(用K1、K2、K3表示)。
(3)一定温度下,在容积2L且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
容 器 | 甲 | 乙 |
反应物投入量 | 1molCH4、1molH2O | a molCH4、a molH2O、b molCO、c molH2 |
经测定甲容器经过5min达到平衡,平衡后甲中气体的压强为开始的1.2倍,甲容器中该反应在5min内的平均速率υ(H2)=_______,若要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则b的取值范围为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com