
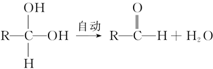
 +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$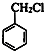 +HCl.
+HCl.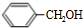 +CH3COOH$→_{△}^{浓硫酸}$
+CH3COOH$→_{△}^{浓硫酸}$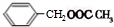 +H2O.
+H2O.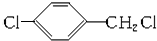 .
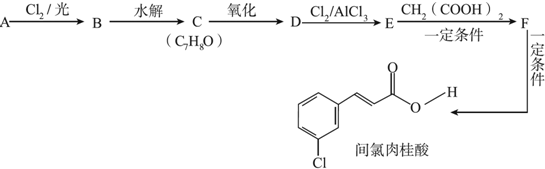
.分析 芳香烃A再光照条件下发生侧链上取代反应生成卤代烃B,卤代烃B水解得到C,结合C的分子式可知,C为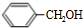 ,A为
,A为 ,B为
,B为 ,C发生氧化反应生成D,而与氯气发生取代反应生成E,结合反应得到I,可知E中含有-CHO,由间氯肉桂酸的结构可知,Cl处于-CHO的间位,故D为
,C发生氧化反应生成D,而与氯气发生取代反应生成E,结合反应得到I,可知E中含有-CHO,由间氯肉桂酸的结构可知,Cl处于-CHO的间位,故D为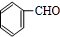 ,E为
,E为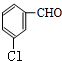 ,由信息I可知F为
,由信息I可知F为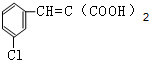 ,据此分析解答.
,据此分析解答.
解答 解:芳香烃A再光照条件下发生侧链上取代反应生成卤代烃B,卤代烃B水解得到C,结合C的分子式可知,C为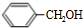 ,A为
,A为 ,B为
,B为 ,C发生氧化反应生成D,而与氯气发生取代反应生成E,结合反应得到I,可知E中含有-CHO,由间氯肉桂酸的结构可知,Cl处于-CHO的间位,故D为
,C发生氧化反应生成D,而与氯气发生取代反应生成E,结合反应得到I,可知E中含有-CHO,由间氯肉桂酸的结构可知,Cl处于-CHO的间位,故D为 ,E为
,E为 ,由信息I可知F为
,由信息I可知F为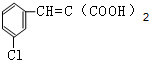 ,
,
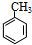
(1)A为 ,名称为甲苯,故答案为:甲苯;
,名称为甲苯,故答案为:甲苯;
(2)C为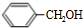 ,为苯甲醇,属于芳香醇,故选c;
,为苯甲醇,属于芳香醇,故选c;
(3)①A在光照的条件下与Cl2反应生成B的方程式为: +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$ +HCl;
+HCl;
②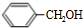 在浓H2SO4存在下与冰醋酸共热发生酯化反应,该反应方程式为:
在浓H2SO4存在下与冰醋酸共热发生酯化反应,该反应方程式为: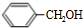 +CH3COOH$→_{△}^{浓硫酸}$
+CH3COOH$→_{△}^{浓硫酸}$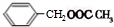 +H2O,
+H2O,
故答案为: +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$ +HCl;
+HCl;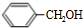 +CH3COOH$→_{△}^{浓硫酸}$
+CH3COOH$→_{△}^{浓硫酸}$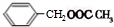 +H2O;
+H2O;
(4)合成路线图中的间氯肉桂酸结构中较大基团处于碳碳双键的两侧,属于反式结构,故答案为:反式;
(5)化学家们研究发现,经A$\stackrel{Cl2/光照}{→}$G$\stackrel{水解}{→}$D这一路线也可达到目的,并能降低成本.经红外光谱分析G与B具有相同的官能团,则G为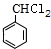 ,若G的一种同分异构体的核磁共振氢谱中只出现三个峰,且峰面积比为1:1:1,则含有侧链为-Cl、-CH2Cl且处于对位,则该同分异构体的结构简式为:
,若G的一种同分异构体的核磁共振氢谱中只出现三个峰,且峰面积比为1:1:1,则含有侧链为-Cl、-CH2Cl且处于对位,则该同分异构体的结构简式为: ,故答案为:
,故答案为: ;
;
(6)F为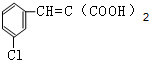 ,分子式为C10H7O4Cl,可以改写为C8H6.2CO2.HCl,间氯肉桂酸的分子式为C9H7O2Cl,可以改写为C8H6.CO2.HCl,1molF与1mol间氯肉桂酸的耗氧量均为(8+$\frac{6}{4}$)mol=9.5mol,二者耗氧量为1:1,故答案为:1:1.
,分子式为C10H7O4Cl,可以改写为C8H6.2CO2.HCl,间氯肉桂酸的分子式为C9H7O2Cl,可以改写为C8H6.CO2.HCl,1molF与1mol间氯肉桂酸的耗氧量均为(8+$\frac{6}{4}$)mol=9.5mol,二者耗氧量为1:1,故答案为:1:1.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断能力,根据反应条件结合间氯肉桂酸结构简式分析推断,题目难度中等.


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:选择题
| A. | 用惰性电极电解饱和氯化钠溶液:2Cl-+2H+═H2↑+Cl2↑ | |
| B. | 用银氨溶液检验乙醛中的醛基:CH3CHO+2Ag(NH3)2++2OH-→CH3COO-+NH4++3NH3+2Aɡ↓+H2O | |
| C. | 向沸水中滴加FeCl3溶液制备胶体:Fe3++3H2O═Fe(OH)3↓+3H+ | |
| D. | 将Cl2溶于水中:Cl2+H2O═Cl-+2H++ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
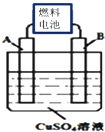 短周期主族元素A,B,C,D,E,F的原子序数依次增大,它们的原子核外电子层数之和为13.B的化合物种类繁多,数目庞大;C,D是空气中含量最多的两种元素,D,E两种元素的单质反应可以生成两种不同的离子化合物;F为同周期半径最小的元素.试回答以下问题:
短周期主族元素A,B,C,D,E,F的原子序数依次增大,它们的原子核外电子层数之和为13.B的化合物种类繁多,数目庞大;C,D是空气中含量最多的两种元素,D,E两种元素的单质反应可以生成两种不同的离子化合物;F为同周期半径最小的元素.试回答以下问题: ,A、C、F三种元素形成的化合物CA4F为离子化合物(填“离子”或“共价”).
,A、C、F三种元素形成的化合物CA4F为离子化合物(填“离子”或“共价”).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用丁达尔效应区分淀粉溶液和食盐水 | |
| B. | 用品红溶液区分SO2与CO2气体 | |
| C. | 用石蕊试液区分KOH溶液与NaOH溶液 | |
| D. | 用碘水区分淀粉溶液与蛋白质溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
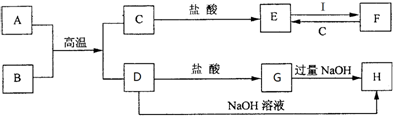

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 结论 |
| 在一杯浑浊的水中加 少量Al2(SO4)3静置 | 烧杯中的水变澄清 | Al2(SO4)3可 以净水 |
| 在一杯浑浊的水中加 少量KCl,静置 | 烧杯中的水 仍然浑浊 | K+不能起净水作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 专一性 | B. | 多样性 | C. | 高效性 | D. | 适应性 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com