
����Ŀ��ͨ����ѧ����ѧϰ��ͬѧ�Ƕ��������Ļ����������˽�һ���˽⡣
��1������H��C��N��O��K����Ԫ�أ���ѡ�����е�Ԫ��д���������ʵĻ�ѧʽ��
����Ȼ������Ҫ�ɷ�____��
�ڼ�����Ѫ�쵰��ϵ��ж�����____��
���ܹ�������������____��
�ܿ������Ϸʵ������____��
��2����ͼ��ij��ʯ��Ʒ�и���Ԫ�غ����ı���ͼ��

�ٸ���ʯ�к�____�ַǽ���Ԫ�أ����к�����������____Ԫ�ء�
�������ӵĽṹʾ��ͼΪ ����X��____��
����X��____��
�۴���ʯ��Ʒ�в����ܺ��еĻ�������____��
A��CaCO3 B��K2SO4 C��Al2O3 D��SiO2
���𰸡�CH4 CO O2 KNO3 3 �� 11 A
��������
��1����Ȼ������Ҫ�ɷ��Ǽ��飬�仯ѧʽΪCH4��һ����̼������Ѫ�쵰��ϣ��仯ѧʽΪ![]() ���������Թ����������仯ѧʽΪO2������صĻ�ѧʽΪKNO3��
���������Թ����������仯ѧʽΪO2������صĻ�ѧʽΪKNO3��
��2������ͼ��֪������ʯ�к�����Ԫ�ء���Ԫ�ء���Ԫ�ع����ַǽ���Ԫ�أ�������Ԫ�صĺ�����ߣ�
�������ӵĺ���������������ԭ�ӵĺ�������������ԭ�ӵĺ���������Ϊ11�����x��11��
����ͼ��֪������ʯ�в���̼Ԫ�أ���˲����ܺ���CaCO3����A����ȷ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ũ�Ⱦ�Ϊ0.1 mol/L�������ΪV0��HX��HY��Һ���ֱ��ˮϡ�������V��pH��![]() ���仯��ϵ��ͼ��ʾ������������ȷ����
���仯��ϵ��ͼ��ʾ������������ȷ����

A��HX��HY�������ᣬ��HX�����Ա�HY����
B�������£���ˮ�������c(H+)��c��OH -����a<b
C����ͬ�¶��£����볣��K( HX)��a>b
D��![]() =3����ͬʱ��������Һ��������HX ��HY��H2O�Ļӷ�������
=3����ͬʱ��������Һ��������HX ��HY��H2O�Ļӷ�������![]() ��С
��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ij��Һ�к���![]() ��
��![]() ��Cl���������ӣ����ֻȡ��һ�θ���Һ(����ʹ�ù��˲���)�����ܰ������������μ��������
��Cl���������ӣ����ֻȡ��һ�θ���Һ(����ʹ�ù��˲���)�����ܰ������������μ��������
(1)Ӧ���ȼ���_____���ӣ�������Լ���ϡ���ᣬ��Ӧ�����ӷ���ʽΪ��_____________��
(2)�ټ���_____���ӣ�������Լ���_________����Ӧ�����ӷ���ʽΪ��__________________��
(3)������_____���ӣ�������Լ���_________����Ӧ�����ӷ���ʽΪ��________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������������λ��ѧ�����о������ӻ����������ϳ������ŵ������ѧ����������һ�ַ��ӻ������������������㻯����a��b��c�Ǻϳ����������ԭ�ϣ���ṹ����ͼ��ʾ������˵������ȷ����

A. b��c��Ϊͬ���칹��
B. a��c����������̼ԭ�Ӿ��п��ܴ���ͬһƽ����
C. a��b��c���ܷ���������Ӧ���ӳɷ�Ӧ���Ӿ۷�Ӧ��������Ӧ
D. a��b��c����ʹ���Ը��������Һ��������Ȼ�̼��Һ��ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(ClNO)���л��ϳ��е���Ҫ�Լ�����ͨ�����·�Ӧ��ã�2NO(g)��Cl2(g) ![]() 2ClNO(g)��
2ClNO(g)��
��1�����������������ڴ����еĺ������������ʱ�������������ȣ��漰���·�Ӧ��
��2NO2(g)��NaCl(s) ![]() NaNO3(s)��ClNO(g)��K1
NaNO3(s)��ClNO(g)��K1
��4NO2(g)��2NaCl(s) ![]() 2NaNO3(s)��2NO(g)��Cl2(g)��K2
2NaNO3(s)��2NO(g)��Cl2(g)��K2
��2NO(g)��Cl2(g) ![]() 2ClNO(g)��K3
2ClNO(g)��K3
��K3��________(��K1��K2��ʾ)��
��2����֪���ֻ�ѧ���ļ����������±�(�������ȵĽṹΪCl��N===O)��
��ѧ�� | N��O | Cl��Cl | Cl��N | N===O |
����/(kJ��mol��1) | 630 | 243 | a | 607 |
��2NO(g)��Cl2(g) ![]() 2ClNO(g)��Ӧ�Ħ�H��a�Ĺ�ϵΪ��H��_______kJ��mol��1��
2ClNO(g)��Ӧ�Ħ�H��a�Ĺ�ϵΪ��H��_______kJ��mol��1��
��3����Ͷ�ϱ�2��1��NO��Cl2���뵽һ��ѹ���ܱ������з�����Ӧ��ƽ��ʱNO��ת�������¶�T��ѹǿp(��ѹ)�Ĺ�ϵ��ͼ(a)��ʾ��
�ٸ÷�Ӧ�Ħ�H________(�>����<������)0��
����pѹǿ�����£�M��ʱ������NO���������Ϊ________��
������Ӧһֱ������pѹǿ�����½��У���M��ķ�ѹƽ�ⳣ��Kp��________(�ú�p�ı���ʽ��ʾ����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ����ѹ���������)��
 ��
��
��4��һ���������ں��º��ݵ��ܱ������а�һ����������NO(g)��Cl2(g)����n(NO)/n(Cl2)��1.5ʱ�ﵽƽ��״̬��ClNO���������������ͼ(b)��D��E��F�����е�________�㡣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ�鼰�������Ƴ���Ӧ���۵���
ѡ�� | ʵ�� | ���� | ���� |
A | ������KIO3��ʳ���м��������Һ��ϡ���ἰKI | ��Һ����ɫ | �����ԣ�IO3- >I2 |
B | ������Һ����������¼���һ��ʱ����������Ƶ�Cu(OH)2����Һ��ϣ�������� | ��ɫ�������� | ����û��ˮ�� |
C | �����£�����������Ũ�ȵ�NaHCO3��CH3COONa��Һ�зֱ�μ�2�η�̪ | ������Һ����죬NaHCO3��Һ��ɫ���� | �����µ�ˮ��ƽ�ⳣ����Kh(CH3COO-)��Kh(HCO3-) |
D | ����ʱ������֧�Թܸ�ȡ5 mL 0.1 mol/L ����KMnO4��Һ���ֱ����0.1 mol/L��0.2 mol/L H2C2O4��Һ��2 mL | ���Թ���Һ����ɫ���Ҽ�0.2 mol/L H2C2O4��Һ���Թ�����ɫ���� | �����������䣬H2C2O4��Һ��Ũ��Խ��ѧ��Ӧ����Խ�� |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧҪ̽��ȼ�յ������Ϳ����������ĺ���������������ʵ�顣
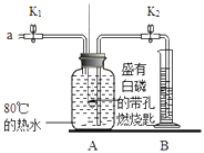
��ʵ�飩
�ټ��װ�õ������ԣ����������á�
����Aƿ�м���80����ˮ����ʢ�а��Ĵ���ȼ�ճ��ٽ�û��ˮ�У�����ƿ�������ײ�ȼ�ա�
�۴�K1��K2����a����Aƿ�й����������ƿ�е�Һ�����ȼ�ճײ�ʱ���ر�K1��K2����ʱ������ͲB��ˮ�����Ϊ200mL���۲쵽Aƿ�еİ���ȼ�ա�
��1���ԱȲ���ں͢۵������֪����ȼ��ȼ�յ�����֮һ��___������ȼ�յķ�Ӧ����ʽΪ_____��
��2����װ����ȴһ��ʱ���K2������۲쵽____��˵�����������������Լռ1/5�����ȷ����װ�����������ã�������ȼ�ճ�λ��©�������______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ʯ�ҷ�������ˮ�У�һ��ʱ���ﵽƽ�⣺Ca(OH)2(s)![]() Ca2+(aq)+2OH-(aq),����������ȷ���ǣ� ��
Ca2+(aq)+2OH-(aq),����������ȷ���ǣ� ��
A. ����Һ�м���������NaOH���壬�����е�Ca(OH)2�Ĺ�������
B. ����Һ�м���Na2CO3��Һ�������е�Ca(OH)2�Ĺ�������
C. ����������Һ�м���CaO����Һ��pH����
D. ����Һ���ȣ���Һ��pH����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����ʱHClO��Ka=3.0��10-8��HF��Ka=3.5��10-4���ֽ�pH���������ͬ�Ĵ�������������Һ�ֱ������ˮϡ�ͣ�pH����Һ����ı仯��ͼ��ʾ������������ȷ����

A. ����IΪ������ϡ��ʱpH�仯����
B. ȡa�����������Һ���к���ͬ�������ͬŨ�ȵ�NaOH��Һ�����Ĵ�����������С
C. a��ʱ������������ͬ��С��п������ʱ������ᷴӦ�����ʴ�
D. b����Һ��ˮ�ĵ���̶ȱ�c����Һ��ˮ�ĵ���̶�С
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com