
【题目】下列反应属于非氧化还原反应的是( )
A. Fe2O3+3CO![]() 2Fe+3CO2
2Fe+3CO2
B. NH4NO3![]() N2O↑十2H2O
N2O↑十2H2O
C. 2FeCl2+Cl2=2FeCl3
D. Cu2(OH)2CO3![]() 2CuO+CO2↑+H2O
2CuO+CO2↑+H2O
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:
【题目】欲用Na2CO3固体配制950mL 0.1 mol·L-1的Na2CO3溶液。配制过程如下图所示
请根据题意回答:
(1)配制该溶液应选用__________mL容量瓶。
(2)用托盘天平称取_________g固体Na2CO3固体。
(3)向容量瓶中加入蒸馏水,直到液面在刻度线下1~2cm时,改用____________滴加蒸馏水至液面的最低点与刻度线相切,盖好瓶塞,摇匀。
(4)在配制上述溶液的实验中,下列操作中会引起结果偏低的有____________(填序号)
A.在烧杯中搅拌溶解溶质时,溅出少量溶液
B.未将洗涤烧杯内壁的溶液转移至容量瓶
C.定容时,加水超过了刻度线,倒出一些再重新加水至刻度线
D.将所配溶液从容量瓶转移到试剂瓶时有少量溶液溅出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)质量比为16∶7∶6的三种气体SO2、CO、NO,分子个数之比为_____________;氧原子个数之比为____________。
(2)在标准状况下,6.8g PH3与标准状况下_______L CH4含有相同数目的H原子。
(3)某气体氧化物化学式为RO2,在标准状况下,1.28 g该氧化物的体积为448 mL,则该氧化物的摩尔质量为________,R的相对原子质量为________。
(4)273 K、1.01×105 Pa时气态单质X2的密度为1.25 g·L-1,则X的相对原子质量为________
(5)相同温度和压强条件下,一定体积的气态氢化物H2R的质量是等体积NH3的2倍,则R的相对原子质量为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)AlCl3的水溶液pH______7(填>、=、<),其原因为______________(用离子方程式表示),将其溶液加热蒸干并灼烧最终得到物质是______(填化学式)。
(2)常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)·c3(OH)=1032,要使c(Cr3+)降至105mol/L,溶液的pH应调至_____。
(3)物质的量浓度相同的三种溶液:①NH4Cl ②氨水 ③NH4HSO4,c(NH4+)大小顺序正确的是______________。 (用序号表示)
(4)常温下两种溶液:a.pH=4 NH4Cl b.pH=4盐酸溶液,其中水电离出C(H+)之比为____________________。
(5)室温,将pH=9的NaOH溶液与pH=4的盐酸溶液混合,若所得混合溶液的pH=6,则NaOH溶液与盐酸的体积比为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】粗铜精炼后的阳极泥中含有Cu、Au(金)和PbSO4等杂质,湿法处理阳极泥进行综合利用的工艺流程如图所示:
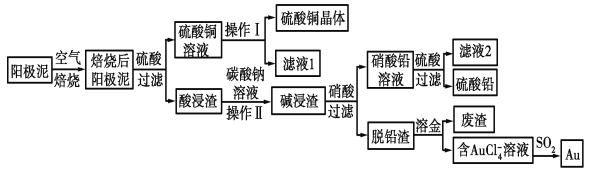
(1)电解精炼含铜、金、铅的粗铜时,电解液应该用________溶液作电解液,电解时阳极的电极反应式为___________________________和Cu-2e-===Cu2+。
(2)完成操作Ⅰ的主要步骤有:__________________,过滤,洗涤,干燥。
(3)写出用SO2还原AuCl4-的离子反应方程式____________________________。
(4)为了减少废液排放、充分利用有用资源,工业上将滤液1并入硫酸铜溶液进行循环操作,请指出流程图中另一处类似的做法________________________。
(5)用离子方程式表示加入碳酸钠溶液的作用:___________________________。[已知298 K时,Ksp(PbCO3)=1.46×10-13,Ksp(PbSO4)=1.82×10-8]。当溶液中c(SO42-)=0.2mol/L时,c(CO32-)=_______________mol/L。(结果保留2位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向V mL 0.1 mol/L氨水中滴加等物质的量浓度的稀H2SO4,测得混合溶液的温度和pOH [pOH=-lgc(OH-)]随着加入稀硫酸的体积的变化如图所示(实线为温度变化,虚线为pOH变化),下列说法不正确的是

A. V =40
B. b点时溶液的pOH > pH
C. a、b、c三点由水电离的c(OH-)依次减小
D. a、b、d三点对应NH3·H2O的电离常数:K(b)>K(d)>K(a)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的氨基甲酸铵固体置于某容积恒定的真空容器中,发生反应:H2NCOONH4(s)![]() 2NH3(g)+CO2(g)在不同温度下,该反应平衡状态部分数据见右表。下列说法正确的是
2NH3(g)+CO2(g)在不同温度下,该反应平衡状态部分数据见右表。下列说法正确的是
温度 | 平衡浓度/(mol·L-1) | |
c(NH3) | c(CO2) | |
T1 | 0.1 | |
T2 | 0.1 | |
A. 若T2>T1,则该反应的ΔH<0
B. T1、T2时,H2NCOONH4转化的Δn(T2)![]() 2Δn(T1)
2Δn(T1)
C. NH3体积分数不变时,说明该反应达到平衡
D. 向容器中充入N2,H2NCOONH4质量增加
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com