
能源问题是人类社会面临的重大课题,甲醇是未来重要的绿色能源之一。以CH4和H2O为原料,通过下列反应来制备甲醇。
Ⅰ.CH4(g)+H2O(g)===CO(g)+3H2(g)
ΔH=+206.0 kJ/mol
Ⅱ.CO(g)+2H2(g)===CH3OH(g)
ΔH=-129.0 kJ/mol
(1)CH4(g)与H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为_____。

(2)将1.0 mol CH4和2.0 mol H2O(g)通入容积为100 L的反应室,在一定条件下发生反应Ⅰ,测得在一定的压强下CH4的转化率与温度的关系如图。
①假设100 ℃时达到平衡所需的时间为5 min,则用H2表示该反应的平均反应速率为________;
②100 ℃时反应Ⅰ的平衡常数为________。
(3)在压强为0.1 MPa、温度为300 ℃条件下,将1.0 mol CO与2.0 mol H2的混合气体在催化剂作用下发生反应Ⅱ生成甲醇,平衡后将容器的容积压缩到原来的 ,其他条件不变,对平衡体系产生的影响是________(填字母序号)。
,其他条件不变,对平衡体系产生的影响是________(填字母序号)。
A.c(H2)减小
B.正反应速率加快,逆反应速率减慢
C.CH3OH的物质的量增加
D.重新平衡时 减小
减小
E.平衡常数K增大
(4)工业上利用甲醇制备氢气的常用方法有甲醇蒸气重整法。该法中的一个主要反应为CH3OH(g)CO(g)+2H2(g),此反应能自发进行的原因是:___。
(5)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后,将Co2+氧化成Co3+,然后以Co3+做氧化剂把水中的甲醇氧化成CO2而净化。实验室用下图装置模拟上述过程:

①写出阳极电极反应式_______________;
②写出除去甲醇的离子方程式___________________。
【解析】 (1)根据盖斯定律,将两个已知的热化学方程式相加可得:CH4(g)+H2O(g)===CH3OH(g)+H2(g) ΔH=+77.0 kJ·mol-1。
(2)v(H2)=3v(CH4)=3×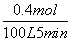 =
=
0.0024 mol·L-1·min-1。根据三段式:
CH4(g)+H2O(g)CO(g)+3H2(g)
起始(mol/L) 0.01 0.02 0 0
转化(mol/L) 0.004 0.004 0.004 0.012
平衡(mol/L) 0.006 0.016 0.004 0.012
则平衡常数:K=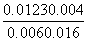 =7.2×10-5。
=7.2×10-5。
(3)增大压强,平衡向正反应方向移动,C、D项正确;但移动的结果不会抵消条件的改变,故c(H2)仍然增大,A项错误;增大压强正逆反应速率均增大,B项错误;平衡常数只与温度有关,温度不变平衡常数不变,E项错误。
(5)Co2+在阳极失电子生成Co3+。
【答案】 (1)CH4(g)+H2O(g)===CH3OH(g)+H2(g)
ΔH=+77.0 kJ·mol-1
(2)①0.0024 mol·L-1·min-1 ②7.2×10-5
(3)CD
(4)该反应是一个熵增的反应(ΔS>0)
(5)①Co2+-e-===Co3+
②6Co3++CH3OH+H2O===CO2↑+6Co2++6H+


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
在一定温度下,向体积恒定的密闭容器中加入1mol X气体和2 mol Y气体,发生如下反应:X(g)+2Y(g) 2Z(g) 此反应达到平衡的标志是
2Z(g) 此反应达到平衡的标志是
A.容器内压强不随时间变化 B.容器内X、Y、Z的浓度之比为1︰2︰2
C.容器内气体的密度不变 D.单位时间消耗0.1mol X同时生成0.2mol Z
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,可逆反应A(气)+3B(气)  2C(气)达到平衡的标志是
2C(气)达到平衡的标志是
A.A、B、C的分子数比为1:3:2 B.A、B、C的浓度相等
C.C生成的速率与C分解的速率相等
D.单位时间生成n mol A,同时生成3n mol B
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是部分短周期元素原子半径与原子序数的关系图,下列说法不正确的是( )

A.N、Z两种元素的离子半径相比前者较大
B.M、N两种元素的气态氢化物的稳定性相比后者较强
C.X与M两种元素组成的化合物能与碱反应,但不能与任何酸反应
D.工业上常用电解Y和N形成的化合物的熔融态制取Y的单质
查看答案和解析>>
科目:高中化学 来源: 题型:
核电荷数小于18的某元素X,其原子核外电子层数为a,最外层电子数为(2a+1)。下列有关元素X的说法中不正确的是( )
A.元素X的原子核内质子数为(2a2-1)
B.元素X的原子半径一定小于 钠的原子半径
钠的原子半径
C.由元素X形成的某些化合物,可能具有杀菌消毒的作用
D.元素X形成的简单离子,各电子层的电子数均达到2n2个(n表示电子层数)
查看答案和解析>>
科目:高中化学 来源: 题型:
光纤通信70年代后期发展起来的一种新型通信技术,目前长距离光纤通信系统已投入使用,光纤通信的光学纤维是由下列哪种物质经特殊工艺制成的 ( )
A.碳 B.石英 C.锗 D.硅
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com