
【题目】为验证卤素单质氧化性的相对强弱,某小组用如图所示装置进行实验(夹持仪器已略去,气密性已检验). 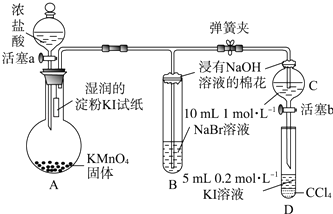
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸.
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹.
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a.
Ⅳ.…
(1)A中产生黄绿色气体,其电子式是 .
(2)验证氯气的氧化性强于碘的实验现象是 .
(3)B中溶液发生反应的离子方程式是 .
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是 .
(5)过程Ⅲ实验的目的是 .
(6)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下 , 得电子能力逐渐减弱.
【答案】
(1)![]()
(2)淀粉KI试纸变蓝
(3)Cl2+2Br﹣=Br2+2Cl﹣
(4)打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D震荡,静置后CCl4层溶液变为紫红色
(5)确认C的黄色溶液中无Cl2 , 排除Cl2对溴置换碘实验的干扰
(6)电子层数依次增多,原子半径逐渐增大
【解析】解:(1)因KMnO4与浓HCl反应可以用来制Cl2 , 其电子式为: ![]() ;故答案为:
;故答案为: ![]() ;(2)因Cl2的氧化性大于I2的氧化性,根据氧化剂的氧化性大于氧化产物的氧化性,可发生:Cl2+2I﹣=I2+2Cl﹣ , I2能使淀粉变蓝; 故答案为:淀粉KI试纸变蓝;Cl2+2I﹣=I2+2Cl﹣; (3)因Cl2的氧化性大于Br2的氧化性,根据氧化剂的氧化性大于氧化产物的氧化性,可发生:Cl2+2Br﹣=Br2+2Cl﹣ , 故答案为:Cl2+2Br﹣=Br2+2Cl﹣ , (4)因Cl2的氧化性大于I2的氧化性,根据氧化剂的氧化性大于氧化产物的氧化性,要发生:Cl2+2I﹣=I2+2Cl﹣ , 同时检验产物碘的存在;故答案为:打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D震荡,静置后CCl4层溶液变为紫(或紫红)色;(5)为验证溴的氧化性强于碘,实验时应避免氯气的干扰,当B中溶液由黄色变为棕红色时,说明有大量的溴生成,此时应关闭活塞a,否则氯气过量,影响实验结论,
;(2)因Cl2的氧化性大于I2的氧化性,根据氧化剂的氧化性大于氧化产物的氧化性,可发生:Cl2+2I﹣=I2+2Cl﹣ , I2能使淀粉变蓝; 故答案为:淀粉KI试纸变蓝;Cl2+2I﹣=I2+2Cl﹣; (3)因Cl2的氧化性大于Br2的氧化性,根据氧化剂的氧化性大于氧化产物的氧化性,可发生:Cl2+2Br﹣=Br2+2Cl﹣ , 故答案为:Cl2+2Br﹣=Br2+2Cl﹣ , (4)因Cl2的氧化性大于I2的氧化性,根据氧化剂的氧化性大于氧化产物的氧化性,要发生:Cl2+2I﹣=I2+2Cl﹣ , 同时检验产物碘的存在;故答案为:打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D震荡,静置后CCl4层溶液变为紫(或紫红)色;(5)为验证溴的氧化性强于碘,实验时应避免氯气的干扰,当B中溶液由黄色变为棕红色时,说明有大量的溴生成,此时应关闭活塞a,否则氯气过量,影响实验结论,
故答案为:确认C的黄色溶液中无Cl2 , 排除Cl2对溴置换碘实验的干扰;(6)因同一主族元素,从上到下,电子层数依次增多,原子半径逐渐增大,元素的金属性逐渐增强,得电子能力逐渐减弱;故答案为:电子层数依次增多,原子半径逐渐增大.
(1)A中产生黄绿色气体为Cl2;(2)根据氧化剂的氧化性大于氧化产物的氧化性,并检验产物碘;(3)根据氧化剂的氧化性大于氧化产物的氧化性;(4)根据氧化剂的氧化性大于氧化产物的氧化性,并检验产物碘的存在;(5)为验证溴的氧化性强于碘,实验时应避免氯气的干扰.;(6)从原子结构(电子层数、原子半径)的角度分析


科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 增大反应物浓度使单位体积内活化分子数和活化分子百分数均增加,有效碰撞增多,反应速率加快
B. 升高温度使单位体积内活化分子百分数大大增加,正反应速率增加,逆反应速率降低
C. 催化剂能降低分子活化时所需能量,使单位体积内活化分子百分数大大增加
D. 增大压强一定能使单位体积内活化分子数增加有效碰撞增多,反应速率加快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,请填写下列空白:
(1)移取10.00 mL密度为ρ g/mL的过氧化氢溶液至250mL (填仪器名称)中,加水衡释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里。
MnO4-+ H2O2+ H+= Mn2++ H2O+□
(3)滴定时,将高锰酸钾标准溶液注入 (填“酸式”或“碱式”)滴定管中。滴定到达终点的现象是 。
(4)重复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为 。
(5)下列操作能使测定结果偏高的是
A.滴定前滴定管尖嘴中有气泡,滴定后气泡消失。
B.读取高锰酸钾标准溶液的刻度时,滴定前平视,滴定后俯视。
C.滴定前,在用蒸馏水洗涤滴定管后,未用高锰酸钾标准液润洗。
D.滴定过程中,锥形瓶中部分溶液溅出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中书写正确的有几项
① FeS固体与稀硝酸混合:FeS + 2H+ = Fe2++H2S
② 用过量氨水吸收烟道气中的SO2:SO2+2NH3·H2O =SO32-+2NH4++H2O
③ 将少量SO2气体通入NaClO溶液中:SO2+2ClO-+H2O=SO32-+2HClO
④ 已知Ka1(H2CO3)> Ka(HClO)> Ka2(HCO3-),向NaClO溶液中通入少量CO2:2ClO-+CO2+H2O=2HClO+CO32-
⑤ 铁屑溶于足量稀硝酸:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O
⑥ 氯气溶于水:Cl2+H2O=2H++Cl-+ClO-
⑦ 实验室用NH4Cl和Ca(OH)2制氨气:NH4++OH-![]() NH3↑+H2O
NH3↑+H2O
⑧ 向NH4Al(SO4)2溶液中逐滴加入Ba(OH)2溶液至SO42-恰好沉淀完全:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O
⑨ 实验室制Cl2:4HCl(浓)十MnO2![]() Mn2++2Cl-+Cl2↑+2H2O
Mn2++2Cl-+Cl2↑+2H2O
⑩ FeCl3溶液刻蚀铜制电路板:Fe3+ +Cu = Fe2+ + Cu2+
A. 1 项 B. 2 项 C. 3 项 D. 4 项
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某恒温密闭容器发生可逆反应Z(?)+W(?)![]() X(g)+Y(?) ΔH ,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件。下列有关说法中不正确的是( )
X(g)+Y(?) ΔH ,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件。下列有关说法中不正确的是( )
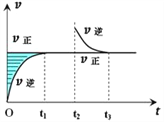
A. Z和W在该条件下一定不为气态
B. t1~t2时间段与t3时刻后,两时间段反应体系中气体的平均摩尔质量不可能相等
C. 若在该温度下此反应平衡常数表达式为K=c(X),则t1~t2时间段与t3时刻后的X浓度相等
D. 若该反应只在某温度T0以上自发进行,则该反应的平衡常数K随温度升高而增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】充分加热如图所示的密闭容器中放置有固体试剂的两个位置, 若钠与氧化银均反应完全且恢复到原来的温度,U形管左右两侧液面相平。下列有关说法中错误的是

A. 反应前后装置内空气的成分保持不变
B. 反应前装置内钠与Ag2O物质的量之比为2:1
C. 热稳定性:生成的钠的氧化物强于Ag2O
D. 反应后有淡黄色固体生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把3mol P和2.5mol Q置于2L密闭容器中,发生如下反应:3P(g)+Q(g)xM(g)+2N(g),5min后达到平衡生成1mol N,经测定这5min内 M的平均速率是0.1mol/(Lmin),下列叙述错误的是( )
A.5min内P的平均反应速率为0.15mol/(Lmin)
B.Q的平衡浓度为1mol/L
C.Q的转化率为25%
D.x是2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com