
相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:
N2(g)+3H2(g)  2NH3(g) ΔH =-92.6 kJ·mol-1。
2NH3(g) ΔH =-92.6 kJ·mol-1。
实验测得起始、平衡时的有关数据如下表所示,下列叙述错误的是
容器 编号 | 起始时各物质的物质的量/mol | 达到平衡时 体系能量的变化 | ||
N2 | H2 | NH3 | ||
① | 1 | 3 | 0 | 放出热量:23.15 kJ |
② | 0.9 | 2.7 | 0.2 | 放出热量:Q kJ |
A.容器①、②中反应的平衡常数相等
B.平衡时,两个容器中NH3的体积分数均为1/7
C.容器②中达到平衡时放出的热量Q=23.15 kJ
D.若其他条件不变,把容器①的体积改为0.5 L,则平衡时放出的热量小于23.15 kJ
C
【解析】
试题分析:同一个反应平衡常数置于温度有关,温度相同,平衡常数相等,A正确;从反应的热化学方程式可以知道,1molN2发生反应放出92.6 kJ,现放出热量为23.15 kJ,则反应的N2物质的量为:23.15 /92.6 =0.25mol,
N2(g)+3H2(g)  2NH3(g)
2NH3(g)
起始(mol) 1 3 0
变化(mol) 0.25 0.75 0.5
平衡(mol) 0.75 2.25 0.5 NH3的体积分数为0.5/(0.75+2.25+0.5)=1/7,②将NH3完全转化为N2 和H2,相当于起始N2、 H2的物质的量分别为1mol和3mol,与①相同,故NH3的体积分数也为1/7,B正确;②要达到①相同的平衡状态,反应要向正向进行,N2从0.9mol变为0.75mol还要反应0.15mol,放出的热量为:0.15×92.6=13.89 kJ,C错误,把容器①的体积改为0.5 L,增大了体积,减小了压强,平衡向逆向移动,故放出的热量小于23.15 kJ,D正确。故选C。
考点:化学反应热的计算、化学平衡的有关计算、化学平衡的移动。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015学年湖南省益阳市高一上学期期中考试化学卷(解析版) 题型:选择题
如果你家里的食用花生油混有水,你将采用下列何种方法分离
A.过滤 B.蒸馏 C.分液 D.萃取
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省高二上学期期末考试化学试卷(解析版) 题型:选择题
以2—氯丙烷为主要原料制1,2—丙二醇CH3CH(OH)CH2OH时,经过的反应为
A.加成—消去—取代 B.消去—加成—取代
C.取代—消去—加成 D.取代—加成—消去
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省龙岩市一级达标校高一上学期期末化学试卷(解析版) 题型:选择题
下列各组物质中,前者是单质,中间是氧化物,后者是混合物的是
A.氯气、次氯酸钠、氯水 B.水银、氧化镁、氢氧化铁胶体
C.木炭、二氧化硫、冰和水 D.钠、氧化钙、过氧化钠
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省龙岩市一级达标校高二上学期期末化学试卷(解析版) 题型:填空题
(12分)某研究性学习小组探究醋酸的溶液情况,进行了如下实验。
(1)取一定量的冰醋酸配制250 mL 0.5000 mol·L-1醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、___________和___________。
(2)用上述0.5000 mol·L-1的醋酸溶液再进行稀释,为测定稀释后醋酸溶液的准确浓度,用0.2000 mol·L-1的NaOH溶液对25.00 mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
实验序号 | 1 | 2 | 3 | 4 |
消耗NaOH溶液的体积(mL) | 25.05 | 25.00 | 23.80 | 24.95 |
则该醋酸溶液的浓度为________________。
(3)实验(2)中,滴定过程中pH变化曲线如图所示(室温条件下)。

①滴定过程中,当滴加12.50mLNaOH时,所得混合溶液中离子浓度由大到小顺序为 。
②当滴加25.00mLNaOH时,反应后测得混合溶液的pH=9。则混合溶液中:水的电离度是纯水的 倍;
c (OH-) -c (CH3COOH) = mol·L-1 。
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省龙岩市一级达标校高二上学期期末化学试卷(解析版) 题型:选择题
下列化学反应表示正确的是
A.Cl2通入水中:Cl2+H2O=2H+ +Cl-+ClO-
B.用惰性电极电解饱和NaCl溶液:2H++2Cl- Cl2↑+H2↑
Cl2↑+H2↑
C.用石墨作电极电解CuSO4溶液:2Cu2++2H2O 2Cu+O2↑+4H+
2Cu+O2↑+4H+
D.钢铁发生吸氧腐蚀时负极反应为:Fe - 3e- = Fe3+
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省龙岩市一级达标校高二上学期期末化学试卷(解析版) 题型:选择题
铁制自来水管与下列材料做成的水龙头连接,锈蚀最快的铁水管所连接的是
A.塑料水龙头 B.铁水龙头 C.铜水龙头 D.陶瓷水龙头
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省漳州市高三3月质量检查化学试卷(解析版) 题型:填空题
(14分)目前机动车使用的电池品种不少,其中铅蓄电池的使用量最大。
I.铅蓄电池的电极材料分别是Pb和PbO2,电解质溶液为稀硫酸。铅蓄电池充放电的总反应方程式为:
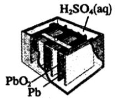
PbO2+Pb+2H2SO4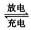 2PbSO4+2H2O,请根据上述情况判断:
2PbSO4+2H2O,请根据上述情况判断:
(1)电池的负极材料是 。
(2)充电时,铅蓄电池阳极的电极反应式为 。
Ⅱ.铅蓄电池使用量的急速增加引起铅污染日益严重,工业上从废铅蓄电池的铅膏回收铅的一种工艺流程如下:
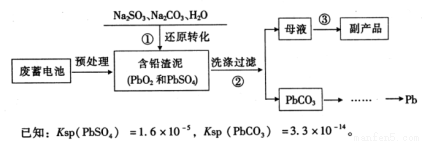
请回答下列问题:
(3)为提高步骤①的化学反应速率,你认为可采取的措施是 (写一条即可)。
(4)写出步骤①中PbSO4转化为PbCO3反应的平衡常数表达式:K = 。
(5)步骤①中发生氧化还原反应的化学方程式为 。
(6)步骤③从母液可获得的副产品为 (写化学式)。
(7)已知:PbCO3在一定条件下可制得PbO,PbO通过进一步反应可制得Pb,写出一个由PbO生成Pb的化学方程式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com