
����Ŀ����1����֪����2H2��g��+O2��g��=2H2O��l����H1=-571.6kJmol-1
��2CO��g��+O2��g��=2CO2��g����H2=-566.0kJmol-1
��CO��g��+2H2��g��![]() CH3OH��g����H3=-90.8kJmol-1
CH3OH��g����H3=-90.8kJmol-1
����״�������ȼ������H�� ��
��2�����ڿ��淴ӦC��S��+H2O��g��![]() CO��g��+H2��g����ƽ�ⳣ������ʽΪ �����жϸ÷�Ӧһ���ﵽ��ѧƽ��״̬�������� ������ѡ������
CO��g��+H2��g����ƽ�ⳣ������ʽΪ �����жϸ÷�Ӧһ���ﵽ��ѧƽ��״̬�������� ������ѡ������
A�������������ƽ����Է�����������ʱ����仯
B��v����H2O��=v����H2��
C��������������ܶȲ���ʱ����仯
D������������������ʱ����仯
E������n mol H2��ͬʱ����n mol CO
��3��ij��ѧ��ȤС��̽����������Ժϳɼ״���Ӧ��Ӱ�졣
CO��g��+2H2��g��![]() CH3OH��g����H=-91kJmol-1
CH3OH��g����H=-91kJmol-1
����300��ʱ�������Ϊ1L���ܱ������м���2mol H2��1mol CO��CO��CH3OH��g����Ũ����ʱ��仯��ͼ��ʾ��
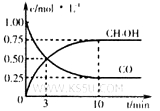
��ӷ�Ӧ��ʼ������ƽ�⣬v��H2��Ϊ ��
����������������ʱ��ֻ�ı����е�һ����������С��ͬѧ����ʵ���������ͼ����������ʵ������� �����������
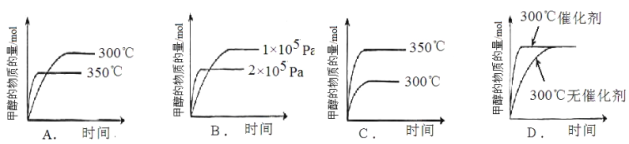
���𰸡�
��1����-763.8 kJ/mol��
��2��K=![]() ��ABC��
��ABC��
��3����0.15mol/Lmin����AD��
��������
�����������1����2H2��g��+O2��g��=2H2O��l����H1=-571.6kJmol-1��
��2CO��g��+O2��g��=2CO2��g����H2=-566.0kJmol-1��
��CO��g��+2H2��g��![]() CH3OH��g����H3=-90.8kJmol-1��
CH3OH��g����H3=-90.8kJmol-1��
���ݸ�˹����֪����+�ڡ�![]() -������CH3OH��g��+
-������CH3OH��g��+![]() O2��g��=CO2��g��+2H2O��l����
O2��g��=CO2��g��+2H2O��l����
��H=-��571.6+![]() ��566.0-90.8��kJ/mol=-763.8kJ/mol���ʴ�Ϊ��-763.8kJ/mol��
��566.0-90.8��kJ/mol=-763.8kJ/mol���ʴ�Ϊ��-763.8kJ/mol��
��2�����淴ӦC��S��+H2O��g��![]() CO��g��+H2��g����ƽ�ⳣ������ʽK=
CO��g��+H2��g����ƽ�ⳣ������ʽK=![]() ��A����Ӧǰ��������������ͬ�������������ƽ����Է����������ϼ�С����ƽ����Է�����������ʱ��仯���ﵽƽ��״̬����A��ȷ��B��������H2O��=������H2��ʱ�������Ũ�Ȳ��ٱ仯����Ӧ�ﵽƽ��״̬����B��ȷ��C����Ӧ��CΪ���壬��Ӧǰ�������������������ݻ����䣬��������
��A����Ӧǰ��������������ͬ�������������ƽ����Է����������ϼ�С����ƽ����Է�����������ʱ��仯���ﵽƽ��״̬����A��ȷ��B��������H2O��=������H2��ʱ�������Ũ�Ȳ��ٱ仯����Ӧ�ﵽƽ��״̬����B��ȷ��C����Ӧ��CΪ���壬��Ӧǰ�������������������ݻ����䣬��������![]() ��֪��������������ܶȲ�������������������ܶȲ���ʱ��仯ʱ��˵����Ӧ�ﵽƽ��״̬����C��ȷ��D�����������غ㶨�ɿ�֪����������������ʼ���ղ���ʱ����仯����D����E������n mol H2��ͬʱ����n mol CO����ʾ�Ķ����淴Ӧ�����ж����淴Ӧ�����Ƿ���ȣ���E���ʴ�Ϊ��K=
��֪��������������ܶȲ�������������������ܶȲ���ʱ��仯ʱ��˵����Ӧ�ﵽƽ��״̬����C��ȷ��D�����������غ㶨�ɿ�֪����������������ʼ���ղ���ʱ����仯����D����E������n mol H2��ͬʱ����n mol CO����ʾ�Ķ����淴Ӧ�����ж����淴Ӧ�����Ƿ���ȣ���E���ʴ�Ϊ��K=![]() ��A BC��
��A BC��
��3������300��ʱ�������Ϊ1L���ܱ������м���2mol H2��1mol CO��CO��CH3OH��g����Ũ����ʱ��仯��ͼ2��ʾ����ӷ�Ӧ��ʼ������ƽ�⣬ƽ��Ũ��c��CH3OH��=0.75mol/L��c��CO��=0.25mol/L���ﵽƽ��ʱ��Ϊ10min����
CO��g��+2H2��g��![]() CH3OH��g��
CH3OH��g��
��ʼ����mol/L�� 1 2 0
�仯����mol/L�� 0.75 1.5 0.75
ƽ������mol/L�� 0.25 0.5 0.75
v��H2��=![]() =0.15mol/Lmin���ʴ�Ϊ��0.15mol/Lmin��
=0.15mol/Lmin���ʴ�Ϊ��0.15mol/Lmin��
��CO��g��+2H2��g��![]() CH3OH��g����H=-91kJmol-1����Ӧ�Ƿ��ȷ�Ӧ��A��ͼ�����ȹ���ƽ���¶ȸߣ��¶�Խ�ߣ�ƽ��������У��״����ʵ�����С����A���ϣ�B��ͼ�����ȹ���ƽ��ѹǿ��Ӧ�����������С�ķ�Ӧ��ѹǿ����ƽ��������У��״����ʵ�������B�����ϣ�C������ƽ���ƶ�ԭ����֪�¶�Խ�ߣ�ƽ��������У��״����ʵ�����С��ͼ���ϣ���C�����ϣ�D����������ӿ췴Ӧ���ʣ����̴ﵽƽ���ʱ�䣬���ﵽƽ��״̬��ͬ����D���ϣ��ʴ�Ϊ��AD��
CH3OH��g����H=-91kJmol-1����Ӧ�Ƿ��ȷ�Ӧ��A��ͼ�����ȹ���ƽ���¶ȸߣ��¶�Խ�ߣ�ƽ��������У��״����ʵ�����С����A���ϣ�B��ͼ�����ȹ���ƽ��ѹǿ��Ӧ�����������С�ķ�Ӧ��ѹǿ����ƽ��������У��״����ʵ�������B�����ϣ�C������ƽ���ƶ�ԭ����֪�¶�Խ�ߣ�ƽ��������У��״����ʵ�����С��ͼ���ϣ���C�����ϣ�D����������ӿ췴Ӧ���ʣ����̴ﵽƽ���ʱ�䣬���ﵽƽ��״̬��ͬ����D���ϣ��ʴ�Ϊ��AD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����⻯��(NaBH4��Ϊ��ɫ��ĩ��������ˮ���⣬�����������(�۵㣺-101�����е㣺33�������ڸɿ������ȶ�����ʪ�����зֽ⣬�����ϳɺ��л��ϳ��г��õ�ѡ���Ի�ԭ����ij�о�С�����ƫ������(NaBO2��Ϊ��Ҫԭ���Ʊ�NaBH4�����������£�����˵������ȷ����( ��
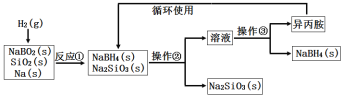
A��ʵ������ȡ����������Ҫ�õ���ʵ����Ʒ�����ӡ���ֽ������Ƭ��С��
B�����������������ֱ��ǹ����������ᾧ
C����Ӧ������֮ǰ�轫��Ӧ��������100�����ϲ�ͨ�����
D����Ӧ�����������뻹ԭ�������ʵ���֮��Ϊ1��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ��������������ȷ����
A. Ħ���ǹ��ʵ�λ���߸�����������֮һ
B. 1 L 0.1 mol/L BaCl2��Һ��������Cl��Ϊ0.1 NA
C. ���³�ѹ�£�11.2 L Cl2�����ķ�����Ϊ0.5 NA
D. ���³�ѹ�£�32 g O2���е���ԭ����Ϊ2 NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ӦN2+3H2![]() 2NH3�տ�ʼʱ��N2��Ũ��Ϊ3mol/L��H2��Ũ��5mol/L��3min����NH3Ũ��Ϊ0.6mol/L�����ʱ���ڣ����з�Ӧ���ʱ�ʾ��ȷ����( )
2NH3�տ�ʼʱ��N2��Ũ��Ϊ3mol/L��H2��Ũ��5mol/L��3min����NH3Ũ��Ϊ0.6mol/L�����ʱ���ڣ����з�Ӧ���ʱ�ʾ��ȷ����( )
A��v(NH3)=0.2mol/(L��min) B��v(N2)=1mol/(L��min)
C��v(H2)=1.67mol/(L��min) D��v(H2)=1.37mol/(L��min)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NAΪ����٤��������ֵ������˵����ȷ����
A. 100g��������Ϊ46%���Ҵ�ˮ��Һ����ԭ����ĿΪ12NA
B. 1L0.5mol/L��CH3COOH��Һ�к��е�H+��Ϊ0.5NA
C. ��״���£�0.2NA��SO3������ռ�е����ԼΪ4.48L
D. ����1molCl2���뷴Ӧʱ������ת����ĿΪ2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʽΪC6H12O2���Ժ�̼��������Һ��Ӧ���������ͬ���칹����
A��4�� B��8�� C��12�� D������12��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2.56gCu��һ������ŨHNO3��Ӧ������Cu�IJ��ϼ��٣���Ӧ�����������ɫ��dz����Cu ��Ӧ���ʱ�����ռ���������1.12L(��״��)����Ӧ������HNO3�����ʵ���Ϊ( )
A��0.05 mol B��1mol C��1.05mol D��0.13mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����᳦��ҩ����Ч�ɷ�M�ĺϳ�·�����������ַ�Ӧ��ȥ�Լ���������:
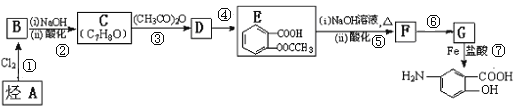
��֪����![]()
��![]()
��1����A��������______________��G�еĹ�����������_______________��
��2����Ӧ���ķ�Ӧ������__________����Ӧ���ķ�Ӧ������______________��
��3��E������NaOH��Һ��Ӧ�Ļ�ѧ����ʽ��______________��
��4����������������D��ͬ���칹����___________�֡����к˴Ź���������4����ҷ����֮��Ϊ6:2:1:1�Ľṹ��ʽ��______________��
�����ڷ����廯�����ұ�������3��ȡ����
���ܺ�NaHCO3��Һ��Ӧ��������
��5����֪![]() �ױ��������������������ʱ������һ��ȡ��������ȡ����������ڶ�λ���������ϵĺϳ�·�ߣ����һ����AΪԭ�Ϻϳɻ�����
�ױ��������������������ʱ������һ��ȡ��������ȡ����������ڶ�λ���������ϵĺϳ�·�ߣ����һ����AΪԭ�Ϻϳɻ�����![]() �ĺϳ�·��______________��
�ĺϳ�·��______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£����ڿ��淴ӦX��g��+3Y��g��![]() 2Z��g������X��Y��Z����ʼŨ�ȷֱ�Ϊ c1��c2��c3������Ϊ�㣩���ﵽƽ��ʱ��X��Y��Z��Ũ�ȷֱ�Ϊ0.1mol/L��0.3mol/L��0.08mol/L���������ж���ȷ���ǣ� ��
2Z��g������X��Y��Z����ʼŨ�ȷֱ�Ϊ c1��c2��c3������Ϊ�㣩���ﵽƽ��ʱ��X��Y��Z��Ũ�ȷֱ�Ϊ0.1mol/L��0.3mol/L��0.08mol/L���������ж���ȷ���ǣ� ��
A��c1��c2=3��1 B��ƽ��ʱ��Y��Z����������֮��Ϊ2��3
C��X��Y��ת������� D��c1��ȡֵ��ΧΪ0.04 mol/L��c1��0.14 mol/L
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com