



 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源:不详 题型:单选题
| A.用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率 |
| B.100mL2mol/L的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变 |
| C.升高体系的温度,活化分子的百分数增大,反应速率加快 |
D.在密闭容器中进行 N2 (g)+ O2(g)  2NO(g)的可逆反应,若温度不变压强不变,充入氦气则该反应的速率加快 2NO(g)的可逆反应,若温度不变压强不变,充入氦气则该反应的速率加快 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.加入适量的铝粉 | B.加入适量的水 |
| C.加入少量的硫酸铜溶液 | D.加入浓度较大的盐酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2Z(g)+W(s),△H<0的反应过程。若使a曲线变为b曲线,可采用的措施是
2Z(g)+W(s),△H<0的反应过程。若使a曲线变为b曲线,可采用的措施是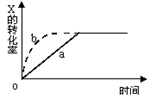
| A.增大体积 | B.增大Y的浓度 |
| C.降低温度 | D.缩小体积 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.只有②③④ | B.只有②④ | C.只有④ | D.全部 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
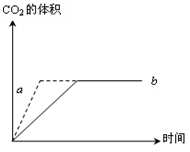
 ②如果实验过程中所用的盐酸是过量的,则所取块状石灰石与粉末状石灰石的质量是否相等?(填“相等”或“不相等”)。
②如果实验过程中所用的盐酸是过量的,则所取块状石灰石与粉末状石灰石的质量是否相等?(填“相等”或“不相等”)。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 实验过程 | 实验现象 | 结论 |
| 向盛有5 mL 5%的H2O2溶液的试管中滴入少量的 HCl,把带火星的木条伸入试管. | 无明显现象 | |
| 向盛有5 mL 5%的H2O2溶液的试管中滴入少量的Fe2(SO4)3,把带火星的木条伸入试管. | 试管中有大量气泡产生,带火星的木条复燃 | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.对于有气体参加的化学反应来说,增大压强,可使活化分子百分数增多,化学反应速率一定增大 |
| B.升高温度,活化分子百分数不变,但是碰撞的频率增大,所以化学反应速率增大 |
| C.增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增大 |
| D.加入正催化剂,可以降低该反应的活化能,会使反应物活化分子百分数增加,所以化学反应速率加快 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.100mL0.1mol/L盐酸 | B.100mL0.2mol/L硝酸 |
| C.75 mL0.2mol/L盐酸 | D.20mL18.4mol/L硫酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com