
| A、霾的形成与PM2.5有直接关系 |
| B、自行车钢架生锈主要是电化学腐蚀所致 |
| C、用加热的方法杀死H7N9禽流感病毒是采用了蛋白质变性原理 |
| D、人类在研究物质微观结构的过程中,扫描隧道显微镜、光学显微镜、电子显微镜先后得到了使用 |


科目:高中化学 来源: 题型:
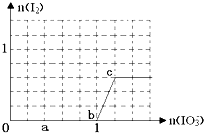 已知:还原性HSO3->I?,氧化性IO3->I2.在含3mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.下列不正确的是( )
已知:还原性HSO3->I?,氧化性IO3->I2.在含3mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.下列不正确的是( )| A、0-b:3HSO3-+IO3-═3SO42-+I-+3H+ |
| B、a点时消耗NaHSO3的物质的量为1.2mol |
| C、b-c间I2是还原产物 |
| D、当溶液中I?与I2的物质的量之比为5:2时,加入的KIO3为1.08mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| 高温高压 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、明矾用于净水:Al3++3H2O═Al(OH)3↓+3H+ |
| B、钢铁吸氧腐蚀的负极反应:Fe-3e-═Fe3+ |
| C、向明矾溶液中加入少量氢氧化钡溶液:Al3++SO42-+Ba2++3OH-═BaSO4↓+Al(OH)3↓ |
D、苯酚钠饱和溶液中通入少CO2: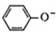 +CO2+H2O→ +CO2+H2O→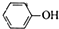 +HCO3- +HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
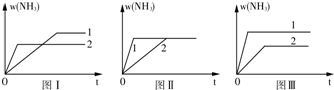
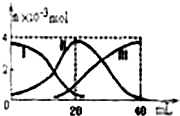 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中I代表H2A,Ⅱ代表HA-,Ⅲ代表A2-,横坐标表示加入NaOH的体积).根据图示判断,下列说法正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中I代表H2A,Ⅱ代表HA-,Ⅲ代表A2-,横坐标表示加入NaOH的体积).根据图示判断,下列说法正确的是( )| A、当V(NaOH)=40mL时,c(Na+)+c(H+)=2c(A2-)+c(OH-) |
| B、当V(NaOH)=20mL时,溶液中离子浓度大小关系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) |
| C、滴加过程中当溶液呈中性时,V(NaOH)<20mL |
| D、HA-的电离程度小于水解程度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应后溶液中ClO-的个数为0.1NA |
| B、原NaOH浓度为1mol/L |
| C、参加反应的氯气分子为0.1NA |
| D、转移电子为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
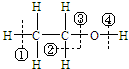 在化学反应中断键位置说法错误的是( )
在化学反应中断键位置说法错误的是( )| A、乙醇在铜催化下与氧气反应,在②④位置断裂,所以只有与羟基直接相连的碳原子上有氢原子才能发生催化氧化 |
| B、乙醇与钠反应,在④位置断裂 |
| C、乙醇与浓硫酸在140℃时,在③或④位置断裂,该反应属于取代反应 |
| D、乙醇与浓硫酸在170℃时,在②③位置断裂,以水分子的形式消去,属于消去反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com