
无水AlCl3可用作有机合成的催化剂、食品膨松剂等。
工业上由铝土矿(主要成分是A12O3和Fe2O3)和石油焦(主要成分是C)按下图所示流
|
|
|
| |||||||||||
 | |||||||||||
 | |||||||||||
|
|
|
(1)氯化铝在加热条件下易升华,气态氯化铝的化学式为Al2Cl6,每种元素的原子最外层均达到8电子稳定结构,则AlCl3是: ▲ 晶体,其结构式为: ▲ 。
(2)氯化炉中Al2O3、Cl2和C反应的化学方程式是 ▲ 。
(3)冷却器排出的尾气中含有大量CO和少量Cl2,需用Na2SO3溶液除去Cl2,此反应的离子方程式为: ▲ 。
(4)升华器中主要含有AlCl3和FeCl3,需加入少量Al,其作用是: ▲ 。
(5)AlCl3产品中Fe元素含量直接影响其品质,为测定产品中Fe元素的含量,现称取16.25g无水AlCl3产品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重残留固体质量为0.32g。则产品中Fe元素的含量为: ▲ 。
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源: 题型:
下列说法正确的是..........................................................................................
A.第ⅠA族的金属单质与水反应一定比第ⅡA族的金属单质剧烈
B.第二周期元素的最高正价和最低负价的绝对值之和等于8
C.同周期主族元素的原子形成简单离子的电子层结构相同
D.第ⅥA族元素的氢化物中,稳定性最好的其沸点也最高
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关说法正确的是
A.准确称取0.4000 g NaOH固体可配成100 mL 0.1000 mol·L-1的NaOH标准溶液
B.催化剂可以加快化学反应速率但不能改变化学反应的焓变
C.100 mL pH=3的HA和HB分别与足量的锌反应,HB放出的氢气多,说明HB酸性比HA弱
D.对于反应2SO2(g)+O2(g)  2SO3(g),压缩气体体积使压强增大(其他条件不变),则SO2的转化率增大,平衡常数K也增大
2SO3(g),压缩气体体积使压强增大(其他条件不变),则SO2的转化率增大,平衡常数K也增大
查看答案和解析>>
科目:高中化学 来源: 题型:

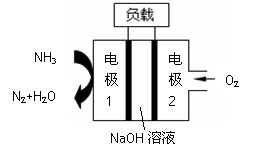
瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电
池示意图如右,有关说法正确的是
A.电池工作时,Na+ 向负极移动
B.电子由电极2经外电路流向电极1
C.电池总反应为:4NH3+3O2=2N2+6H2O
D.电极2发生的电极反应为:O2+ 4H + + 4e-=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
CaCl2常用于冬季道路除雪,建筑工业的防冻等,实验室常用作干燥剂。工业上常用大理石(含有少量Al3+、Fe2+、Fe3+等杂质)来制备。下图为实验室模拟其工艺流程:


已知:常温下,溶液中的Fe3+、Al3+、Fe2+以氢氧化物形式完全沉淀的pH分别为:3.7,4,9.7。
(1)反应Ⅰ中,需将大理石粉碎、搅拌,同时适当加热,其目的是: ▲ 。
写出反应Ⅰ中主要反应的离子方程式: ▲ 。
(2)上述使用盐酸的浓度为10%,若用37%的浓盐酸来配制500mL的此盐酸所需的玻璃仪器有:玻璃杯、量筒、烧杯、胶头滴管、 ▲ 。
(3)反应Ⅱ中的离子方程式: ▲ 。
(4)反应Ⅲ中必须控制加入Ca(OH)2的量,使溶液的pH约为8.0,此时沉淀a的成分为:
▲ ,若pH过大,则可能发生副反应的离子方程式: ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
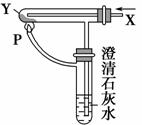
按右图装置通入X气体,并在管P处点燃,实验结果是澄清石灰水变浑浊,则X、Y可能是 ( )。
A.H2和Fe2O3
B.CO和CuO
C.H2 和Na2CO3
和Na2CO3
D.CO和Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列微粒半径大小比较正确的是:
A.Na+<Mg2+<Al3+<O2- B.S2->Cl->Na+>Al3+
C.Na<Mg<Al<S D.Ca<Rb<K<Na
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数,下列叙述中正确的是( )
A.14 g乙烯和丙烯的混合物中总原子数为3NA
B.常温下11.2 L甲烷气体含有甲烷分子数为0.5NA
C.5.6 g铁与足量的稀硫酸反应失去电子数为0.3 NA
D.0.1 mol·L-1的氢氧化钠溶液中含钠离子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.在水中能电离出离子的化合物一定是离子化合物
B.CO2分子中含极性键,且溶于水能导电,所以CO2是电解质
C.Ca(OH)2微溶于水,所以是弱电解质
D.CH3COOH在水中只能部分电离,所以是弱电解质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com