“温室效应”是哥本哈根气候变化大会研究的环境问题之一.CO
2是目前大气中含量最高的一种温室气体.因此,控制和治理CO
2是解决“温室效应”的有效途径.
(1)其中一种途径是将CO
2转化成有机物实现碳循环.如:
2CO
2(g)+2H
2O(l)═C
2H
4(g)+3O
2(g)△H=+1411.0kJ/mol
2CO
2(g)+3H
2O(l)═C
2H
5OH(1)+3O
2(g)△H=+1366.8kJ/mol
则由乙烯水化制乙醇反应的热化学方程式为
.
(2)在一定条件下,6H
2(g)+2CO
2(g)?CH
3CH
2OH(g)+3H
2O(g).
根据上表中数据分析:
温度(k)
CO2转化率(%)
|
500 |
600 |
700 |
800 |
| 1.5 |
45 |
33 |
20 |
12 |
| 2 |
60 |
43 |
28 |
15 |
| 3 |
83 |
62 |
37 |
22 |
①温度一定时,提高氢碳比
,CO
2的转化率
(填“增大”“减小”“不变”).
②该反应的正反应为
(填“吸”或“放”)热反应.
(3)一定条件下,将3molH
2和1molCO
2两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3H
2(g)+CO
2(g)?CH
3OH(g)+H
2O(g).2min末该反应达到平衡,测得CH
3OH的浓度为0.2mol/L.下列判断不正确的是
.
a.该条件下此反应的化学平衡常数表达式为K=
| c(CH3OH)?c(H2O) |
| c3(H2)?c(CO2) |
b.H
2的平均反应速率为0.3mol/(L?s)
c.CO
2的转化率为60%
d.若混合气体的密度不再改变时,该反应一定达到平衡状态
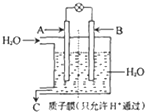
(4)科技人员设想以如图所示装置及电化学原理,将CO
2和H
2转化为甲醇.若A处通入CO
2,B处通入H
2,C为CH
3OH
①B极为
极
②A极的电极反应式为
(5)CO
2在自然界循环时可与CaCO
3反应,CaCO
3是一种难溶物质,已知常温下,其溶解度为1.2×10
-3g,则其Ksp为
.

 “温室效应”是哥本哈根气候变化大会研究的环境问题之一.CO2是目前大气中含量最高的一种温室气体.因此,控制和治理CO2是解决“温室效应”的有效途径.
“温室效应”是哥本哈根气候变化大会研究的环境问题之一.CO2是目前大气中含量最高的一种温室气体.因此,控制和治理CO2是解决“温室效应”的有效途径.

 阅读快车系列答案
阅读快车系列答案 和
和 D、35Cl和37Cl E、乙醇和乙二醇
D、35Cl和37Cl E、乙醇和乙二醇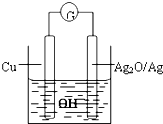 普通水泥在固化过程中自由水分子减少,并且溶液呈碱性.根据这一物理化学特点,科学家发明了电动势法测水泥初凝时间.此法的原理如图所示,反应的总方程式为:2Cu+Ag2O=Cu2O+2Ag,下列有关说法正确的是( )
普通水泥在固化过程中自由水分子减少,并且溶液呈碱性.根据这一物理化学特点,科学家发明了电动势法测水泥初凝时间.此法的原理如图所示,反应的总方程式为:2Cu+Ag2O=Cu2O+2Ag,下列有关说法正确的是( )