
【题目】已知: A 用于医疗消毒, C 为常用调味品; E 与 B 都能发生银镜反应, E 的相对分子质量比 B 大 12,请回答:
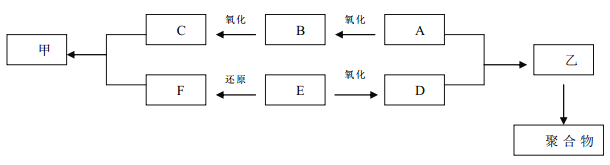
(1)求 E 的结构简式_______;乙生成聚合物的反应类型_______。
(2)C 生成甲的方程式_______。
(3)下列说法不正确的是________。
A. 物质 A 与金属钠反应比水与金属钠反应要剧烈
B. 用蒸馏的方法分离物质 A 与 C 可得到纯净的 A
C. 根据溴水褪色现象,可以证明物质 E 中一定存在碳碳双键
D.新制碱性氢氧化铜悬浊液可鉴别物质 A、 B 和 C
【答案】 CH2=CHCHO 加聚反应 CH3COOH + CH3CH2CH2OH![]() CH3COOCH2CH2CH3 + H2O ABC
CH3COOCH2CH2CH3 + H2O ABC
【解析】试题分析: A 用于医疗消毒,则A为乙醇; A经两步氧化得到的C 为常用调味品,则C为醋酸、B为乙醛;E可还原为F、氧化为D, E 与 B 都能发生银镜反应, E的相对分子质量比 B 大 12,则E为丙烯醛、F为1-丙醇、D为丙烯酸、乙为丙烯酸乙酯,乙为发生加聚反应生成聚合物—聚丙烯酸乙酯。
(1)E的结构简式CH2=CHCHO;乙生成聚合物的反应类型加聚反应。
(2)C 生成甲的方程式CH3COOH + CH3CH2CH2OH![]() CH3COOCH2CH2CH3 + H2O。
CH3COOCH2CH2CH3 + H2O。
(3)下列说法:A.物质 A 与金属钠反应比水与金属钠反应要缓慢,A不正确;B. A和C都是易挥发的液体,所以用蒸馏的方法分离物质 A 与 C 无法得到纯净的A,B不正确;C.含有醛基的物质也能使溴水褪色,所以根据溴水褪色现象,不能证明物质 E 中一定存在碳碳双键,C不正确;D.乙醇不与新制碱性氢氧化铜悬浊液反应,乙酸可以使新制碱性氢氧化铜悬浊液变澄清,乙醛与新制碱性氢氧化铜悬浊液共热后可以生成砖红色的沉淀,所以,新制碱性氢氧化铜悬浊液可鉴别物质 A、 B 和 C,D正确。综上所述,不正确的是ABC。


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】在2 L容积不变的容器中,发生N2+3H2 NH3的反应。现通入4 mol H2和4 mol N2,10 s内用H2表示的反应速率为0.12 mol·L-1·s-1,则10 s后容器中N2的物质的量是( )
A. 1.6 mol B. 2.8 mol C. 3.6 mol D. 3.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明:H2O2具有立体结构,两个氢原子像在一本半展开的书的两页纸上,两页纸面的夹角为94°,氧原子在书的夹缝上,O—H键与O—O键之间的夹角为97°。下列说法不正确的是( )
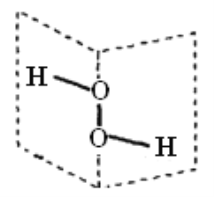
A. H2O2分子中既含极性键,又含非极性键
B. H2O2为极性分子
C. H2O2分子中的两个O原子均是sp3杂化
D. H2O2分子中既有σ键,又有π键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,不同酸性条件下的0.1 mol·L-1 HF溶液中,c(HF)、c(F-)与溶液pH的变化关系如图所示。下列说法正确的是

A. 随着溶液pH增大,![]() 不断增大
不断增大
B. 由水电离出的c(H+):Q>X=Y
C. HF的电离常数Ka=1.0×10-3.2
D. 0.1 mol/LNaF溶液的pH约为8.2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室做钠和水反应的实验时,下列关于实验现象的描述错误的是
A.钠浮在水面上四处游动B.钠溶成小球,并且伴有“嘶嘶”声音
C.向反应后的溶液中加入酚酞,溶液颜色变红D.反应中有大量白色沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合金在生活、生产、国防等领域有广泛应用。镍是重要的合金元素,例如镧镍合金、白铜(铜镍合金)、铝镍合金等。
(1)基态镍原子的外围电子排布式为_____________。
(2)在NiSO4溶液中滴加稀氨水能形成配位化合物[Ni(NH3)4]SO4。
①H、N、O、Ni的电负性大小顺序为______________________。
②与SO42—互为等电子体的分子(写出一种即可)______________。
③SO32—、SO42—中S的杂化类型都是___________;但它们的实际空间构型却不同,其主要原因是________________________________________________________________。
(3)工业上,采用反应Ni(s)+4CO(g)![]() Ni(CO)4(g)提纯粗镍。推测Ni(CO)4晶体中存在的作用力有__________。
Ni(CO)4(g)提纯粗镍。推测Ni(CO)4晶体中存在的作用力有__________。
a、范德华力 b、配位键 c、非极性键 d、极性键 e、离子键
(4)镧镍合金的晶胞如图1所示,镍原子除了1个在体心外,其余都在面上。该合金中镍原子和镧原子的个数比为________。
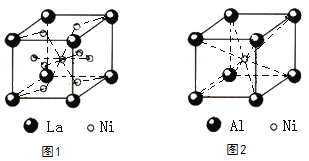
(5)铝镍合金的晶胞如图2所示。已知:铝镍合金的密度为ρg/cm3,NA代表阿伏加德罗常数的数值,则镍、铝的最短核间距(d)为________________pm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温常压下,在带有相同质量活塞的容积相等的甲、乙两容器里,分别充有二氧化氮和空气,分别进行下列两项实验:
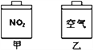
(a)将两容器置于沸水中加热
(b)在活塞上都加2 kg的砝码
已知:N2O4(g)![]() 2NO2(g) △H>0在以上两情况下,甲和乙容器的体积大小,正确的是
2NO2(g) △H>0在以上两情况下,甲和乙容器的体积大小,正确的是
A. (a)甲>乙,(b)甲>乙 B. (a)甲>乙,(b)甲=乙
C. (a)甲<乙,(b)甲>乙 D. (a)甲>乙,(b)甲<乙
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com