
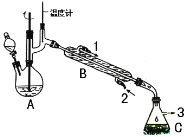
【题目】在有机反应中加氧去氢的反应叫氧化反应,去氧加氢的反应叫还原反应,如乙烯与氢气的加成反应也叫还原反应。1-苯乙醇因具有玫瑰香气味而广泛用于各种食用香精中,实验室用苯乙酮制备1-苯乙醇的反应、装置示意图和有关数据如下:

试剂[ | 熔点/℃[ | 沸点/℃ | 密度/g·cm-3 | 溶解性 | ||
水 | 乙醇 | 乙醚 | ||||
1-苯乙醇 | 20 | 203.4 | 1.013 | 不溶 | 溶 | 溶 |
苯乙酮 | 19.7 | 202.3 | 1.028 | 不溶 | 溶 | 溶 |
硼氢化钠 | 36 | 400 | 1.076 | 溶 | 溶 | 不溶 |
乙醇 | -117.3 | 78.4 | 0.789 | 溶 | - | 溶 |
乙醚 | -116.3 | 34.6 | 0.713 | 微溶 | 溶 | - |
实验步骤:
在A中加入15mL 95%的乙醇和1.0g硼氢化钠,搅拌下再滴入8mL苯乙酮,然后在搅拌的条件下,滴加足量的3mol·L-1的盐酸;使A中反应液的温度保持在75-80℃,使其中大部分乙醇蒸发,出现分层,再加入10mL乙醚。将混合反应液倒入分液漏斗中分液,水层再用10mL乙醚萃取,合并两次有机相,再进行简单蒸馏除去乙醚。最后经提纯收集到1-苯乙醇4.5g。
回答下列问题:
(1) 苯乙酮制备1-苯乙醇的反应类型是 ;
(2)仪器B的名称为______________;
(3)反应完成后,加入10mL乙醚,充分振荡后,上层为__________(填“水层”或“有机层”)
(4)反应中加入乙醇的目的是________________________________;
(5)两次合并的有机相进行蒸馏除去乙醚,采用的最佳加热方式是_________(填字母),若回收乙醚,则收集馏分的温度范围是____________________;
a.酒精为加热 b.水浴加热 c.油浴加热 d.酒精喷灯加热
(6)本实验的产率为_____________(保留两位有效数字)。
(7) 1-苯乙醇除用作香料外也用于有机合成,如1-苯乙醇与冰醋酸酯化反应制得乙酸苏合香酯,写出此反应化学反应方程式______________________________。
【答案】(1) 还原反应;(2)直形冷凝管;(3)有机层;(4)溶解硼氢化钠使反应物充分接触,加快反应速率; (5)b ;33~37℃;(6)54%;
(7) CH3COOH+ 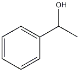
![]()
 +H2O
+H2O
【解析】
试题分析:(1)由苯乙酮制备1-苯乙醇的反应中羰基加氢发生了还原反应,故答案为:还原反应;
(2)仪器B是直形冷凝管,故答案为:直形冷凝管;
(3) 根据表中有机物密度分析,乙醚的密度小于水,其它有机物密度大于水,所以反应完成后,加入10mL乙醚,充分振荡后,上层为有机层,故答案为:有机层;
(4) 根据题中信息,苯乙酮不溶于水易溶于乙醇,要使硼氢化钠与苯乙酮充分反应,就要使它们能充分接触,所以用乙醇可以溶解硼氢化钠和苯乙酮,使反应物充分接触,故答案为:溶解硼氢化钠和苯乙酮,使反应物充分接触,加快反应速率;
(5) 乙醚的沸点只有34.6℃,所以可以用水浴加热的方式,若回收乙醚,则收集馏分的温度范围是35℃附近,故答案为:b ;33~37℃;
(6) 8mL苯乙酮的质量为8mL×1.028g/mL=8.224g,完全反应生成1-苯乙醇的质量为8.224g×![]() =8.361g,产率为
=8.361g,产率为![]() ×100%=54%,故答案为:54%;
×100%=54%,故答案为:54%;
(7) 1-苯乙醇与冰醋酸酯化反应制得乙酸苏合香酯,此反应化学反应方程式为CH3COOH+ 
![]()
 +H2O,故答案为:CH3COOH+
+H2O,故答案为:CH3COOH+ 
![]()
 +H2O。
+H2O。


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,在容积为V L的密闭容器中进行aN(g)![]() bM(g)的放热反应,M、N物质的量随时间的变化曲线如图所示:
bM(g)的放热反应,M、N物质的量随时间的变化曲线如图所示:

(1)此反应的化学方程式中=______。
(2)t2时两线交叉点__平衡状态(填“是”或“不是”),v正__v逆(填“>”“<” 或“=”)。
(3)此反应达到平衡时,反应物的转化率为____________。
(4)下列描述能说明上述反应达到平衡状态的是__________。
①反应中M与N物质的量之比为2∶5 ②混合气体的总物质的量不随时间的变化而变化③M的转化率达到最大 ④如容器为绝热容器,体系内温度不再变化
II某温度时,把1 mol N2O4气体通入体积为10 L的真空密闭容器中,立即出现红棕色[因为发生N2O4(无色)![]() 2NO2(红棕色)的反应],反应进行4 s时,NO2的浓度为0.04mol·L-1,再经过一段时间后反应达到平衡状态,这时容器内压强为开始时的1.8倍,则
2NO2(红棕色)的反应],反应进行4 s时,NO2的浓度为0.04mol·L-1,再经过一段时间后反应达到平衡状态,这时容器内压强为开始时的1.8倍,则
(1)前4 s以N2O4浓度变化表示的平均反应速率为 。
(2)在4 s末时容器内的压强是开始时的 倍。
(3)平衡时容器内NO2的浓度是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学—选修5:有机化学基础】H可作为溶剂,用于制造油漆、粘合剂和除漆剂等。下图是合成H和高聚物M的一种合成路线:
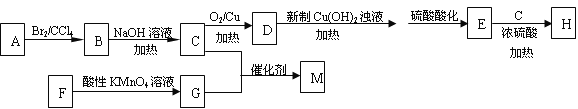
已知以下信息:
①A的产量可以用来衡量一个国家的石油化工发展水平。
②H分子结构中含有六元环。
③烃F相对分子质量为106,可以使酸性高锰酸钾溶液褪色,但不能使溴的CCl4溶液褪色。
④核磁共振氢谱显示F分子结构中只有两种化学环境的氢。
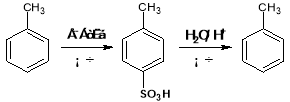
⑤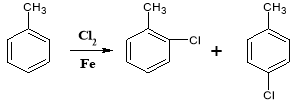 ;
;
回答下列问题:
(1)由C生成D的化学方程式为 ,反应类型为
(2)H的化学名称是 ,由C、G生成M的化学方程式:
(3)F的结构简式为
(4)同时满足下列条件G的同分异构体有 种(不考虑立体异构)。
①能与Na2CO3溶液反应生成无色无味气体
②遇FeCl3溶液发生显色反应
其中核磁共振氢谱中有4组峰,且面积比为1:2:2:1的结构简式是_______。
(5)上述由F的同分异构体X经如下步骤可合成 。
。
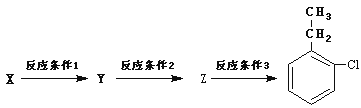
反应条件1所选择的试剂为 ;反应条件2所选择的试剂为 ;Z的结构简式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米氧化亚铜在水的光解等领域具有极大应用潜能,是极具开发前景的绿色环保光催化剂。目前主要的合成方法有电解法、高温固相法等。
(1)有研究表明阳极氧化法成功制得了Cu2O 纳米阵列,装置如图:
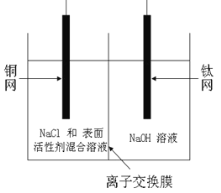
该电池的阳极反应方程式为 离子交换膜为_______(填阳或阴)离子交换膜,铜网应连接电源的_____极。
(2)在高温下用甲烷将粉状CuO 还原也可制得Cu2O。
已知:①2Cu(s)+1/2O2(g)=Cu2O(s);△H = -169kJ/mol
②CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H = -846.3 kJ/mol
③ Cu(s)+1/2O2(g)=CuO(s);△H = -157 kJ/mol
则该反应的热化学方程式是:__________。
(3)在相同的密闭容器中,用等质量的三种纳米Cu2O(用不同方法制得)分别进行催化分解水的实验:2H2O(g) ![]() 2H2(g)+O2(g) △H>0。水蒸气浓度随时间t变化如下表所示:
2H2(g)+O2(g) △H>0。水蒸气浓度随时间t变化如下表所示:
序号 |
| 0 | 10 | 20 | 30 | 40 | 50 |
① | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
② | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
③ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
①对比实验的温度:T2 T1(填“﹥”“﹤”或“﹦”),原因是___________________。
②实验①前20 min的平均反应速率 v(O2)=
③比较不同方法制得的Cu2O的催化效果应选用__________组实验,原因是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂电池应用很广,某种锂离子电池,其正极材料可再生利用。其正极材料有钴酸锂(LiCoO2)、导电剂乙炔黑和铝箔等。充电时,该锂离子电池负极发生的反应为6C+xLi++xe-=LixC6,现欲利用以下工艺流程回收正极材料中的某些金属资源(部分条件未给出)。
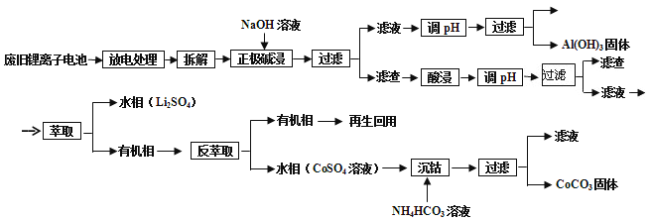
回答下列问题:
(1)写出“正极碱浸”中发生反应的化学方程式____________;
(2)“酸浸”一般在80℃下进行,写出该步骤中发生的主要氧化还原反应的化学方程式________________________;如果可用盐酸代替H2SO4和H2O2的混合溶液,可能发生反应的离子方程式___________________________;
(3)写出“沉钴”过程中发生反应的化学方程式______________________________;
(4)充放电过程中,发生LiCoO2与Li1-xCoO2之间的转化,写出充电时正极的电极反应_____________________________________;
(5)在整个回收工艺中,可回收到的金属化合物有____________(填化学式);
(6)最近美国和韩国的科学家合作研究出新型锂—空气电池,他们的锂—空气电池在放电过程中产生稳定的晶状超氧化锂(LiO2),超氧化锂可以很容易地分解成锂和氧,从而具有更高的效率和更长的循环寿命。请写出该电池正极的电极反应 ____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,属于同位素的是(填序号,下同) ,属于同素异形体的是 ,互为同系物的是 ,属于同分异构体的是 ,属于同种物质的是 。
A.O2和O3 B.D和T C.![]()
D.![]() E.
E.

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇、甲醚是被广泛使用的新型清洁燃料,工业生产乙醇的一种反应原理为:
2CO(g)+4H2(g)![]() CH3CH2OH(g)+H2O(g) △H=-256.1kJmol-1。
CH3CH2OH(g)+H2O(g) △H=-256.1kJmol-1。
已知:H2O(l)=H2O(g)△ H=+44kJmol-1 CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=-41.2kJmol-1
CO2(g)+H2(g) △H=-41.2kJmol-1
(1)以CO2(g)与H2(g)为原料也可合成乙醇,其热化学方程式如下:
2CO2(g)+6H2(g)![]() CH3CH2OH(g)+3H2O(l) △H=__________________kJmol-1
CH3CH2OH(g)+3H2O(l) △H=__________________kJmol-1
(2)把2molH2和1molCO通入1L的反应器中,一定条件下发生反应:
2CO(g)+4H2(g)![]() CH3OCH3(g)+H2O(g)△H,其CO的平衡转化率随温度、压强变化关系如图所示。
CH3OCH3(g)+H2O(g)△H,其CO的平衡转化率随温度、压强变化关系如图所示。
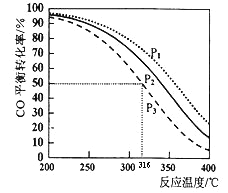
①以下能说明2CO(g)+4H2(g)![]() CH3OCH3(g)+H2O(g)达平衡状态的是___________
CH3OCH3(g)+H2O(g)达平衡状态的是___________
A.密度不再变化
B.CH3CH2OH蒸汽的体积分数不再变化
C.c(CO)/c(H2)不变
D.[c(CH3OCH3)c(H2O)]/[c(CO)c(H2)]不变
②图中的压强大小为: ,△H___________0(填“>”“<”或“=”),若在P3和316℃时,测得容器中n(H2)=n(CH3OCH3),此时反应的v(正)______v(逆)(填“>”“<”或“=”)。
③P3和316℃时反应的平衡常数________________
(3)汽车使用乙醇汽油并不能更加有效减少NOx的排放,气缸中生成NO的反应为:
N2(g)+O2(g)![]() 2NO(g) △H>0
2NO(g) △H>0
①汽车启动后,气缸内温度越高,单位时间内NO排放量越大,原因是_________________
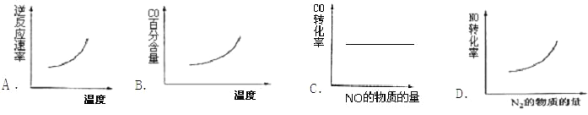
②汽车尾气净化中的一个反应如下:2NO(g)+2CO(g)![]() N2(g)+2CO2(g)△H=-746.8kJ/mol-1。在恒容的密闭容器中,反应达到平衡后,改变某一条件,下列示意图正确的是_______
N2(g)+2CO2(g)△H=-746.8kJ/mol-1。在恒容的密闭容器中,反应达到平衡后,改变某一条件,下列示意图正确的是_______
(4)乙醇-空气燃料电池中使用的电解质是搀杂了Y2O3的ZrO2晶体,它在高温下能传导O2-离子。该电池负极的电极反应式为__________________。用该电池为Pb+PbO2+2H2SO4![]() 2PbSO4+2H2O充电,充电一段时间后(假定两极充电前质量相等),测得两极质量差为6.4g时,通过电路电子的物质的量为__________________。
2PbSO4+2H2O充电,充电一段时间后(假定两极充电前质量相等),测得两极质量差为6.4g时,通过电路电子的物质的量为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用少量的溴水和足量的乙醇制备1,2-二溴乙烷的装置如下图所示:
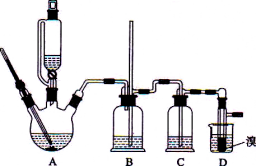
有关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g · cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -l30 | 9 | -1l6 |
回答下列问题:
(1)烧瓶A中发生的主要的反应方程式_____________________。
(2)装置B的作用是_____________________。
(3)在装置C中应加入___________(填字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(4)若产物中有少量未反应的Br2,最好用________(填字母)洗涤除去。
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇 e.Na2SO3溶液
(5)若产物中有少量副产物乙醚.可用_______________的方法除去。
(6)反应过程中应用冷水冷却装置D,但又不能过度冷却(如用冰水),其原因是_______________。
(7)判断该制备反应已经结束的最简单方法是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃A 0.2 mol 在氧气中完全燃烧后,生成CO2和H2O各1.2 mol。试回答:
(1)烃A的分子式为_____________。
(2)若取一定量的烃A完全燃烧后,生成CO2和H2O各3 mol,则有________g烃A参加了反应,燃烧时消耗标准状况下的氧气___________L。
(3)若烃A不能使溴水褪色,但在一定条件下能与氯气发生取代反应,其一氯取代物只有一种,则烃A的结构简式为__________________。
(4)若烃A能使溴水褪色,在催化剂作用下,与H2加成,其加成产物经测定分子中含有4个甲基,烃A可能有的结构简式为__________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com