
【题目】空气的主要污染物为硫的氧化物和氮的氧化物。研究人员设计了同时净化废气中二氧化硫和氮的氧化物的方法,将其转化为硫酸和硝酸,工艺流程如下:

各室中发生的反应如下:
氧化室:NO2+SO2+H2O==H2SO4+NO
清除室:NO+NO2==N2O3、N2O3+2H2SO4==2NOHSO4(固体)+H2O
分解室:4NOHSO4(固体)+O2+2H2O==4H2SO4+4NO2
(1)物质①和②分别为(填化学式)________、__________。
(2)写出SO2、O2与H2O反应生成H2SO4的化学方程式:_____________________。
 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:
【题目】在一个容积为2L的密闭容器中,加入0.8mol A2气体和0.6mol B2气体,一定条件下发生如下反应:A2(g)+B2(g)═2AB(g)△H<0,反应中各物质的浓度随时间的变化情况如图所示.下列说法正确的是( ) 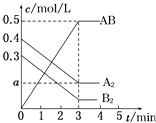
A.图中a点的值为0.05
B.该反应的平衡常数K=0.03
C.平衡时A2的转化率为62.5%
D.温度升高,平衡常数K值增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年IUPAC命名117号元素为TS(中文名![]() ,tián),TS的原子核外最外层电子数是7.下列说法不正确的是( )
,tián),TS的原子核外最外层电子数是7.下列说法不正确的是( )
A. TS是第七周期第ⅦA族元素 B. TS的同位素原子具有相同的电子数
C. TS在同族元素中非金属性最弱 D. 中子数为176的TS核素符号是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关有机物A描述中正确的是( ) 
A.A分子中含有2个手性碳原子
B.A分子核磁共振氢谱有6种峰
C.0.1mol 有机物A能与足量的金属钠反应放出0.1mol氢气
D.A能发生的反应类型有:加成、取代、氧化、酯化、消去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究铜及其化合物的性质对科研、生产生活有重要的意义.
(1)铜可采用如下方法制备
①火法炼铜:Cu2S+O2![]() 2Cu+SO2
2Cu+SO2
②湿法炼铜:CuSO4+Fe═FeSO4+Cu
上述两种方法中,铜元素均被 (填“氧化”或“还原”)成铜单质,若用①法每制得32gCu,转移电子的物质的量是 .
(2)在潮湿的空气中铜可以发生电化学腐蚀,生成铜绿,铜绿的化学式为 发生腐蚀的正极反应式为 ,由铜和锌组成的黄铜合金不易生锈,其防腐蚀的方法是 .
(3)①Li﹣﹣CuO电池总反应为:2Li+CuO═Li2O+Cu.电解质溶液为高氯酸锂有机溶液,电池的正极反应式为 .
②Cu2O是一种半导体材料,可在碱性溶液中用电解法制取,电解总反应式为:
2Cu+H2O![]() Cu2O+H2↑,阳极反应式为 ;Cu2O投入稀硫酸中,得到蓝色溶液和红色沉淀,写出该反应的离子方程式 .
Cu2O+H2↑,阳极反应式为 ;Cu2O投入稀硫酸中,得到蓝色溶液和红色沉淀,写出该反应的离子方程式 .
(4)为了回收粗铜精炼后阳极泥中的Ag和Au,某实验小组查阅了有关资料如下表:
编号 | 常温下反应 | 化学平衡常数 |
反应甲 | Au+6HNO3Au(NO3)3+3NO2↑+3H2O | <10﹣5 |
反应乙 | Au3++4Cl﹣[AuCl4]﹣ | >105 |
从资料中可知,常温下金很难与硝酸反应,但却可溶于王水(浓硝酸与浓盐酸体积比为l:3的混合物).请你运用化学平衡移动原理,简要说明金能溶于王水的原因 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( ) 
A.W元素的第一电离能小于Y元素的第一电离能
B.Y、Z的阴离子电子层结构都与R原子的相同
C.p能级未成对电子最多的是Z元素
D.X元素是电负性最大的元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(1)已知:N2(g)+O2(g)=2NO(g) △H=+180.5kJ/mol
N2(g)+3H2(g) ![]() 2NH3(g) △H=-92.4kJ/mol
2NH3(g) △H=-92.4kJ/mol
2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ/mol
写出氨气催化氧化生成一氧化氮气体和水蒸气的热化学反应方程式。
(2)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对N2(g)+3H2(g) ![]() 2NH3(g)反应的影响,实验结果如图所示:(图中T表示温度,n表示物质的量)
2NH3(g)反应的影响,实验结果如图所示:(图中T表示温度,n表示物质的量)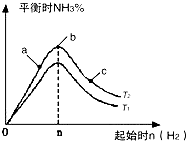
①图象中T2和T1的关系是:T2T1(填“高于”、“低于”、“等于”、“无法确定”).
②若比较在a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是(填字母).
(3)N2O5是一种新型硝化剂,其性质和制备受到人们的关注。一定温度下,在恒容密闭容器中N2O5可发生下列反应:2N2O5(g) ![]() 4NO2(g) + O2(g).△H﹥0,下表为反应在T1温度下的部分实验数据:
4NO2(g) + O2(g).△H﹥0,下表为反应在T1温度下的部分实验数据:
| 0 | 500 | 1000 |
| 5.00 | 3.52 | 2.48 |
①500s内NO2的平均生成速率为。
②该反应的化学平衡常数表达式为。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com