
【题目】3.87克锌铜合金完全溶解于150mL、密度为1.20g/cm3、质量分数为21%的稀硝酸中,得到NO气体896mL (标准状况),向反应后的溶液中加入适量的1.0mol/LNaOH溶液,恰使溶液中的金属离子全部沉淀。下列说法不正确是
A. 该稀硝酸中HNO3的物质的量浓度是4.0mol/L
B. 加入NaOH溶液的体积是560mL
C. 被还原的硝酸的物质的量为0.04mol
D. 得到的金属氢氧化物的沉淀为5.81克
【答案】D
【解析】试题分析:A.密度为1.40g/cm3、质量分数为63%的浓硝酸的物质的量浓度=![]() mol/L=4mol/L,故A正确;B.加入适量的1.0mol/L NaOH溶液,恰使溶液中的金属离子全部沉淀,此时溶液中溶质为NaNO3,由N元素守恒可知n(NaNO3)+n(NO2)=n(HNO3),则n(NaNO3)=0.15L×4mol/L-
mol/L=4mol/L,故A正确;B.加入适量的1.0mol/L NaOH溶液,恰使溶液中的金属离子全部沉淀,此时溶液中溶质为NaNO3,由N元素守恒可知n(NaNO3)+n(NO2)=n(HNO3),则n(NaNO3)=0.15L×4mol/L-![]() =0.56mol,由钠离子守恒n(NaOH)=n(NaNO3)=0.56mol,故需要1.0mol/L NaOH溶液体积为
=0.56mol,由钠离子守恒n(NaOH)=n(NaNO3)=0.56mol,故需要1.0mol/L NaOH溶液体积为![]() =0.56L=560mL,故B正确;C.被还原的硝酸生成NO气体,根据N原子守恒可知,起氧化剂的硝酸的物质的量=
=0.56L=560mL,故B正确;C.被还原的硝酸生成NO气体,根据N原子守恒可知,起氧化剂的硝酸的物质的量=![]() =0.04mol,故C正确;D.由电荷守恒可知,氢氧化物中氢氧根的物质的量等于转移电子物质的量,即氢氧根的物质的量为0.04mol×(5-2)=0.12mol,故氢氧化物质量=3.87g+0.12mol×17g/mol=5.91g,故D错误,故选D。
=0.04mol,故C正确;D.由电荷守恒可知,氢氧化物中氢氧根的物质的量等于转移电子物质的量,即氢氧根的物质的量为0.04mol×(5-2)=0.12mol,故氢氧化物质量=3.87g+0.12mol×17g/mol=5.91g,故D错误,故选D。


科目:高中化学 来源: 题型:
【题目】将浓度为2c mol·L-1、质量分数为a%的氨水,加水稀释至浓度为c mol·L-1,质量分数变为b%。则a、b之间的大小关系为 ( 已知:氨水的浓度越大密度越小 )
A. a=2b B. 2b>a>b C. a>2b D. 不能比较
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1L 0.1mol/L AgNO3溶液在以Ag作阳极,Fe作阴极的电解槽中电解,当阴极上增重2.16g时,下列判断中正确的是( )
A.溶液的浓度变为0.08mol/L
B.阳极上产生112ml O2 (标准状况)
C.转移的电子数是1.204×1022 个
D.反应中有0.01mol Ag 被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程所放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃用品是________________。
(2)烧杯间填满碎纸条的作用__________________。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 ___________(“偏大、偏小、无影响”)
(4)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 ________( “变多”“变少”“不变”),所求中和热_______(“相等、不相等”)
(5)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会_____________(“偏大”、“偏小”、“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积为V L的密闭容器中通入amolCO和bmolO2,一定条件下反应后容器内碳原子数和氧原子数之比为
A. a︰b B. a︰2b C. a︰(a+2b) D. a︰2(a+2b)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应3A(g)![]() 3B(?)+C(?);达到平衡时,混合气体的平均相对分子质量
3B(?)+C(?);达到平衡时,混合气体的平均相对分子质量![]() 与温度的关系如图所示,下列判断中正确的是
与温度的关系如图所示,下列判断中正确的是
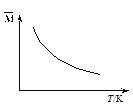
A. 若正反应吸热,则B、C可能都是气体
B. 若正反应吸热,则B、C一定都是气体
C. 若正反应放热,则B、C一定都是气体
D. 若正反应放热,则B、C可能都是固体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com