
����Ŀ������������գ�
��1���������ʣ����������ƹ��� ��ͭ˿ ���Ȼ������� ��ϡ���� ��CO2����ް�ˮ ��̼�����Ʒ�ĩ �����Ǿ��� �������Ȼ��� ���������ƹ��壮 ���������գ�����״̬���ܵ������ �� ���ڵ���ʵ��� �� ���ڷǵ���ʵ��� �� ������ˮ��������ķ���ʽΪ �� ��̼��������Һ�еμӼ��γ���ʯ��ˮ��������Ӧ�����ӷ���ʽΪ ��
��2���õ����ű������ת�Ƶķ������Ŀ��KClO3+6HCl��Ũ��=KCl+3Cl2��+3H2O �� �÷�Ӧ����������ͻ�ԭ�����������Ϊ �� �����6.72L Cl2����״�������ɣ���Ӧ��ת�Ƶ��ӵĸ���Ϊ
��3������ʯ���̱�ʯ���������Ҫ��ѧ�ɷ�ΪBenAl2Si6O18 �� ������������ʽ��ʾΪnBeOAl2O36SiO2 �� ��nֵΪ���������˽��ơ���������������������Ƴɣ�������ijɷֿɼ�����Ca2Mg5Si8O22��OH��2 �� ���仯ѧʽ��д����������ʽΪ ��
���𰸡�
��1���ڢܢޢ�٢ۢߢ�⣻�ݢࣻ NaHSO4=Na++H++SO42���� Ca2++2OH��+2HCO3��=CaCO3��+2H2O+CO32��
��2��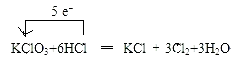 ��5��1��0.5NA
��5��1��0.5NA
��3��3��2CaO?5MgO?8SiO2?H2O
���������⣺��1�����������ƹ��岻�����ɵ��ӻ��������ƶ������ӣ������磬��ˮ��Һ�л�����״̬���ܵ���Ļ�����ǵ���ʣ�
��ͭ˿�������ɵ��ӣ��ܵ��磬�ǵ��ʣ��Ȳ��ǵ����Ҳ���Ƿǵ���ʣ�
���Ȼ������岻�����ɵ��ӻ��������ƶ������ӣ������磬��ˮ��Һ���ܵ���Ļ�����ǵ���ʣ�
��ϡ���Ậ�������ƶ������ӣ��ܹ����磬�ǻ����Ȳ��ǵ����Ҳ���Ƿǵ���ʣ�
��CO2���岻�����ɵ��ӻ��������ƶ������ӣ������磬�������ܵ���������ƶ������ӣ����ڷǵ���ʣ�
�ް�ˮ���������ƶ������ӣ��ܹ����磬�ǻ����Ȳ��ǵ����Ҳ���Ƿǵ���ʣ�
��̼�����Ʒ�ĩ�������ɵ��ӻ��������ƶ������ӣ������磬��ˮ��Һ�л�����״̬���ܵ���Ļ����
�����Ǿ��� �������ɵ��ӻ��������ƶ������ӣ������磬��ˮ��Һ�к�����״̬�²��ܵ���Ļ�������ڷǵ���ʣ�
�������Ȼ��ƺ��������ƶ������ӣ��ܵ��磬��ˮ��Һ�л�����״̬���ܵ���Ļ�����ǵ���ʣ�
���������ƹ��壬�������ɵ��ӻ��������ƶ������ӣ������磬��ˮ��Һ�л�����״̬���ܵ���Ļ�����ǵ���ʣ�
���ԣ�����״̬���ܵ�����Ǣڢܢޢᣬ���ڵ���ʵ��Ǣ٢ۢߢ�⣬���ڷǵ���ʵ��Ǣݢࣻ
��������Ϊǿ����ʣ���ˮ��Һ����ȫ�������������ӡ������ӡ���������ӣ����뷽��ʽ��NaHSO4=Na++H++SO42����
����������������Ӧ����̼���ơ�̼��ƺ�ˮ����Ӧ�����ӷ���ʽ��Ca2++2OH��+2HCO3��=CaCO3��+2H2O+CO32����
���Դ��ǣ��ڢܢޢ�٢ۢߢ�⣻�ݢࣻNaHSO4=Na++H++SO42���� Ca2++2OH��+2HCO3��=CaCO3��+2H2O+CO32������2���÷�Ӧ�У����������Ԫ�صĻ��ϼ���+5�۱�Ϊ0�ۣ��������������������HCl��ClԪ�ػ��ϼ��ɩ�1�����ߵ�0�۱���������Cl2Ϊ��������õ����ű�ʾΪ�� 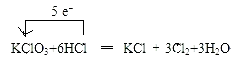 ��
��
���ݷ���ʽKClO3+6HCl��Ũ��=KCl+3Cl2��+3H2O��֪��������Ϊ����أ���ԭ��Ϊ�Ȼ��⣬6mol�Ȼ���μӷ�Ӧ������ԭ�����Ȼ�����5mol�����Ը÷�Ӧ����������ͻ�ԭ�����������Ϊ��5��1��
6.72L Cl2������������ʵ���Ϊ ![]() =0.3mol�����ݷ���ʽ��֪����3mol����ת��5mol���ӣ�������0.3mol����ת�Ƶ�����Ϊ��0.5NA��
=0.3mol�����ݷ���ʽ��֪����3mol����ת��5mol���ӣ�������0.3mol����ת�Ƶ�����Ϊ��0.5NA��
���Դ��ǣ� 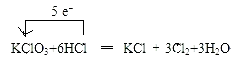 ��5��1�� 0.5NA����3��nBeO��Al2O3��6SiO2������Oԭ���غ�ã�n+3+6��2=18������n=3�����ݹ����θ�д�����������ʽΪ�����ý���������ϻ��ý����������������ˮ��ͬʱҪ��ѭԭ���غ㣬Ca2Mg5Si8O22��OH��2�ɱ�ʾΪ��2CaO5MgO8SiO2H2O��
��5��1�� 0.5NA����3��nBeO��Al2O3��6SiO2������Oԭ���غ�ã�n+3+6��2=18������n=3�����ݹ����θ�д�����������ʽΪ�����ý���������ϻ��ý����������������ˮ��ͬʱҪ��ѭԭ���غ㣬Ca2Mg5Si8O22��OH��2�ɱ�ʾΪ��2CaO5MgO8SiO2H2O��
���Դ��ǣ�3��2CaO5MgO8SiO2H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��HΪ��ѧ��ѧ�г������ʣ�����֮���ת����ϵ��ͼ��ʾ�����г�����AΪ��̬�ǽ������ʣ�CΪ��ɫ�д̼�����ζ�����壬D��GΪ��ɫ����ζ�����壬��C��D����ʹ����ʯ��ˮ����ǣ�E������Ϊ��ɫ����ζ��Һ�壻FΪ����ɫ��ĩ�� �ش��������⣺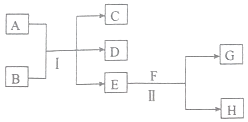
��1��F�Ļ�ѧʽΪ �� ��Ӧ����ÿ����1molG��ת�Ƶĵ�����ĿΪ ��
��2����Ӧ��Ļ�ѧ����ʽΪ ��
��3����ȥD�л��е�C���壬��ѡ��������ĸ���� a������������Һ b������̼��������ҺC������̼������Һ d�����Ը��������Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������A�ǵؿ��к������Ľ���������A���Բ�����ͼ�仯�����ֲ��뷴Ӧ�����ʺͷ�Ӧ����ʡ�ԣ��� 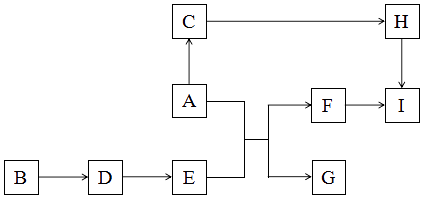
��֪��
����A��¶�ڿ�����ʱ��Ѹ������C��D��һ�ֵ���ɫ�Ļ����G�����壻H�������Σ�
��1����д���������ʵĻ�ѧʽ��D�� F�� I��
��2����д����������G�����ӷ���ʽ��H�백ˮ��Ӧ����I�����ӷ���ʽ��
��3�����ѽ���A��Ƭ�ڿ����м���ʱ���۲쵽�������ǽ���A�ۻ��������䣬ԭ���� ��
��4��ijͬѧ������ý���A��ŨHNO3�ڳ����·�Ӧֱ�ӵõ���H�ķ�������ͬѧ�ķ����Ƿ��ܴﵽʵ��Ŀ�ģ����ǻ��ԭ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����¹���Ԫ�����ڱ��ṹ��������ȷ���ǣ� ��
A. Ԫ�����ڱ���7�����壬8������
B. Ԫ�����ڱ���3�������ں�3��������
C. �ڢ�A��λ��Ԫ�����ڱ��ĵ�����(��������)
D. 0��λ��Ԫ�����ڱ��ĵ�18��(��������)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ���ǣ� ��
A.![]() +
+ ![]() ��
��  ����ȡ����Ӧ
����ȡ����Ӧ
B.���������Ը��������Һ���𱽺ͼ���
C.�л���C3H8��C6H14һ����ͬϵ��
D.��ϩ�����п�����8��ԭ�Ӵ���ͬһƽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͭ�Ļ�������ϡHNO3�У���Ӧ����ˣ��˳��Ĺ�������Ͷ��������������ų�������Һ��һ�����еĽ�������
A��Cu(NO3)2
B��Fe(NO3)3
C��Fe(NO3)2
D��Fe(NO3)2��Cu(NO3)2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2Al+2NaOH+2H2O = 2NaAlO2 +3H2�� ��Ƴ�ԭ��أ���������Ӧ����
A��̼�� B���� C���������� D�����ж�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Թ��ռ�60mL NO��NO2�Ļ�����壬������ʢ��ˮ��ˮ���У�������ͨ��O2 �� ���ֱ�ͨ��VmL��40mL��V��40��O2ʱ����ʣ��20mL���壨��Ϊ��״������ �ٵ�ͨ��40mL O2ʱʣ���������
�ڻ��������NO2�������mL
��V��ֵ��
�ܵ�ǡ��û������ʣ��ʱ��������Һ�����ʵ���Ũ��Ϊ��������Һ����ɢ��mol/L��������С��������λ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ױ������ϵ�һ�������6��ͬ���칹�壬��Щһ��������������Ķ�Ӧ���ױ����۵�ֱ��б����£�
һ������ױ� | 234�� | 206�� | 213.8�� | 204�� | 214.5�� | 205�� |
��Ӧ���ױ� | 13�� | ��54�� | ��27�� | ��54�� | ��27�� | ��54�� |
�ɱ������ݿ����ƶϣ��۵�Ϊ234���һ������ױ��Ľṹ��ʽΪ______________���۵�Ϊ��54��Ķ��ױ�������Ϊ__________________________________��
�𰸣� ![]() |����ױ�(1,3���ױ�)
|����ױ�(1,3���ױ�)
��1�� ��������
��������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com