
(14分)人工固氮是指将氮元素由游离态转化为化合态的过程。
I.最近一些科学家研究采用高质子导电性的SCY陶瓷(能传递H+)实验氮的固定一电解法合成氨,大大提高了氮气和氢气的转化率。
总反应式为:N2+3H2  2NH3
2NH3
则在电解法合成氨的过程中,应将H2不断地通入_________极(填“阴”或“阳”) ;
向另一电极通入N2,该电极的反应式为__________________________。
II.据报道,在一定条件下,N2在掺有少量氧化铁的二氧化钛催化剂表面能与水发生反应,主要产物为NH3相应的反应方程式为:2N2(g)+6 H2O (g)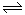 4NH3(g)+3O2(g) △H=Q ①
4NH3(g)+3O2(g) △H=Q ①
(1)上述反应的平衡常数表达式为_______________。
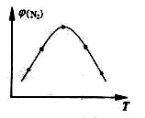
(2)取五份等体积N2和H2O的混合气体(物质的量之比均为1:3), 分别加 入体积相同的恒容密闭容器中,在温度不相同的情况下发生反应,反应相同时间后,测得氮气的体积分数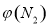 与反应温度T的关系曲线如下图所示,则上述反应的Q________0(填“>”、“<”或“=”)。
与反应温度T的关系曲线如下图所示,则上述反应的Q________0(填“>”、“<”或“=”)。
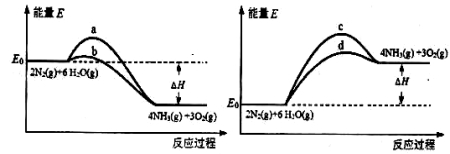
(3)若上述反应在有催化剂的情况下发生,则下图所示的a、b、c、d四条曲线中,能表示反应体系能量变化的是_______(填字母代号),图中△H绝对值为1530kJ·mol-1。
III.目前工业合成氨的原理是: N2(g)+3H2(g)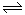 2NH3(g) △H=-93.0kJ/mol ②
2NH3(g) △H=-93.0kJ/mol ②
回答下列问题:
(1)结合II中的数据,则2H2(g)+ O2(g)=2 H2O (g)的△H=___________。
(2)在一定温度下,将1molN2和3mol H2混合置于体积不变的密闭容器中发生反应,达到平衡状态时,测得气体总物质的量为2.8mol。
①达平衡时,H2的转化率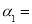 ______________。
______________。
②在相同条件下,若起始时只将NH3置于该容器中,达到平衡状态时NH3的转化率
为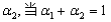 时,则起始时NH3的物质的量
时,则起始时NH3的物质的量 _________mol。
_________mol。
(14分)Ⅰ. 阳(2分) N2+6H++6e-===2NH3 (2分)
Ⅱ.(1)K=c(NH3)4·c(O2)3/c(N2)2·c(H2O)6(2分)
(2)>(1分) (3)d(1分)
Ⅲ. (1)-572.0 kJ·mol-1(2分,单位不写不给分)
(2)①60%(2分) ②2(2分)
【解析】
试题分析:I. 在电解法合成氨的过程中,氢气发生氧化反应,所以通入电解池的阳极,另一极通入氮气,则氮气发生还原反应,与阳极产生的氢离子结合 氨气,电极反应式为N2+6H++6e-===2NH3;
II.(1)根据平衡常数的表达式可知该反应的平衡常数K= c(NH3)4·c(O2)3/c(N2)2·c(H2O)6;
(2)图像的最高点表示反应达到平衡时氮气得体积分数,随温度升高,氮气得体积分数减小,说明升高温度平衡正向移动,所以正向是吸热反应,所以Q>0;
(3)2N2(g)+6 H2O (g)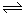 4NH3(g)+3O2(g) △H=Q是吸热反应,则反应物的总能量低于生成物的总能量,且使用催化剂,可以降低反应的活化能,而反应热不变,所以应选择d曲线;
4NH3(g)+3O2(g) △H=Q是吸热反应,则反应物的总能量低于生成物的总能量,且使用催化剂,可以降低反应的活化能,而反应热不变,所以应选择d曲线;
III.(1)由II知Q=+1530kJ/mol,根据盖斯定律得所求方程式2H2(g)+ O2(g)=2 H2O (g)的△H=(②×2-①)/3=[(-93.0)×2-1530]kJ/mol/3=-572.0kJ/mol;
(2)①设反应达平衡时消耗氮气得物质的量是xmol,则
N2(g)+3H2(g)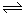 2NH3(g)
2NH3(g)
开始时(mol) 1 3
转化的(mol) x 3x 2x
平衡时(mol) 1-x 3-3x 2x
根据题意有1-x+3-3x+2x=2.8,所以x=0.6mol,则氢气的转化率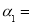 3x/3×100%=60%;
3x/3×100%=60%;
②当α1+α2=1时说明只将NH3置于该容器中,达到平衡状态与原平衡是等效平衡,则将氮气、氢气全部转化为氨气的物质的量即可达到等效平衡,所以1mol氮气、3mol氢气完全转化为氨气的物质的量是2mol.
考点:考查电化学原理的应用,化学平衡理论的应用,平衡常数的表示,反应热效应的判断,盖斯定律的应用,等效平衡的判断,转化率的计算


 名题金卷系列答案
名题金卷系列答案科目:高中化学 来源:2015届河南省偃师市高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列反应的离子方程式正确的是
A.铜片加入三氯化铁溶液中:Cu+2Fe3+=2Fe2++Cu2+
B.盐酸中加入碳酸钙:CO32-+2H+=H2O+CO2↑
C.AlCl3溶液中加入足量的氨水:Al3++3OH-=Al(OH)3↓
D.NaHCO3溶液中加入盐酸:CO32-+2H+=H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源:2015届河北省唐山市高三年级摸底考试理综化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A.用CH3COOH溶解CaCO3: CaCO3+2H+=Ca2++H2O+C02↑
B.Fe2(SO4)3和Ba(OH) 2溶液混合:Fe3++SO42-+Ba2++3OH- Fe(OH)3↓+ BaSO4↓
C.硫酸工业尾气中的SO2用过量的氨水吸收:2NH3·H2O+ SO2 =2NH4++ SO32-+H2O
D.Cu溶于浓HNO3:Cu+ 4H++ 2NO3一=Cu2++ 2NO↑+ 4H2O
查看答案和解析>>
科目:高中化学 来源:2015届河北省“五个一名校联盟”高三教学质量监测(一)化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值。下列叙述正确的是
A.0.1molCl2常温下与过量NaOH溶液反应转移电子总数为 0.1NA
B.25℃时, pH=13的1.0LBa(OH)2溶液中含有的OH-数目为0.2NA
C.0.25mol Na2O2中含有的阴离子数为0.5 NA
D.1L0.1mol·L-1的硫化钠溶液中硫离子数目为0.1NA
查看答案和解析>>
科目:高中化学 来源:2015届河北省“五个一名校联盟”高三教学质量监测(一)化学试卷(解析版) 题型:选择题
下列金属防腐的措施中,使用外加电流的阴极保护法的是
A.水中的钢闸门连接电源的负极B.金属护拦表面涂漆
C.枪炮表面涂上一层油D.地下钢管连接镁块
查看答案和解析>>
科目:高中化学 来源:2015届河北正定中学上学期高三第一次考试化学试卷(解析版) 题型:选择题
①pH=2的CH3COOH溶液;②pH=2的HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液。相同条件下,有关上述溶液的比较中,不正确的是( )
A.水电离的c(H+):①=②=③=④
B.若将②、③溶液混合后,pH=7,则消耗溶液的体积:②>③
C.等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量:②最大
D.向溶液中加入100mL水后,溶液的pH:③>④>②>①
查看答案和解析>>
科目:高中化学 来源:2015届河北正定中学上学期高三第一次考试化学试卷(解析版) 题型:选择题
镁及其化合物一般无毒(或低毒)、无污染,且镁原电池放电时电压高而平稳,使镁原电池越来越成为人们研制绿色原电池的关注焦点。其中一种镁原电池的反应为:
x Mg+Mo3S4  Mgx Mo3S4 。下列说法错误的是( )
Mgx Mo3S4 。下列说法错误的是( )
A.放电时Mg2+向正极迁移
B.充电时阳极反应为:Mo3S42x-—2xe? =Mo3S4
C.充电时Mo3S4发生氧化反应
D.放电时负极反应为:xMg ? 2xe? = xMg2+
查看答案和解析>>
科目:高中化学 来源:2015届江西省高三暑期化学试卷(解析版) 题型:填空题
(10分) 元素周期表中第ⅦA族元素的单质及其化合物的用途广泛。
(1)与氯元素同族的短周期元素的原子结构示意图为________。
(2)能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是________(填序号)。
a.Cl2、Br2、I2的熔点 b.Cl2、Br2、I2的氧化性
c.HCl、HBr、HI的热稳定性 d.HCl、HBr、HI的酸性
(3)工业上,通过如下转化可制得KClO3晶体:

①完成Ⅰ中反应的总化学方程式:
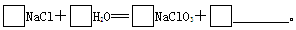
②Ⅱ中转化的基本反应类型是________________,该反应过程能析出KClO3晶体而无其他晶体析出的原因是____________________________________。
(4)一定条件下,在水溶液中1 mol Cl-、ClO(x=1,2,3,4)的能量(kJ)相对大小如右图所示。
①D是________(填离子符号)。
②B→A+C反应的热化学方程式为________________(用离子符号表示)。

查看答案和解析>>
科目:高中化学 来源:2015届江西省第一学期高三第一次月考化学(A卷)试卷(解析版) 题型:填空题
以有机物A为原料合成重要精细化工中间体TMBA( )和抗癫痫药物H(
)和抗癫痫药物H( )的路线如下(部分反应略去条件和试剂):
)的路线如下(部分反应略去条件和试剂):

已知:I. RONa + R’X → ROR’+ NaX;
II. RCHO + R’CH2CHO 
 + H2O(R、R’表示烃基或氢)
+ H2O(R、R’表示烃基或氢)
(1)A的名称是 ;C能发生银镜反应,则C分子中含氧官能团的名称是 。
(2)①和②的反应类型分别是 、 。
(3)E的结构简式是 ,
(4)D的同分异构体有多种,其中属于芳香族酯类化合物的共有 种。
(5)F与新制Cu(OH)2悬浊液发生反应的化学方程式是 。
(6)已知酰胺键( )有类似酯基水解的性质,写出抗癫痫病药物H与足量NaOH溶液发生反应的化学方程式 。
)有类似酯基水解的性质,写出抗癫痫病药物H与足量NaOH溶液发生反应的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com