
【题目】碘是人体不可缺少的元素,为了防止碘缺乏,现在市场上流行一种加碘盐,就是在精盐中添加一定量的KIO3进去.某研究小组为了检测某加碘盐中是否含有碘,查阅了有关的资料,发现其检测原理是:在溶液中 KIO3+5KI+3H2SO4=3I2+3H2O+3K2SO4
(1)用双线桥表示该反应中电子转移的方向和数目:该反应中氧化产物与还原产物的质量比是 , 0.1mol KIO3参加反应时转移电子mol
(2)实验结束后分离I2和K2SO4溶液所用的试剂是
A.Na2SO4溶液B.酒精 C. CCl4 D.食盐水
所用的分离方法是 , 所用仪器是 , 你怎么判断该食盐中是否含碘 .
(3)上面实验中用到一定物质的量浓度的稀硫酸,若配制1mol/L的稀硫酸溶液480mL,需用18mol/L浓H2SO4mL,配制中需要用到的主要玻璃仪器是(填序号) .
A.100mL量筒 B.托盘天平 C.玻璃棒D.100mL容量瓶 E.50mL 量筒 F.胶头滴管 G.烧杯 H.500mL容量瓶
(4)下面操作造成所配稀硫酸溶液浓度偏高的是
A.溶解后溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.用量筒量取浓硫酸后洗涤量筒并把洗涤液转移到容量瓶
E.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线.
【答案】
(1)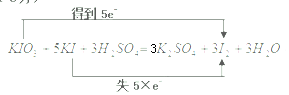 ,5:1,0.5
,5:1,0.5
(2)C,萃取分液,分液漏斗,静置分层后下层溶液为紫红色则说明有碘
(3)27.8,CEFGH
(4)A,C,D
【解析】解:(1)反应KIO3+5KI+3H2SO4=3I2+3H2O+3K2SO4的双线桥为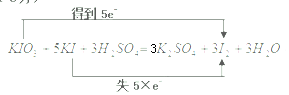 ,在此反应中,氧化产物与还原产物均为I2,且物质的量之比为5:1,故质量之比为5:1;反应中当有1molKIO3反应时,转移5mol电子,故当0.1mol KIO3参加反应时转移电子0.5mol,
,在此反应中,氧化产物与还原产物均为I2,且物质的量之比为5:1,故质量之比为5:1;反应中当有1molKIO3反应时,转移5mol电子,故当0.1mol KIO3参加反应时转移电子0.5mol,
故答案为: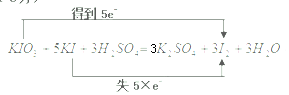 ;5:1;0.5;
;5:1;0.5;
(2)I2在有机溶剂中的溶解度大于在水中的溶解度,故将I2从K2SO4溶液中分离,应采取萃取分液的方法来分离,使用的主要仪器是分液漏斗,选用的萃取剂的应同时满足以下要求:碘单质在萃取剂中的溶解度大于在水中的溶解度;萃取剂与水互不相溶;溶质、萃取剂和水三者间互不反应,故应选四氯化碳,萃取后,由于四氯化碳的密度比水大,故分液后碘的四氯化碳溶液在下层,呈紫红色,
故答案为:C;萃取分液;分液漏斗;静置分层后下层溶液为紫红色则说明有碘;
(3)设需要的浓硫酸的体积为VmL,根据溶液的稀释定律可知:1mol/L×500mL=18mol/L×VmL,解得:V=27.8mL;
配制一定物质的量浓度的溶液的步骤是:计算、量取、稀释、移液、洗涤、定容、摇匀可知选用的仪器是50mL量筒、烧杯、玻璃棒、500mL容量瓶和胶头滴管,故选CEFGH,
故答案为:27.8;CEFGH;
(4)A.溶解后溶液没有冷却到室温就转移,则冷却后溶液体积偏小,则浓度偏高,A符合题意;
B.转移时没有洗涤烧杯、玻璃棒,会造成溶质的损失,则浓度偏低,B不符合题意;;
C.向容量瓶加水定容时眼睛俯视液面,则溶液体积偏小,则浓度偏高,C符合题意;;
D.用量筒量取浓硫酸后洗涤量筒,但洗涤液不能转移到容量瓶中,否则溶质偏多,则浓度偏高,D符合题意;
E.摇匀后发现液面低于刻度线是正常的,又加蒸馏水至刻度线则会造成浓度偏低,E不符合题意;
故答案为:ACD.
(1)反应KIO3+5KI+3H2SO4=3I2+3H2O+3K2SO4反应中,5KI~5/2I2,KIO3~1/2I2所以氧化产物与还原产物均为I2,且物质的量之比为5:1;反应中当有1molKIO3反应时,转移5mol电子,故当0.1mol KIO3参加反应时转移电子0.5mol;(2)将I2从K2SO4溶液中分离,采取萃取分液的方法来分离,使用的主要仪器是分液漏斗,用四氯化碳,作萃取剂在下层,呈紫红色;(3)设需要的浓硫酸的体积为VmL,根据溶液的稀释定律可知:1mol/L×500mL=18mol/L×VmL,解得:V=27.8mL;配制一定物质的量浓度的溶液的步骤是:计算、量取、稀释、移液、洗涤、定容、摇匀可知选用的仪器是50mL量筒、烧杯、玻璃棒、500mL容量瓶和胶头滴管;(4)误差分析注意操作引起的溶质、溶剂与仪器的变化。


科目:高中化学 来源: 题型:
【题目】将物质的量均为3.00mol物质A、B混合于5L容器中,发生如下反应:3A+B2C,在反应过程中C的物质的量分数随温度变化如图所示: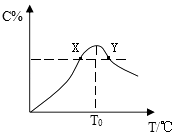
(1)T0对应的反应速率v(正)v(逆)(用“=”、“>”或“<”表示,下同);
(2)此反应的正反应为热;(填“放”或“吸”)
(3)X、Y两点A物质正反应速率的大小关系是YX;
(4)温度T<T0时,C%逐渐增大的原因是:;
(5)若Y点的C的物质的量分数为25%,则参加反应的A物质的量为mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,表中序号分别代表某一元素。请回答下列问题.
周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ③ | ④ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)可作半导体材料的元素是 ______(填元素符号);
(2)气态氢化物与其最高价氧化物的水化物可直接化合生成一种盐的元素是 ______(填名称);
(3)第三周期中离子半径最小的是___________(填离子符号);
(4)① ~ ⑨的最高价氧化物的水化物中:酸性最强的是 __________(填化学式);碱性最强的是________(填化学式),它与⑥的最高价氧化物的水化物反应的离子方程式为__________。
(5)⑧、⑨可形成A2B2型的共价化合物,分子中二者均满足8电子稳定结构,则其电子式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,不属于氧化还原反应的是( )
A.H2+F2═2HF
B.3CO+Fe2O3 ![]() 2Fe+3CO2
2Fe+3CO2
C.NaOH+HCl═NaCl+H2O
D.4HNO3 ![]() 2H2O+4NO2↑+O2↑
2H2O+4NO2↑+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常以烃的含氧衍生物X为主要原料生产可降解塑料PCL{![]() }及阻燃剂四溴双酚A。合成线路如下:
}及阻燃剂四溴双酚A。合成线路如下:

已知:① X的蒸汽密度是相同条件下H2的47倍,遇FeCl3溶液显紫色;C为![]()
②
③![]()
(1)X的分子式为_______________;B的名称是_________________。
(2)B→C还需要的反应试剂及条件是_______________。C→D的反应类型是________。
(3)写出X→Y的化学方程式:_________________________________________。
(4)0.5mol四溴双酚A在一定条件下与足量的NaOH溶液反应,最多消耗_____molNaOH。
(5)符合以下条件的D的同分异构体有_______种(不考虑空间异构)。
①含有两个甲基和两种官能团 ②能使溴的CCl4溶液褪色 ③能发生银镜反应
(6)已知由烯烃直接制备不饱和酯的新方法为: ![]() ,利用乙烯为有机原料(无机物和反应条件自选)合成聚合物涂料
,利用乙烯为有机原料(无机物和反应条件自选)合成聚合物涂料![]() ,,写出合成该涂料的反应流程图:______________________________________________。
,,写出合成该涂料的反应流程图:______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列属于微量元素的一组是( )
A. C、H、N、P、Mn B. Cl、Fe、S、N、Mg
C. B、Cu、Zn、Mn、Mo D. N、P、K、Cu、Fe、I
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去粗盐中的Ca2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列操作:①过滤;②加适量的盐酸;③加过量的Na2CO3溶液;④加过量BaCl2溶液,正确的操作顺序是( )
A.①③④②B.③①④②C.①②③④D.④③①②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z四种短周期元素的原子序数依次增大,W的某种原子无中子,X、Y可形成原子个数比为1∶1的具有漂白性的物质,工业上常用电解饱和YZ溶液来获得Z的单质及其他产品。下列说法正确的是
A. W和X、Y、Z均能形成18电子的分子
B. 上述四种元素的原子半径大小顺序为r(Z)>r(Y)>r(X)>r(W)
C. X、Y之间形成的化合物可能同时含有离子键和非极性共价健
D. W、X、Z三种元素形成的化合物一定是弱酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应A(g)+3B(g)![]() 2C(g)+2D(g) 在4种不同情况下反应速率分别如下,其中反应速率v最大的是
2C(g)+2D(g) 在4种不同情况下反应速率分别如下,其中反应速率v最大的是
A. v(A)=0.15mol/(L·min) B. v (B)=0.6 mol/(L·min)
C. v (C)=0.3 mol/(L·min) D. v (D)=0.1 mol/(L·min)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com