
����Ŀ���±���Ԫ�����ڱ���һ���֣�������ŷֱ����ijһԪ�ء���ش��������⣮
���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
2 | �� | �� | �� | �� | ||||
3 | �� | �� | �� | �� | �� | �� |
��1�������뵼����ϵ�Ԫ���� ______����Ԫ�ط��ţ���
��2����̬�⻯����������������ˮ�����ֱ�ӻ�������һ���ε�Ԫ���� ______�������ƣ���
��3���������������Ӱ뾶��С����___________�������ӷ��ţ���
��4���� ~ �������������ˮ�����У�������ǿ���� __________���ѧʽ����������ǿ����________���ѧʽ�������������������ˮ���ﷴӦ�����ӷ���ʽΪ__________��
��5���ࡢ����γ�A2B2�͵Ĺ��ۻ���������ж��߾�����8�����ȶ��ṹ���������ʽΪ_________________��
���𰸡� Si �� Al3+ ![]() NaOH
NaOH ![]()
![]()
����������������Ϣ��֪���٢ڢۢܢݢޢߢ���ֱ������Ԫ����C��N��O��F��Na��Al��Si��S��Cl��Ar��
��������Ϣ��֪���٢ڢۢܢݢޢߢ���ֱ������Ԫ����C��N��O��F��Na��Al��Si��S��Cl��Ar��
��1�������뵼����ϵ�Ԫ����Si��
��2���ɰ������Ժ����ữ����������泥���������ֻ����һ������֪����̬�⻯����������������ˮ�����ֱ�ӻ�������һ���ε�Ԫ���ǵ���
��3�����������У�����������2�����Ӳ㣬�ǽ�����������3�����Ӳ㣬�ʽ������ӵİ뾶��С������Ӳ�ṹ��ͬ�����ӵİ뾶��ԭ�������������С�����������Ӱ뾶��С����Al3+��
��4���� ~ �������������ˮ�����У�������ǿ����![]() ��������ǿ����NaOH�����������������ˮ����
��������ǿ����NaOH�����������������ˮ����![]() ��Ӧ�����ӷ���ʽΪ
��Ӧ�����ӷ���ʽΪ![]() ��
��
��5����������γ�A2B2�͵Ĺ��ۻ���������ж��߾�����8�����ȶ��ṹ���������ʽΪS2Cl2������ʽΪ![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ú��ʯ���п�������������ԭ��A��B��A��һ�ֹ�ʵ����������IJ�����������һ�����ҵ�ʯ�ͻ�����չˮƽ��B��һ�ֱ�ˮ�����״Һ�壬B����̼������Ԫ����ɣ�̼Ԫ������Ԫ�ص�������Ϊ12:1��B����Է�������Ϊ78���ش��������⣺
(1)A�ĵ���ʽ_______��B�Ľṹ��ʽ_____________________��
(2)��A���ڵ�ͬϵ��Cʹ������Ȼ�̼��Һ��ɫ�Ļ�ѧ��Ӧ����ʽ��___________________��
(3)�ڵ�ˮ�м���B���ú������________________��
(4)B��Ũ�����Ũ������50��60�淴Ӧ�Ļ�ѧ��Ӧ����ʽ��_____________________________����Ӧ���ͣ�________��
(5)��������A��B��ȫȼ��ʱ����O2�����ʵ���________(��A>B��A<B��A��B��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£�A��g��+3B��g�� ![]() 2C��g����ƽ��ı�־�ǣ�������
2C��g����ƽ��ı�־�ǣ�������
A.��λʱ���ڼ���xmolA��ͬʱ����3xmolB
B.��Ӧ���ٽ���
C.��n��A����n��B����n��C��=1��3��2ʱ
D.�����ϵ��ƽ����Է����������ٸı�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���Ũ�Ⱦ�Ϊ0.1 mol��L��1�������Ϊ100 mL������һԪ��HX��HY����Һ�У��ֱ����NaOH���壬lg![]() �����NaOH�����ʵ����ı仯��ͼ��ʾ(���Լ���NaOH���嵼����Һ�¶�������ı仯)������������ȷ����
�����NaOH�����ʵ����ı仯��ͼ��ʾ(���Լ���NaOH���嵼����Һ�¶�������ı仯)������������ȷ����

A. a����ˮ�������c(H��)��10��12 mol��L��1
B. b��ʱ���ǡ����ȫ�к�
C. c����Һ�У�c(Y��)>c(HY)
D. HX��HY������������HX>HY
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������ڰ��������������ȷ����
A. �������ǵ����ʵ���ɵ�λ,���ɰ������Ȼ���ɵ�
B. ÿ����������Ӷ�����һ��������һ���Ȼ�
C. һ��������İ�������һ����������Ȼ���ˮ�����γɶ���
D. ��������������ٺ���һ��������һ���Ȼ����Ҷ���һ��������һ���Ȼ�������ͬһ��̼ԭ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ԫ���в��������������Ĵ���Ԫ�ص��� �� ��
A. K B. P C. B D. Ca
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ҫ�ĵ��ʣ��ϳ�ԭ��Ϊ��N2��g��+3H2��g�� ![]() 2NH3��g����H=��92.4kJ/mol���ش��������⣺
2NH3��g����H=��92.4kJ/mol���ش��������⣺
��1��д��ƽ�ⳣ��K�ı���ʽ �� ��������¶ȣ��÷�ӦKֵE����ѧ��Ӧ���� �� N2��ת���������������С�����䡱����
��2����500�桢20MPaʱ����N2��H2����һ���ݻ�Ϊ2L���ܱ������з�����Ӧ����Ӧ�����и������ʵ����仯��ͼ��ʾ���ش��������⣺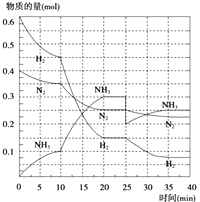
��10min����NH3��ʾ��ƽ����Ӧ���ʣ� ��
����10��20min�ڣ�NH3Ũ�ȱ仯��ԭ�������
A�����˴��� B����С�������
C�������¶� D������NH3���ʵ���
�۵�1��ƽ���ʱ��Ϊ�� �� ��2��ƽ���ʱ��Ϊ�� �� ��1��ƽ�⣺ƽ�ⳣ��K1= �������ݵı���ʽ������2��ƽ��ʱNH3�����������
���ڷ�Ӧ������25minʱ�����߷����仯��ԭ�� ��
��ڶ���ƽ��ʱ����ƽ���ƽ�ⳣ��K2K1 �� ������ڡ�����С�ڡ����ڡ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������岻��ȱ�ٵ�Ԫ�أ�Ϊ�˷�ֹ��ȱ���������г�������һ�ּӵ��Σ������ھ���������һ������KIO3��ȥ��ij�о�С��Ϊ�˼��ij�ӵ������Ƿ��е⣬�������йص����ϣ���������ԭ���ǣ�����Һ�� KIO3+5KI+3H2SO4=3I2+3H2O+3K2SO4
��1����˫���ű�ʾ�÷�Ӧ�е���ת�Ƶķ������Ŀ���÷�Ӧ�����������뻹ԭ������������� �� 0.1mol KIO3�μӷ�Ӧʱת�Ƶ���mol
��2��ʵ����������I2��K2SO4��Һ���õ��Լ���
A��Na2SO4��ҺB���ƾ��� C�� CCl4 D��ʳ��ˮ
���õķ��뷽���� �� ���������� �� ����ô�жϸ�ʳ�����Ƿ� ��
��3������ʵ�����õ�һ�����ʵ���Ũ�ȵ�ϡ���ᣬ������1mol/L��ϡ������Һ480mL������18mol/LŨH2SO4mL����������Ҫ�õ�����Ҫ���������ǣ�����ţ� ��
A��100mL��Ͳ ���� B��������ƽ �� C��������D��100mL����ƿ E��50mL ��Ͳ F����ͷ�ι� G���ձ� �� H��500mL����ƿ
��4����������������ϡ������ҺŨ��ƫ�ߵ����� ��
A.�ܽ����Һû����ȴ�����¾�ת��
B.ת��ʱû��ϴ���ձ���������
C.������ƿ��ˮ����ʱ�۾�����Һ��
D.����Ͳ��ȡŨ�����ϴ����Ͳ����ϴ��Һת�Ƶ�����ƿ
E.ҡ�Ⱥ���Һ����ڿ̶��ߣ��ּ�����ˮ���̶��ߣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ŀǰ���е�H5N1�������в��������к���A��U��G��C���ּ������˵���ò������Ŵ������ǣ� ��
A. DNA B. RNA C. DNA��RNA D. DNA��RNA
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com