
【题目】可逆反应A(g)+3B(g)![]() 2C(g)+2D(g) 在4种不同情况下反应速率分别如下,其中反应速率v最大的是
2C(g)+2D(g) 在4种不同情况下反应速率分别如下,其中反应速率v最大的是
A. v(A)=0.15mol/(L·min) B. v (B)=0.6 mol/(L·min)
C. v (C)=0.3 mol/(L·min) D. v (D)=0.1 mol/(L·min)
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案科目:高中化学 来源: 题型:
【题目】黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:S(s)+2KNO3(s)+3C(s)![]() K2S(s)+N2(g)+3CO2(g) ΔH=x kJ·mol1
K2S(s)+N2(g)+3CO2(g) ΔH=x kJ·mol1
已知:碳的燃烧热ΔH1=a kJ·mol1
S(s)+2K(s)![]() K2S(s) ΔH2=b kJ·mol1
K2S(s) ΔH2=b kJ·mol1
2K(s)+N2(g)+3O2(g)![]() 2KNO3(s) ΔH3=c kJ·mol1
2KNO3(s) ΔH3=c kJ·mol1
则x为
A.3a+bc B.c3ab C.a+bc D.cab
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关。下列说法错误的是
A. PM2.5是指粒径不大于2.5μm的可吸入悬浮颗粒物
B. 绿色化学要求从源头上消除或减少生产活动对环境的污染
C. 燃煤中加入CaO可以减少酸雨的形成及温室气体的排放
D. 天然气和液化石油气是我国目前推广使用的清洁燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有以下物质:① NaOH 溶液 ② 液氨 ③BaCO3 固体 ④ 熔融KHSO4⑤ Fe ( OH )3胶体 ⑥ 铜 ⑦ CO2 ⑧ CH3COOH。
(1)以上物质中属于混合物的是_____(填序号)。以上物质中属于非电解质的是_____(填序号)。
(2)对物质⑤进行通电,观察到阴阳两极的现象是_____。以上纯净物中能导电的是_____(填序号)。
(3)写出①和⑧的水溶液反应的离子方程式________。
(4)写出④的电离方程式_____。
(5)在足量④的水溶液中加入少量③,发生反应的离子方程式为_____。
(6)在含0.4mol ①的溶液中缓缓通入标准状况下6.72LCO2,气体被全部吸收,则反应后溶液的溶质有_____(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2Fe2O3(s) +3C(s)=3CO2(g) +4Fe(s) △H=+468.2 kJ/mol
C(s)+O2(g)=CO2(g) △H=-393.5 kJ/mol
根据以上热化学方程式判断,下列说法正确的是 ( )
A. C(s)的燃烧热为393.5kJ
B. 右图可表示由C生成CO2的反应过程和能量关系
C. O2(g)与Fe(s)反应放出824.35kJ热量时,转移电子数为4NA
D. Fe2O3(s)+ ![]() C(g)=
C(g)= ![]() CO2(g)+2Fe(s) △H <234.1 kJ/mol
CO2(g)+2Fe(s) △H <234.1 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向0.1mol/I.的NH4HCO3溶液中逐渐加入0.1mol/LNaOH溶液时,含氮、含碳粒子的分布情况如图所示(纵坐标是各粒子的分布系数,即物质的量分数)。根据图象,下列说法不正确的是( )
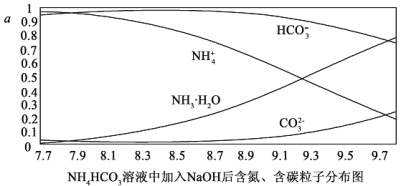
A.开始阶段,HCO3-反而略有增加,可能是因为NH4HCO3溶液中存在H2CO3发生的主要反应是H2CO3+OH-═HCO3-+H2O
B.当pH大于8.7以后,碳酸氢根离子和铵根离子同时与氢氧根离子反应
C.pH=9.5时,溶液中c(HCO3-)>c(HN3H2O)>c(NH4+)>c(CO32-)
D.滴加氢氧化钠溶液时,首先发生的反应为2NH4HCO3+2NaOH═(NH4)2CO3+Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某硫酸钠溶液50mL中含有1.15gNa+,取出10mL稀释至20mL后所得溶液中SO42-的物质的量浓度是______。
(2)12.4 g Na2X中含有0.4 mol Na+,则该物质的化学式为_______________。
(3)标准状况下四种气体:①6.72 L CH4②3.01×1023个HCl分子③13.6 g H2S④0.2 mol NH3,氢原子个数从大到小的排序是__________________________(写序号)。
(4)室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室,分别向A、B两室充入H2、O2的混合气体和1 mol空气,此时活塞的位置如图所示。

①A室混合气体所含分子总数约为___________________________。
②实验测得A室混合气体的质量为34 g,则该混合气体的密度是同温同压下氦气密度的___倍。
③若将A室H2、O2的混合气体点燃引爆,恢复原温度后,最终活塞停留的位置在____刻度,容器内气体压强与反应前气体压强之比为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com