
【题目】如图是元素周期表的一部分,表中所列字母分别代表一种元素
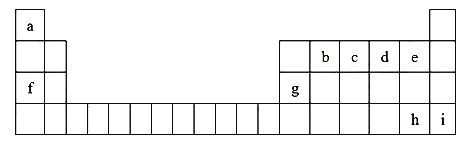
回答下列问题:
(1)h元素的名称是______,九种元素中金属性最强的是_______ (填元素符号)。
(2)f的最高价氧化物对应的水化物的化学式____(填化学式)。
(3)b、c、d、e的原子半径依次________(填增大或减小)。
(4)e、h元素的氢化物中,热稳定性大的是__(填氢化物的化学式)。
(5)化合物f2d2与化合物 a2d 反应的离子方程式__________。
(6)工业上冶炼g元素的单质的化学方程式__________。
【答案】 溴 Na NaOH 减小 HF 2Na2O2 + 2H2O = 4Na + +4OH- + O2 2Al2O3 = 4Al +3O2
【解析】根据元素在周期表中的位置,可以推知A为H,B为C,C为N,D为O,E为F,F为Na,G为Al,H为Br,I为Kr.
(1)h元素的名称是 溴;元素周期表中,从上到下,元素的金属性逐渐增强,从右到左,元素的金属性逐渐增强,所以金属性最强的金属在左下角,即为九种元素中金属性最强的是Na (填元素符号)。(2)f的最高价氧化物对应的水化物的化学式 NaOH。(3)同周期元素的原子,从左到右原子半径逐渐减小,b、c、d、e的原子半径依次减小。(4)元素周期表中,从上到下,元素的非金属性逐渐减弱,氢化物稳定性减弱,e、h元素的氢化物中,热稳定性大的是HF。(5)化合物f2d2与化合物 a2d 反应的离子方程式2Na2O2 + 2H2O = 4Na + +4OH- + O2 。(6)工业上冶炼g元素的单质的化学方程式2Al2O3 ![]() 4Al +3O2。
4Al +3O2。


科目:高中化学 来源: 题型:
【题目】下列反应中属于吸热反应的是
A. 镁跟盐酸反应 B. 乙醇的燃烧
C. 盐酸与氢氧化钠溶液反应 D. Ba(OH)2·8H2O晶体与NH4Cl晶体的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置图合理的是

A. 装置①可实现:Cu+2H2O![]() Cu(OH)2+H2↑
Cu(OH)2+H2↑
B. 装置②能构成锌铜原电池
C. 装置③可用于粗铜的电解精炼
D. 装置④可用于浓硫酸干燥氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2014新课标1】溴酸银(AgBrO3)溶解度随温度变化曲线如图所示,下列说法错误的是( ) 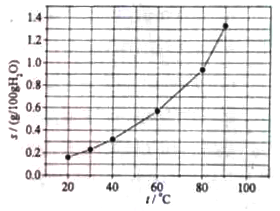
A.溴酸银的溶解时放热过程
B.温度升高时溴酸银溶解速度加快
C.60 ℃时溴酸银的Ksp约等于6×10-4
D.若硝酸钾中含有少量溴酸银,可用重结晶方法提纯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,属于同分异构体的是
A.O2和O3
B.CH2=CHCH2CH3和CH3CH=CHCH3
C. CH3CH2OH和CH3OCH3
D. CH3CH2CH3和CH3(CH2)2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. SO2和O3、PO43—和ClO4—互为等电子体
B. 甲烷分子失去一个H+,形成CH3—,其碳原子的杂化类型发生了改变
C. CH4、BCl3、SO2都是含有极性键的非极性分子
D. 所有元素的基态原子核外电子排布都遵循构造原理
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2016上海卷】无水MgBr2可用作催化剂。实验室采用镁屑与液溴为原料制备无水MgBr2,装置如图1,主要步骤如下:
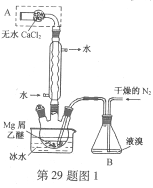
步骤1 三颈瓶中装入10 g镁屑和150 mL无水乙醚;装置B中加入15 mL液溴。
步骤2 缓慢通入干燥的氮气,直至溴完全导入三颈瓶中。
步骤3 反应完毕后恢复至常温,过滤,滤液转移至另一干燥的烧瓶中,冷却至0℃,析出晶体,再过滤得三乙醚合溴化镁粗品。
步骤4 室温下用苯溶解粗品,冷却至0℃,析出晶体,过滤,洗涤得三乙醚合溴化镁,加热至160℃分解得无水MgBr2产品。
已知:①Mg和Br2反应剧烈放热;MgBr2具有强吸水性。
②MgBr2+3C2H5OC2H5![]() MgBr2·3C2H5OC2H5
MgBr2·3C2H5OC2H5
请回答:
(1)仪器A的名称是____________。
实验中不能用干燥空气代替干燥N2,原因是___________。
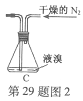
(2)如将装置B改为装置C(图2),可能会导致的后果是___________。
(3)步骤3中,第一次过滤除去的物质是___________。
(4)有关步骤4的说法,正确的是___________。
A.可用95%的乙醇代替苯溶解粗品B.洗涤晶体可选用0℃的苯
C.加热至160℃的主要目的是除去苯D.该步骤的目的是除去乙醚和可能残留的溴
(5)为测定产品的纯度,可用EDTA(简写为Y4-)标准溶液滴定,反应的离子方程式:Mg2++ Y4-====Mg Y2-
①滴定前润洗滴定管的操作方法是__________。
②测定时,先称取0.2500g无水MgBr2产品,溶解后,用0.0500 mol·L-1的EDTA标准溶液滴定至终点,消耗EDTA标准溶液26.50 mL,则测得无水MgBr2产品的纯度是________________________(以质量分数表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应 K2Cr2O7+14HCl(浓)=2CrCl3+2KCl+3Cl2↑+7H2O 中,氧化产物是( )
A. K2Cr2O7B. KClC. CrCl3D. Cl2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com