
����Ŀ����������һ�����ڴ�л���ṹ��ʽΪCH3��CH��OH����COOH���Իش�
��1����������к��еĹ�������_____ ��_____���������ƣ�
��2������ܷ����ķ�Ӧ��_____������ţ�
A��������Ӧ B��ȡ����Ӧ C���ӳɷ�Ӧ D����ȥ��Ӧ��
��300����ǰ��������ѧ�Ҳ����������������ûʳ�������ɫ��Ӧ�����ɴ˷���������īˮ��ûʳ����ĽṹʽΪ��

��1����ûʳ��������īˮ��Ҫ������_____���������ʣ�������ţ�
A���� B���� C��ȩ D������
��2��д��ûʳ����������������Һ���ȷ�Ӧ�Ļ�ѧ����ʽ��_______________��
���ڢ�CH2=CH2 ��![]() ��CH3CH2OH ��CH3COOH �ݾ���ϩ���������У�
��CH3CH2OH ��CH3COOH �ݾ���ϩ���������У�
��1�����ڸ߷��ӻ��������_____�����������ʵ���ţ���ͬ������
��2����ʹBr2��CCl4��Һ��ɫ����_____��
��3�����ܷ���ȡ����Ӧ���ܷ����ӳɷ�Ӧ����_____��
��4������Na2CO3��Һ��Ӧ����_____��
��5���ܷ���������Ӧ����_____��
���𰸡� �ǻ� �Ȼ� C B ![]() +4NaOH��
+4NaOH��![]() +4H2O �� �� �� �� �� ��
+4H2O �� �� �� �� �� ��
����������������һ��������������к��еĹ��������ʽ��
����������ûʳ��������к��еĹ��������ʽ��
�����������л���ķ�����ɡ����еĹ����š����ʵȷ����жϡ�
��⣺��һ����1����������Ľṹ��ʽ��֪��������к��еĹ��������ǻ����Ȼ���
��2������ܷ����ķ�Ӧ��_____������ţ�
A�������ǻ����Ȼ����ܷ���������Ӧ��A����B�������ǻ����Ȼ����ܷ���ȡ����Ӧ��B����C�������ǻ����Ȼ������ܷ����ӳɷ�Ӧ��C��ȷ��D�������ǻ����ܷ�����ȥ��Ӧ��D����ѡC��
��������1�������к��з��ǻ��������Ȼ���������ɫ��Ӧ������ûʳ��������īˮ��Ҫ�����˷����������ʣ���ѡB��
��2�����ǻ����Ȼ������������Ʒ�Ӧ����ûʳ����������������Һ���ȷ�Ӧ�Ļ�ѧ����ʽΪ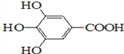 +4NaOH��
+4NaOH��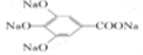 +4H2O��
+4H2O��
��������1����Է���������10000���ϵ�Ϊ�߷��ӻ���������ڸ߷��ӻ�������Ǿ���ϩ��
��2����ϩ����̼̼˫������ʹBr2��CCl4��Һ��ɫ��
��3�������ӵ�̼̼������̼̼������̼̼˫��֮�䣬��˱����ܷ���ȡ����Ӧ���ܷ����ӳɷ�Ӧ��
��4�����Ậ���Ȼ�������Na2CO3��Һ��Ӧ��
��5���Ҵ������ǻ������Ậ���Ȼ����ܷ���������Ӧ�����Ҵ������ᡣ


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȼú�����CO2��CO��SO2�ȴ�����Ⱦ�ȼú�������ط�Ӧ���Ȼ�ѧ����ʽ���£�
CaSO4(s)+CO(g) ![]() CaO(s) + SO2(g) + CO2(g) ��H1 =+281.4kJ/mol (��Ӧ��)
CaO(s) + SO2(g) + CO2(g) ��H1 =+281.4kJ/mol (��Ӧ��)
1/4CaSO4(s)+CO(g) ![]() 1/4CaS(s) + CO2(g) ��H2 = -43.6kJ/mol (��Ӧ��)
1/4CaS(s) + CO2(g) ��H2 = -43.6kJ/mol (��Ӧ��)
��1�����㷴ӦCaO(s) + 3CO(g ) + SO2(g) ![]() CaS(s) +3 CO2(g) ��H=____________��
CaS(s) +3 CO2(g) ��H=____________��
��2��һ���¶��£���ij�����ܱ������м���CaSO4(s)��1molCO����ֻ������ӦI��������˵���÷�Ӧ�Ѵﵽƽ��״̬����_____________������ţ�
a�������ڵ�ѹǿ�������仯 b������(CO)������(CO2)
c��������������ܶȲ������仯 d��n��CO��+n��CO2��=1mol
��3��һ���¶��£����Ϊ1L�����м���CaSO4(s)��1molCO����ֻ������ӦII�����CO2�����ʵ�����ʱ��仯����ͼ������A��ʾ��
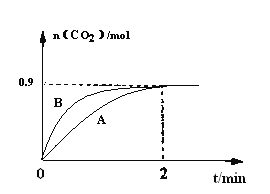
����0~2min�ڵ�ƽ����Ӧ����v��CO��=____________��
������B��ʾ����������A��ȸı�ķ�Ӧ��������Ϊ____________���һ�����ɣ���
����Ҫ��߷�Ӧ��ϵ��CO2������������ɲ�ȡ�Ĵ�ʩΪ__________________��
��4��һ���¶��£�������ܱ������м���CaSO4(s)��1molCO��������˵����ӦI�ͷ�ӦIIͬʱ��������________________������ţ���
a.��Ӧ��������ʹƷ����ɫ
b.��Ӧ�����У�CO�����������С
c.��Ӧ��ϵ��ƽ��ǰ��SO2��CO2���������Ũ��֮����ʱ�䷢���仯
d.��ϵѹǿ������
��5���̵����е�SO2��CO2�������������Ҳ��������������Һ���ա�
��֪��25��ʱ��̼���������ĵ���ƽ�ⳣ���ֱ�Ϊ��
̼�� K1��4.3��10-7 K2��5.6��10��11
������K1��1.5��10��2 K2��1.0��10��7
��������ʵ�У����ܱȽ�̼���������������ǿ������__________�����ţ���
a.25���£�����̼����ҺpH���ڱ�����������ҺpH
b��25���£���Ũ�ȵ�NaHCO3��ҺpH����NaHSO3��Һ
c����SO2����ͨ��NaHCO3��Һ���ݳ�����ͨ�����ʯ��ˮ������ʯ��ˮ�����
d����CO2����ͨ��NaHSO3��Һ���ݳ�����ͨ��Ʒ����Һ��Ʒ����Һ����ɫ
��25��ʱ������������Һ�����̵������õ�pH=6������Һ������Һ��c��SO32-����c��HSO3-��=___________��
��H 2SO3��Һ��NaHCO3��Һ��Ӧ����Ҫ���ӷ���ʽΪ____________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ü�ӵ绯ѧ���ɶԴ�����Ⱦ��NO���������������乤��ԭ����ͼ��ʾ������Ĥ����H+��H2Oͨ��������˵����ȷ����

A. �缫IΪ����,�缫��ӦʽΪ2H2O+2e-=2OH-+H2��
B. ���ʱH+�ɵ缫I��缫IIǨ��
C. �������еķ�ӦΪ2NO+2S2O42-+2H2O=N2+4HSO3-
D. ÿ����1molNO����ͬʱ�õ�32gO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������������ϢϢ��أ����������������
A. ��������ɹ㷺����ʳƷ������
B. С�մ���������ͷ۵���Ҫ�ɷ�֮һ
C. ȼ�ջ�ʯȼ�����������������һ����Ҫ����
D. �轺������ʳƷ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ������ܹ��ﵽʵ��Ŀ�ĵ���( )

A��ʵ���Ҳ���ͼ����ʾװ���ռ�SO2
B������ͼ����ʾװ�ñȽ�KMnO4��Cl2��S��������ǿ��
C��ʵ�������Ȼ�̼�г����������壬�������ı��������ú��Һ���ɳ�ȥ���Ȼ�̼�е���
D����ȡ0.40 g NaOH��ֱ������100 mL����ƿ�м�ˮ���̶��ߣ�������0.10 mol/L NaOH��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����þԭ�Ӻ�����____�ֲ�ͬ�˶�״̬�ĵ��ӣ�____�ֲ�ͬ����״̬�ĵ��ӣ�
��A��B��C��D��E����5��Ԫ�ء�����գ�
��1��AԪ�ػ�̬ԭ�ӵ��������3��δ�ɶԵ��ӣ��������2�����ӣ���Ԫ�ط���Ϊ_____
��2��BԪ�صĸ�һ�����ӵĵ��Ӳ�ṹ�����ͬ��B��ԭ�ӽṹʾ��ͼΪ_____
��3��CԪ���ǵ�����������δ�ɶԵ��ӵ�����Ԫ�أ����ĵ����Ų�ͼΪ_____
��4��DԪ�ػ�̬ԭ�ӵ�M��ȫ������N����һ�����ӣ�D��̬ԭ�ӵĵ����Ų�ʽΪ_____
��5��Eԭ�ӹ���3���۵��ӣ�����һ���۵���λ�ڵ����ܲ�d�����ָ����Ԫ�������ڱ�����������������������_____
�磮�÷��š�������������=���������и����ϵ��
��1����һ�����ܣ�N_____O��Mg_____Ca��
��2���縺�ԣ�O_____F��N_____P��
��3�������ߵͣ�ns_____np��4s_____3d��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������H����Ҫ���л������E��F��һ�������ºϳɣ������ַ�Ӧ������ʡ�ԣ�����ע���ͷ��ָ��
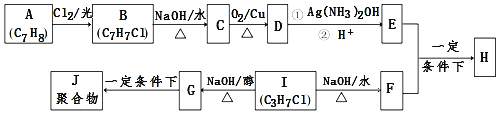
��֪������Ϣ��
i��A���ڷ�������H����������
ii��I�ĺ˴Ź�������Ϊ����壬�ҷ�������Ϊ6��1��
�ش��������⣺
��1��B�Ľṹ��ʽ_____��
��2��B��C��G��J�����ķ�Ӧ����_____��_____��
��3����E+F��H�Ļ�ѧ����ʽ_____��
��D��������Һ��Ӧ�Ļ�ѧ����ʽ_____��
��4��I��ͬϵ��K��I��Է���������28��K�ж���ͬ���칹�壮
��K��ͬ���칹�干_____�֣�
����K���ܷ�����ȥ��Ӧ����K�Ľṹ��ʽΪ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й�ϵͼ�У�A��һ�����Σ�D��Է���������C��Է���������16��E��ǿ�ᣬ��X������ǿ�ỹ��ǿ��ʱ��������ת����ϵ����X��ǿ��ʱ��A��B��C��D��E������ͬһ��Ԫ�أ���X��ǿ��ʱ��A��B��C��D��E��������һ��Ԫ�ء�����˵��һ������ȷ����(����)
![]()
A. D��H2O��Ӧ����E����������ԭ��Ӧ
B. ��X��ǿ��ʱ��E��HNO3����X��ǿ��ʱ��E��H2SO4
C. ��X��ǿ��ʱ��C�ڳ���������̬����
D. A���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���������Ũ�����ڳ����·�Ӧ�ܲ���������������ͼ��ʾ��ʵ��װ�����Ʊ��������������������������������ķ�Ӧ��ÿ�����߿��ʾһ����Ԫװ�ã������д������(����)
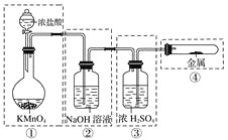
A. �ٺ͢ڴ� B. ֻ�Тڴ�
C. �ں͢۴� D. �ڡ��ۡ��ܴ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com