
����Ŀ��ijͬѧ���о�Ԫ�����ʵݱ����ʵ��ʱ���Լ������һ��ʵ�鷽��������¼���й�ʵ������(���±������еġ�ʵ�鷽�����롰ʵ������ǰ��һ���Ƕ�Ӧ��ϵ)��
ʵ�鲽�� | ʵ������ |
�ٽ�þ����ɰֽ��ĥ�����Թ��У���������ˮ������ˮ���ڣ�������Һ�еμӷ�̪��Һ | A.����ˮ���ϣ��۳�С���Ĵ��ζ���������˻˻��������֮��ʧ����Һ��ɺ�ɫ |
�������Ƶ�Na2S��Һ�еμ����Ƶ���ˮ | B.�������������Һ���dz��ɫ |
�۽�һС������Ʒ�����з�̪��Һ����ˮ�� | C.���ҷ�Ӧ��Ѹ�ٲ���������ɫ���� |
�ܽ�þ��Ͷ��ϡ������ | D.��Ӧ��ʮ�־��ң�������ɫ���� |
�ݽ�����Ͷ��ϡ������ | E.���ɰ�ɫ��״�������̶�������ʧ |
����AlCl3��Һ�еμ�NaOH��Һ������ | F.���ɵ���ɫ���� |
���������ͬѧ���������ʵ�鱨�档
(1)ʵ��Ŀ�ģ��о�__________________Ԫ�����ʵݱ���ɡ�
(2)ʵ����Ʒ���Լ��������ơ�þ����������ϡ���ᡢ������ˮ������Na2S��Һ��AlCl3��Һ��NaOH��Һ����̪��Һ�ȡ�
������______��______����ֽ���ԹܼС���ͷ�ιܡ����ӡ�С��������Ƭ��ɰֽ�����ȡ�
(3)ʵ�����ݣ�(��д��ʵ�鲽���Ӧ��ʵ������ı�ź͢٢ڵĻ�ѧ����ʽ����ʵ��Ľ���)
ʵ������ | �� | �� | �� | �� | �� | �� |
ʵ������(��A��F) | __ | __ | __ | __ | __ | __ |
��__________________________________________________��
��___________________________________________________��
��ʵ��Ľ��ۣ�__________________________________________________��
���𰸡� ͬ���ڡ������������𰸶��÷֣� �Թ� �ƾ��� B F A C D E Mg��2H2O![]() Mg(OH)2��H2�� Cl2��Na2S===S����2NaCl ����ԭ�������ĵ�����ͬ����Ԫ�ش����ҽ������������ǽ���������ǿ
Mg(OH)2��H2�� Cl2��Na2S===S����2NaCl ����ԭ�������ĵ�����ͬ����Ԫ�ش����ҽ������������ǽ���������ǿ
��������
��1������Ŀ��֪��ʵ��Ŀ��Ϊͬ����Ԫ�����ʵݱ���ɣ��ʴ�Ϊ��ͬ���ڣ���2���������ˮ���������ڣ�����Ҫ�ƾ��ƣ�������ˮ����ķ�Ӧ���Թ��н��У��ʴ�Ϊ���Թܡ��ƾ��ƣ���3����þ����ɰֽ��ĥ�����Թ��У���������ˮ������ˮ���ڣ�þ����ˮ��Ӧ���������������ݲ�������Ӧ����������þ����Һ�ʼ��ԣ�������Һ�еμӷ�̪��Һ����Һ�ʺ�ɫ��þ�������ã������������ᷢ���û���Ӧ����þ��Ͷ��ϡ�����У����ҷ�Ӧ��Ѹ�ٲ���������ɫ���壬������Ͷ��ϡ�����У���Ӧ��ʮ�־��ң�������ɫ���壻�����Ƶõ�Na2S��Һ���������Ƶ���ˮ��������Na2S����������ԭ��Ӧ����Ӧ�Ļ�ѧ����ʽΪNa2S+Cl2=2NaCl+S����һС������Ʒ�����з�̪��Һ����ˮ�У�����ˮ��Ӧ�����������ƺ���������ѧ����ʽ��2Na+2H2O=2NaOH+H2�����Դ˿ɵó��������ң�ͬ����Ԫ��ԭ�ӵ�ʧ���������ݼ����õ��������������ʴ�Ϊ��
ʵ������ | �� | �� | �� | �� | �� | �� |
ʵ������(��A��F) | B | F | A | C | D | E |
Na2S+Cl2=2NaCl+S����2Na+2H2O=2NaOH+H2����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������������������Ҫ�������������ĺ�����������NaClO2��NaClO��ClO2 ��Cl2
�ش�����������
��1��NaClO2�����Ļ�ѧ��������________________��
��2��������Ͷ��ˮ����һ��ʱ����백��ϵõ�һ�ֽ�����Ȱ�(NH2Cl)��NH2Cl �����Ի�����������Ҳ��һ��ǿɱ���������������ڳ�������ˮ��������������________________���û�ѧ����ʽ��ʾ����
��3�� ����Ч�Ⱥ��������������������������������������䶨����ÿ�˺��������������������൱�ڶ��ٿ�Cl2 �������������������ֺ���������������������ǿ����________________��
��4������ˮ����ClO2 �������ˮ����Ҫ��ClO2 ��Ũ����0.1~0.8 mg��L-1֮�䡣�õ��������ClO2 �����������ˮ��ClO2 Ũ�ȵ�ʵ�鲽��������
������.ȡһ�������ˮ�������������⻯������������������Һ���������������������Һ��
������.��Na2S2O3 ��Һ�ζ������������õ���Һ��
��֪��a. ����ʱ����ͬpH �����������������±���ʾ��
pH | 2 | 7 |
�������� | Cl- | ClO2- |
b. 2S2O32-+I2==S4O62-��2I-��
���������з�Ӧ����ʱ��Һ��___________��������ɫ��������ɫ����
����ˮ�������Ϊ1.0L���ڲ�����������10mL1.0��10-3mol��L-1Na2S2O3 ��Һ�����ˮ����c(ClO2)=___________mg��L-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ϴ��ʢ��ֲ���͵��Թ�����ѡ�õ��Լ���( )
A. ϡ���� B. ��ˮ C. �ȼ�Һ D. ϡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���У�����ȷ����
A. ��֬ˮ��IJ�����һ��������
B. ��������������ᷴӦ��Ҳ����NaOH��Ӧ
C. ���ࡢ��֬�͵����ʶ����ڸ߷��ӻ�����
D. ҽ������75%�ľƾ���������Ϊ����ʹ�����ʱ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й���ɫ��Ӧ����������ȷ����
A.ֻ�н����Ļ���������ʱ�Ż��в�ͬ����ɫ
B.ÿ��ʵ���˿��Ҫ��ˮϴ��
C.������ɫ�ܲ���ֻ������ɫ��˵����Ʒ�к�KԪ�ض�����NaԪ��
D.����Ʒ���ճʻ�ɫ���ж�һ����NaԪ�أ��������ų�����������Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ������ ��
A. ���ؽ���ѧ��ת��Ϊ����
B. ��ԭ��صĸ����͵��ص������϶��Ƿ���ʧ���ӵ�������Ӧ
C. �ö��Ե缫��ⱥ��NaCl��Һһ��ʱ����� ͨ���Ȼ������壬��ʹ���Һ�ָ���ԭ״̬
D. �ö��Ե缫���Na2SO4��Һ���������������������ʵ���֮��Ϊ1:2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һ�к�Cl��Ũ����С���ǣ� ��
A.100mL0.25mol/L��NaCl��ҺB.30mL0.1mol/L��KCl��Һ
C.20mL0.1mol/L��CaCl2��ҺD.10mL0.1mol/L��AlCl3��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������A��Ԫ���γɵĻ���������Ҫ�İ뵼�������Ӧ����㷺�����黯��(GaAs)���ش��������⣺
��1����̬Gaԭ�ӵĺ�������Ų�ʽΪ__________����̬Asԭ�Ӻ�����__________��δ�ɶԵ��ӡ�
��2����ʧȥ���ӵ�������(��λ��kJ��mol-1)����ֵ����Ϊ577��1985��2962��6192���ɴ˿���֪�ص���Ҫ���ϼ�Ϊ__________��+3����ĵ縺�Ա���__________(������������С��)��
��3���Ƚ������ص�±������۵�ͷе㣬������仯���ɼ�ԭ��__________________________��
�ص�±���� | GaCl3 | GaBr3 | GaI3 |
�۵�/�� | 77.75 | 122.3 | 211.5 |
�е�/�� | 201.2 | 279 | 346 |
GaF3���۵㳬��1000�������ܵ�ԭ����_______________________________________��
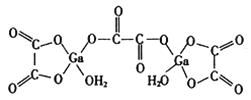
��4����ˮ�ϲ����صĽṹ��ͼ��ʾ��������ԭ�ӵ���λ��Ϊ__________���������̼ԭ�ӵ��ӻ���ʽΪ__________��
��5���黯���۵�Ϊ1238�������������ṹ��ͼ��ʾ����������Ϊa=565pm���þ��������Ϊ__________��������ܶ�Ϊ__________(��NAΪ�����ӵ���������ֵ���г���ʽ����)g��cm-3��
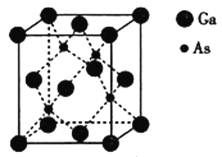
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ��ʾװ�ý�������ʵ�飬�ܵó���Ӧʵ����۵���
ѡ�� | �� | �� | �� | ʵ����� |
|
A | Ũ���� | MnO2 | ����-KI ��Һ | �����ԣ�Cl2>I2 | |
B | Ũ���� | ���� | ��ˮ | Ũ���������ˮ�ԡ������� | |
C | ϡ���� | Na2SO3 | Ba(NO3)2��Һ | SO2������Ա��ξ������ɰ�ɫ���� | |
D | Ũ���� | Na2CO3 | Na2SiO3��Һ | ���ԣ�����>̼��>���� |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com