
【题目】已知NaHSO3溶液显酸性,溶液中存在以下平衡:HSO3-+ H2O![]() H2SO3 + OH-① HSO3-
H2SO3 + OH-① HSO3-![]() H+ + SO32- ②,向0.1mol/L的NaHSO3溶液中分别加入以下物质,下列有关说法正确的是
H+ + SO32- ②,向0.1mol/L的NaHSO3溶液中分别加入以下物质,下列有关说法正确的是
A.加入少量金属Na,平衡①左移,平衡②右移,溶液中c(HSO3-)增大
B.加入少量Na2SO3固体,则c(H+) + c(Na+) = c(HSO3-) + c(OH-) +![]() c(SO32-)
c(SO32-)
C.加入少量NaOH溶液,![]() 、
、![]() 的值均增大
的值均增大
D.加入氨水至中性,则c(Na+) = c(SO32-)+c(HSO3- )+ c(H2SO3)
【答案】CD
【解析】
A. 加入少量金属Na,Na与HSO3-电离出的H+反应,促使平衡②右移,HSO3-离子浓度减小,又促使平衡①左移,平衡①左移,平衡②右移,溶液中c(HSO3-)浓度减小,A错误;
B. 加入少量Na2SO3固体溶解后溶液中存在电荷守恒,c(H+)+c(Na+)=2c(SO32-)+c(HSO3-)+c(OH-),B错误;
C. 加入氢氧化钠与氢离子反应,c(H+)减小,平衡右移,抑制水解,平衡左移,c(SO32-),c(OH-)浓度增大,c(HSO3-)减小,![]() 、
、![]() 的比值增大,C正确;
的比值增大,C正确;
D. 在NaHSO3溶液中钠离子与硫元素的所有存在形式物质的量相等,加入氨水至中性后该数量关系依然存在,所以c(Na+)=c(SO32-)+c(HSO3-)+c(H2SO3),D正确。
答案选CD。


 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:高中化学 来源: 题型:
【题目】下列有关苯的叙述中,错误的是( )
A.能使酸性KMnO4溶液褪色
B.无色、有特殊气味的液体,不溶于水,密度比水的小
C.在FeBr3催化作用下,苯与液溴反应生成溴苯和溴化氢
D.50~60℃时,在浓硫酸存在下,苯与浓硝酸反应生成硝基苯和水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳循环可以通过下列途径:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g) ![]() +49.0kJ,在容积为2 L的密闭容器中充入1 mol CO2和3 mol H2,在两种不同的实验条件下进行反应,测得CH3OH(g)的物质的量随时间变化情况如图所示:
+49.0kJ,在容积为2 L的密闭容器中充入1 mol CO2和3 mol H2,在两种不同的实验条件下进行反应,测得CH3OH(g)的物质的量随时间变化情况如图所示:
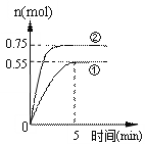
(1)前5 min内实验①的平均反应速率v(H2)=_____mol/(Lmin)。
(2)能说明上述反应达到平衡状态的是_________(填编号)。
a.混合气体的平均相对分子质量不随时间变化而变化
b.单位时间内每消耗3 mol H2,同时生成1 mol H2O
c.CO2的体积分数在混合气体中保持不变
d.v逆(CO2) =3v正(H2)
(3)与①相比,②仅改变一种反应条件,所改变的条件是____________,判断的理由_______________________________________________________。
(4)在一定温度下,把2.0 LCO2和6.0 LH2通入一个带活塞的体积可变的密闭容器中,活塞的一端与大气相通,反应达到平衡后,测得混合气体为7.0 L。若需控制平衡后混合气体为6.5 L,则可采取的措施是_____;欲使反应的K减小,可以采取的措施是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一般来说,对一种未知有机物结构的测定主要包括以下几个方面:
①确定相对分子质量;
②测定元素组成(种类和比例);
③研究该有机物的各种性质;
④确定结构。
(1)相对分子质量的确定一般利用质谱法,蒸气密度法等。某有机物![]() 的质谱图显示其相对分子质量最大是72。组成元素的测定常采用元素分析仪,也可采用燃烧法。称取
的质谱图显示其相对分子质量最大是72。组成元素的测定常采用元素分析仪,也可采用燃烧法。称取![]()
![]() ,在足量氧气中充分燃烧,生成物通过浓硫酸后,浓硫酸的质量增加
,在足量氧气中充分燃烧,生成物通过浓硫酸后,浓硫酸的质量增加![]() ,剩余气体通过碱石灰,碱石灰的质量增加
,剩余气体通过碱石灰,碱石灰的质量增加![]() ,则
,则![]() 的分子式为______。
的分子式为______。
(2)核磁共振谱常用氢谱或碳谱,它主要测定分子中具有不同特点的![]() 或
或![]() 的种类与比例。如对于有机物
的种类与比例。如对于有机物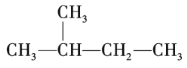 ,其
,其![]() 谱有四个峰,峰高比为
谱有四个峰,峰高比为![]() ;
;![]() 谱有四个峰,峰高比为
谱有四个峰,峰高比为![]() 。有机物
。有机物![]() 的
的![]() 谱有两个峰,峰高比为
谱有两个峰,峰高比为![]() ,氢谱有一个峰。试写出有机物
,氢谱有一个峰。试写出有机物![]() 的结构简式:______。
的结构简式:______。
(3)![]() 的一氯代物有______种,二氯代物有______种。
的一氯代物有______种,二氯代物有______种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】明代《天工开物》记载了“火法”冶炼锌的方法:“炉甘石十斤,装载入一泥罐内,…然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,…冷淀,毁罐取出,…,即倭铅也”,现代工业开发了用NH3—NH4Cl水溶液浸出氧化锌烟灰(主要成分为ZnO 、少量Pb、CuO和As2O3)制取高纯锌的工艺流程如图所示。
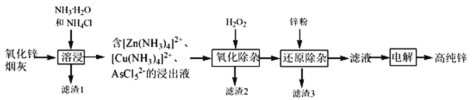
请回答下列问题:
(1)《天工开物》中炼锌的方法中“泥封”的目的是____________。
(2)滤渣1的主要成份分别是_______(填化学式),“过滤”用到的玻璃仪器是__________。
(3) “溶浸”时,氧化铜参与反应的相关离子方程式是________;“溶浸”时可以适当升高温度,但不宜过高,其原因是________________。
(4) “氧化除杂”的目的是将AsCl52-转化为As2O5胶体,再经吸附聚沉除去,溶液始终接近中性,该反应的离子方程式是_____________________。
(5) “电解”含 [Zn(NH3)4]2+的溶液,阴极放电的电极反应式是_________。阳极区产生一种无色无味的气体,将其通入滴有KSCN的FeCl2溶液中,无明显现象,该气体是_______(写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻、能量密度大等优良性能,得到广泛应用。回答下列问题:
(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为__、__(填标号)。
A.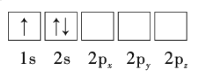
B.
C.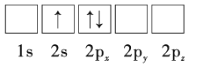
D.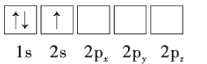
(2)Li+与H-具有相同的电子构型,r(Li+)小于r(H-),原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源问题是现代社会发展的三大基本问题之一。
(1)焦炭可用于制取水煤气。实验测得1.2 g 碳与水蒸气完全反应生成水煤气时,吸收了13.16 kJ热量。该反应的热化学方程式为_________________________;该反应在________条件下能自发进行(选“高温”、“低温”或“任意温度”)。
(2)甲醇(CH3OH)广泛用作燃料电池的燃料,工业上可由CO和H2来合成,化学方程式为CO(g)+2H2(g)![]() CH3OH(g)。如图是在不同温度下CO的转化率随时间变化的曲线。
CH3OH(g)。如图是在不同温度下CO的转化率随时间变化的曲线。
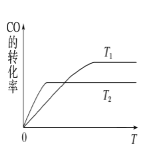
①T1________T2(填“>”、“<”或“=”)。T1和T2温度下的平衡常数大小关系是K1________(填“>”、“<”或“=”)K2。
②若容器容积不变,下列措施不能增加CO转化率的是________(填字母)。
a.降低温度 b.将CH3OH(g)从体系中分离
c.使用合适的催化剂 d.充入He,使体系总压强增大
③生成甲醇的化学反应速率(v)与时间(t)的关系如图所示。则图中t2时采取的措施可能是___________________;
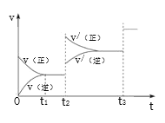
t3时采取的措施可能是 _________________。
④若在T1℃时,往一密闭容器通入等物质的量CO和H2测得容器内总压强1MPa,40min达平衡时测得容器内总压强为0.6MPa,计算生成甲醇的压强平衡常数KP=________(MPa)-2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)甲醇(CH3OH)燃料电池是以铂为电极,以KOH溶液为电解质溶液,在两极区分别加入CH3OH和O2即可产生电流。负极加入的物质是________;正极的电极反应为_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com