
【题目】
请根据所给装置回答下列问题:
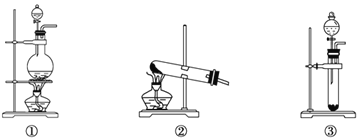
(1)A是制取CO2的装置,最好选用下列装置中的______________ (填序号)。
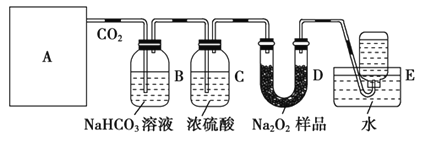
(2)B装置中发生的离子方程式是_______________________。C装置的作用是_______________________。
(3)D装置中发生反应的化学方程式是_________________。
(4)要想得到较纯净的氧气,可在装置D和E之间增加一盛有________(填写试剂名称)的________(填写装置名称)。
(5)如何检验集气瓶中收集到的气体______________________。
【答案】(1)③;
(2)HCO3-+H+=H2O+CO2↑,除去CO2中混有的水蒸气;
(3)2Na2O2+2CO2=2Na2CO3+O2;
(4)碱石灰干燥管或U形管(或NaOH溶液洗气瓶);
(5)将带火星木条伸入集气瓶,木条复燃。
【解析】试题分析:(1)制备CO2用碳酸钙和盐酸的反应,即选项的装置为③;(2)制取的CO2中混有HCl,装置B的作用是除去CO2中混有HCl,发生的反应是HCO3-+H+=CO2H↑+H2O,装置C的作用是除去CO2中的水蒸气;(3)装置D中发生2Na2O2+2CO2=2Na2CO3+O2;(4)装置D中出来的气体,混有未反应的CO2,可能影响实验,因此需要在D和E之间添加碱石灰干燥管或U形管(或NaOH溶液洗气瓶);(5)验证氧气,将带火星木条伸入集气瓶,木条复燃。


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案科目:高中化学 来源: 题型:
【题目】下列表述中,与盐类水解无关的是
A. 明矾和FeCl3可作净水剂 B. 盛放NaOH溶液的试剂瓶不能用玻璃塞
C. 草木灰与铵态氮肥不能混合施用 D. NH4Cl与ZnCl2溶液可作焊接中的除锈剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学一选修3:物质结构与性质】A、B、C、D、E五种元素的原子序数依次增大。A 是原子半径最小的元素;B的最外层电子数是次外层电子数的2倍; D的L能层有两对成对电子;E+的核外有三个能层,且都外于全满状态。试回答下列问题:
(1)基态E原子核外电子的排布式为___________________。
(2)B、C、D三种元素的电负性由大到小的顺序是____________(填元素符号)。A、C、D三种元素形成的常见离子化合物中阳离子的空间构型为_____________,阴离子的中心原子轨道采用______________杂化。
(3)E(CA3)![]() 离子的颜色是___________;含有化学键类型是_____________;离子中C原子杂化轨道类型是__________________。
离子的颜色是___________;含有化学键类型是_____________;离子中C原子杂化轨道类型是__________________。
(4)D、E能形成两种晶体,其晶胞分别如甲、乙两图。晶体乙中,E的配位数为_________;在一定条件下,甲和C2A4反应生成乙,同时生成在常温下分别为气体和液体的另外两种常见无污染物质。该化学反应方程式为______________________。

(5)若甲的密度为ρ g/cm3,NA表示阿伏加德罗常数,则甲晶胞的边长可表示为_________cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.0.012kg12C所含的碳原子数就是阿伏伽德罗常数
B.等质量的O2和O3中所含氧原子的物质的量相同
C.等物质的量的分子所含原子数目一定相等
D.标准状况下,1molH2的体积约为22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以CuSO4溶液为电解质溶液进行粗铜(合Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是
A. 电能全部转化为化学能
B. 反应溶液中Cu2+向阳极移动
C. 粗铜接电源正极,发生氧化反应
D. 利用阳极泥可回收Zn、Ag、Pt、Au等金属
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)以下反应:①木炭与水制备水煤气 ②氯酸钾分解 ③炸药爆炸 ④酸与碱的中和反应 ⑤生石灰与水作用制熟石灰 ⑥ Ba(OH)2·8H2O与NH4Cl,属于放热反应的是 (填序号),写出反应⑥的化学方程式__ 。
(二)为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应措施.化学反应的焓变通常用实验进行测定,也可进行理论推算。
(1)丙烯是石化工业的主要原料之一,由于市场对丙烯的需求量激增,丙烷脱氢制丙烯的技术日益受到重视。某研究机构需得到C3H8(g)===3C(石墨,s)+4H2(g)的ΔH,但直接测定实验难进行,可通过下图中各组物质能量总和及相互间转化中的能量变化计算得到:

①判断:ΔH________0(选填“>”、“<”或“=”)。
②ΔH=___________(用含ΔH1、ΔH2、ΔH3的代数式表示)。
(2)实验测得,5g甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇燃烧的热化学方程式:_________________。
(3)由气态基态原子形成1mol化学键释放的最低能量叫键能.从化学键的角度分析,化学反应的过程就是反应物的化学键的断裂和生成物的化学键的形成过程.在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量.已知反应N2(g)+3H2(g)![]() 2NH3(g) △H=a kJ·mol-1。试根据表中所列键能数据计算a的数值: (写出 + 或-)。[
2NH3(g) △H=a kJ·mol-1。试根据表中所列键能数据计算a的数值: (写出 + 或-)。[
化学键 | H-H | N-H | N≡N |
键能/kJ·mol-1 | 436 | 391 | 945 |
(4)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的反应热进行推算。
已知:C(石墨,s)+O2(g)=CO2(g) △H1=-393.5kJ·mol-1
2H2(g)+O2(g)=2H2O(l) △H2=-571.6kJ·mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H3=-2599kJ·mol-1
根据盖斯定律,计算298K时由C(石墨,s)和H2(g)生成C2H2(g)反应的反应的热化学方程式: _ _ _。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应与四个基本反应类型的关系如下图所示,则下列化学反应属于阴影部分的是( )

A.Cl2+2KBr=Br2+2KCl
B.2NaHCO3![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
C.4Fe(OH)2+O2+2H2O=4Fe(OH)3
D.2Na2O2+2CO2=2Na2CO3+O2(提示:Na2O2中的氧为-1价)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com