
【题目】【化学一选修3:物质结构与性质】A、B、C、D、E五种元素的原子序数依次增大。A 是原子半径最小的元素;B的最外层电子数是次外层电子数的2倍; D的L能层有两对成对电子;E+的核外有三个能层,且都外于全满状态。试回答下列问题:
(1)基态E原子核外电子的排布式为___________________。
(2)B、C、D三种元素的电负性由大到小的顺序是____________(填元素符号)。A、C、D三种元素形成的常见离子化合物中阳离子的空间构型为_____________,阴离子的中心原子轨道采用______________杂化。
(3)E(CA3)![]() 离子的颜色是___________;含有化学键类型是_____________;离子中C原子杂化轨道类型是__________________。
离子的颜色是___________;含有化学键类型是_____________;离子中C原子杂化轨道类型是__________________。
(4)D、E能形成两种晶体,其晶胞分别如甲、乙两图。晶体乙中,E的配位数为_________;在一定条件下,甲和C2A4反应生成乙,同时生成在常温下分别为气体和液体的另外两种常见无污染物质。该化学反应方程式为______________________。

(5)若甲的密度为ρ g/cm3,NA表示阿伏加德罗常数,则甲晶胞的边长可表示为_________cm。
【答案】(1)![]() ;
;
(2)O>N>C,正四面体,sp2;
(3)深蓝色,共价键、配位键,sp3;
(4)2,4CuO+N2H4![]() 2Cu2O+2H2O+N2↑;(5)
2Cu2O+2H2O+N2↑;(5)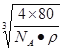
【解析】试题分析:A是原子半径最小的元素,即A为H,B的最外层是次外层电子数的2倍,即B为C,D的L层有两对成对电子,推出D为O,则C为N,E+的核外三个能层,且都处于全满状态,推出E为Cu,(1)铜位于第四周期,IB族,核外电子排布式为![]() ;(2)同周期从左向右,电负性增大,即O>N>C;构成离子化合物是NH4NO3,阳离子是NH4+,有4个σ键,孤电子对数为(5-1-4)/2=0,价层电子对数为4,因此空间构型为正四面体,阴离子是NO3-,有3个σ键,孤电子对数(5+1-3×2)/2=0.5,价层电子对数为4,杂化轨道数等于价层电子对数,即杂化类型为sp3;(3)化学式为Cu(NH3)42+,此离子显深蓝色,NH3中含有共价键,Cu2+和NH3间存在配位键,C2A4是N2H4,NH3中N的杂化类型是sp3;(4)根据乙的晶胞,Cu的配位数为2,D位于顶点:8×1/8=1,一个位于体心,D的个数为1+1=2,E位于体心,个数为4,因此化学式为Cu2O,生成无污染的气体,即N2,因此化学反应方程式为:4CuO+N2H4
;(2)同周期从左向右,电负性增大,即O>N>C;构成离子化合物是NH4NO3,阳离子是NH4+,有4个σ键,孤电子对数为(5-1-4)/2=0,价层电子对数为4,因此空间构型为正四面体,阴离子是NO3-,有3个σ键,孤电子对数(5+1-3×2)/2=0.5,价层电子对数为4,杂化轨道数等于价层电子对数,即杂化类型为sp3;(3)化学式为Cu(NH3)42+,此离子显深蓝色,NH3中含有共价键,Cu2+和NH3间存在配位键,C2A4是N2H4,NH3中N的杂化类型是sp3;(4)根据乙的晶胞,Cu的配位数为2,D位于顶点:8×1/8=1,一个位于体心,D的个数为1+1=2,E位于体心,个数为4,因此化学式为Cu2O,生成无污染的气体,即N2,因此化学反应方程式为:4CuO+N2H4![]() 2Cu2O+2H2O+N2↑;(5)甲中,Cu位于体心,真正属于晶胞的是4个,O的个数为8×1/8+2×1/2+1+4×1/4=4,甲的化学式为CuO,晶胞的质量为4×80/NAg,根据密度的定义,因此边长为
2Cu2O+2H2O+N2↑;(5)甲中,Cu位于体心,真正属于晶胞的是4个,O的个数为8×1/8+2×1/2+1+4×1/4=4,甲的化学式为CuO,晶胞的质量为4×80/NAg,根据密度的定义,因此边长为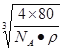 。
。


 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源: 题型:
【题目】将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是 ( )
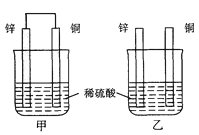
A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中溶液的pH均增大
D.产生气泡的速度甲比乙慢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对阿伏伽德罗定律及推论的理解不正确的是( )
A.同温同压下,气体的体积之比等于它们的物质的量之比
B.同温同压下,气体的体积之比等于它们的质量之比
C.同温同压下,相同体积的气体质量比等于它们的相对分子质量之比
D.同温同压下,气体的密度之比等于它们的相对分子质量之比
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)根据反应8NH3+3Cl2=6NH4Cl+N2,回答下列问题:
①该反应中氧化剂是 ,氧化产物是 。
②该反应中被氧化的物质与被还原的物质物质的量之比为 。
③用单线桥法标出点子转移的方向与数目。
(2)某一反应体系中存在下列6种物质:NO、FeSO4、Fe(NO3)3、HNO3、Fe2(SO4)3和H2O.已知存在下列转化关系:HNO3→NO,请完成下列各题:
①该反应的氧化剂是 ,还原剂是 。
②该反应中1mol氧化剂 (填“得到”或“失去”) mol电子。
③当有0.1molHNO3被还原,此时生成标准状况下NO的体积是 L。
④请把各物质填在下面空格处,需配平:
□______+□______=□______+□______+□______+□
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在“绿色化学工艺”中,理想状态是反应物中的原子全部转化为欲制得的产物,即原子利用率为100%,下列反应类型能体现“绿色化学工艺”的是( )
A.化合反应
B.复分解反应
C.分解反应
D.取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于铅蓄电池Pb+PbO2+2H2SO4![]() PbSO4+2H2O的说法正确的是
PbSO4+2H2O的说法正确的是
A.在放电时,正极发生的反应是Pb(s)+SO42—(aq)=PbSO4(s)+2e—
B.在放电时,该电池的负极材料是铅板
C.在充电时,电池中硫酸的浓度不断变小
D.在充电时,阳极发生的反应是PbSO4(s)+2e—=Pb(s)+SO42—(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
请根据所给装置回答下列问题:
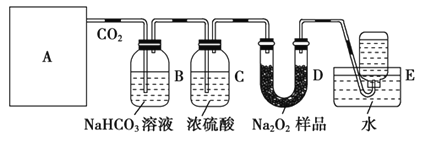
(1)A是制取CO2的装置,最好选用下列装置中的______________ (填序号)。
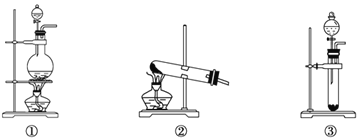
(2)B装置中发生的离子方程式是_______________________。C装置的作用是_______________________。
(3)D装置中发生反应的化学方程式是_________________。
(4)要想得到较纯净的氧气,可在装置D和E之间增加一盛有________(填写试剂名称)的________(填写装置名称)。
(5)如何检验集气瓶中收集到的气体______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与社会、生产、生活紧切相关,下列说法正确的是
A. 水玻璃可用于生产黏合剂和灭火剂
B. 煤的干馏、油脂的皂化和石油的分馏都属于化学变化
C. 高铁车厢大部分材料采用铝合金,因铝合金强度大、质量轻、抗腐蚀能力强
D. 发酵粉能使焙制出的糕点疏松多孔,是因为发酵粉中含有碳酸钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《自然》杂志在线发表了由中美两国华人科学家共同完成的一项突破“快速充放电铝离子电池”,其原理如下图所示。下列有关说法正确的是( )
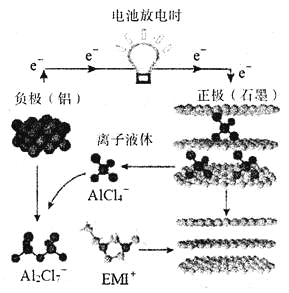
A. 电池放电时,负极反应式:Al-3e-=Al3+
B. 电池充电时,电池正极(石墨)上发生还原反应
C. 电池充电时,电路中每转移0.3 mol电子,理论上生成2.7g Al
D. 离子液体是一种能导电的物质,电池充电时,离子液体中EMI+向石墨电极移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com