
【题目】《自然》杂志在线发表了由中美两国华人科学家共同完成的一项突破“快速充放电铝离子电池”,其原理如下图所示。下列有关说法正确的是( )
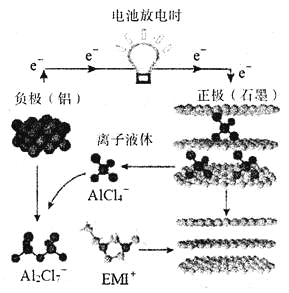
A. 电池放电时,负极反应式:Al-3e-=Al3+
B. 电池充电时,电池正极(石墨)上发生还原反应
C. 电池充电时,电路中每转移0.3 mol电子,理论上生成2.7g Al
D. 离子液体是一种能导电的物质,电池充电时,离子液体中EMI+向石墨电极移动
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】【化学一选修3:物质结构与性质】A、B、C、D、E五种元素的原子序数依次增大。A 是原子半径最小的元素;B的最外层电子数是次外层电子数的2倍; D的L能层有两对成对电子;E+的核外有三个能层,且都外于全满状态。试回答下列问题:
(1)基态E原子核外电子的排布式为___________________。
(2)B、C、D三种元素的电负性由大到小的顺序是____________(填元素符号)。A、C、D三种元素形成的常见离子化合物中阳离子的空间构型为_____________,阴离子的中心原子轨道采用______________杂化。
(3)E(CA3)![]() 离子的颜色是___________;含有化学键类型是_____________;离子中C原子杂化轨道类型是__________________。
离子的颜色是___________;含有化学键类型是_____________;离子中C原子杂化轨道类型是__________________。
(4)D、E能形成两种晶体,其晶胞分别如甲、乙两图。晶体乙中,E的配位数为_________;在一定条件下,甲和C2A4反应生成乙,同时生成在常温下分别为气体和液体的另外两种常见无污染物质。该化学反应方程式为______________________。

(5)若甲的密度为ρ g/cm3,NA表示阿伏加德罗常数,则甲晶胞的边长可表示为_________cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应与四个基本反应类型的关系如下图所示,则下列化学反应属于阴影部分的是( )

A.Cl2+2KBr=Br2+2KCl
B.2NaHCO3![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
C.4Fe(OH)2+O2+2H2O=4Fe(OH)3
D.2Na2O2+2CO2=2Na2CO3+O2(提示:Na2O2中的氧为-1价)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:C(s)+2H2(g)![]() CH4(g)。在VL的容器中投入amol碳(足量),同时通入2amol H2,控制条件使其发生上述反应,测得碳的平衡转化率随压强及温度的变化关系如下图所示。下列说法不正确的是( )
CH4(g)。在VL的容器中投入amol碳(足量),同时通入2amol H2,控制条件使其发生上述反应,测得碳的平衡转化率随压强及温度的变化关系如下图所示。下列说法不正确的是( )
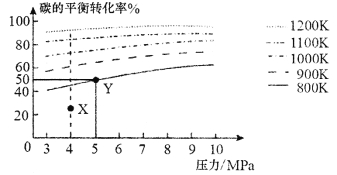
A.上述正反应为吸热反应
B.在4MPa、1200K时,图中X点v(H2)正>v(H2)逆
C.Y点H2的转化率为50%
D.工业上维持6MPa、1000K而不采用10MPa、1000K,主要是因为前者碳的转化率高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2O5是一种新型硝化剂,在一定温度下可发生以下反应:2N2O5(g)![]() 4NO2(g)+O2(g) △H>0一定温度时,向密闭容器中通入N2O5,部分实验数据见下表:
4NO2(g)+O2(g) △H>0一定温度时,向密闭容器中通入N2O5,部分实验数据见下表:
时间/s[K] | 0 | 500 | 1000 | 1500 |
c(N2O5)/mol/L | 0.50 | 0.35 | 0.25 | 0.25 |
下列说法中错误的是
A.500 s时O2的浓度为0.075 mol/L
B.平衡后,升高温度,正反应速率先增大后减小
C.平衡后,要使平衡常数增大,改变的条件是升高温度
D.1000 s时将容器的体积缩小一半,重新达到平衡时0.25 mol/L<c(N2O5)<0.50 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知3.0g AO32- 中核外电子数比质子数多6.02×1022个,下列说法中正确的是
A.A元素的相对原子质量为12
B.AO32-的摩尔质量为60
C.3.0gAO32- 的物质的量是0.02mol
D.A原子的摩尔质量32g/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为 1L的密闭容器中充入1mol CO和2mol H2混合气体,发生以下反应:CO(g)+2H2(g)![]() CH3OH(g)。T1、T2温度下,CH3OH的物质的量随着时间的变化关系如下图所示。下列有关说法正确的是
CH3OH(g)。T1、T2温度下,CH3OH的物质的量随着时间的变化关系如下图所示。下列有关说法正确的是

A.T1>T2
B.K(T1)>K(T2)
C.T1温度下达到平衡后,再充入一定量CO,CO的转化率增大
D.T2温度下,0~10min间v(H2)=0.06mol·L-1·min-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com