
【题目】下列说法中,正确的是( )
A. SO2能使FeCl3、酸性KMnO4溶液迅速褪色
B. 可以用澄清石灰水来鉴别SO2与CO2
C. 硫粉在过量的纯氧中燃烧可以生成SO3
D. 少量SO2通入浓的CaCl2溶液中可以生成白色沉淀
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
【题目】消除氮氧化物、二氧化硫等物质造成的污染是目前研究的重要课题。
(1)燃煤烟气脱硫常用如下方法。
①用生物质热解气(主要成分CO、CH4、H2)将SO2在高温下还原成单质硫。涉及的部分反应如下:2CO(g)+SO2(g)=S(g)+2CO2(g) △H1= + 8.0 kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H2=-566.0kJ·mol-1
2H2(g)+O2(g)=2H2O(g) △H3=-483.6 kJ·mol-1
则H2(g)还原SO2(g)生成S(g)和H2O(g)的热化学方程式为______________________。
②一氧化碳还原法:在绝热恒容的密闭容器中,反应2CO(g)+SO2(g)![]() S(s)+2CO2(g)达到平衡时,下列说法正确的是____(填序号)。
S(s)+2CO2(g)达到平衡时,下列说法正确的是____(填序号)。
a.容器内气体的压强保持不变 b.分离出S,正反应速率减小
若再充入一定量的CO2,反应的平衡常数不变
③用氨水将SO2转化为NH4HSO3,再氧化成(NH4)2SO4。实验测得NH4HSO3溶液中![]() =15,则溶液的pH为________。 (已知:H2SO3的Ka1=1.5×10-2,Ka2=1.0×10-7)
=15,则溶液的pH为________。 (已知:H2SO3的Ka1=1.5×10-2,Ka2=1.0×10-7)
(2)电解NO可以制备NH4NO3,其工作原理如下图所示,阳极的电极反应式为:____________,为使电解产物全部转化为NH4NO3,需补充物质A,A是___________ 。

(3)Na2S是常用的沉淀剂。某工业污水中含有等浓度的Cu2+、Fe2+、Pb2+,滴加Na2S溶液后首先析出的沉淀是________。当最后一种离子沉淀完全时(该离子浓度为10-5 mol·L-1),此时S2-的浓度为_________________________
(已知: Ksp(FeS)=6.3×10-18 ;Ksp(CuS)=6×10-36 ;Ksp(PbS)=2.4×10-28)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 沸点:邻二甲苯>间二甲苯>对二甲苯
B. 鸡蛋淸在NH4Cl溶液中能发生盐析,但是不能和盐酸发生化学反应
C.  有机物A的分子式为C16H16O3
有机物A的分子式为C16H16O3
D.  滴入酸性KMnO4溶液振荡,紫色褪去,能证明其结构中存在碳碳双键
滴入酸性KMnO4溶液振荡,紫色褪去,能证明其结构中存在碳碳双键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化硼的熔点为-107.3 ℃,沸点为12.5 ℃,易水解生成硼酸(H3BO3),可用于制造高纯硼、有机合成催化剂等。实验室制取三氯化硼的原理为B2O3+3C+3Cl2![]() 2BCl3+3CO。
2BCl3+3CO。
(1)甲组同学拟用下列装置制取纯净干燥的氯气(不用收集)。

①装置B中盛放的试剂是__,装置C的作用是___________________。
②装置A中发生反应的离子方程式为 _____________________________。
(2)乙组同学选用甲组实验中的装置A、B、C和下列装置(装置可重复使用)制取BCl3并验证反应中有CO生成。

①乙组同学的实验装置中,依次连接的合理顺序为
A→B→C→G→__→__→__→__→F→D→I。
②能证明反应中有CO生成的现象是___________________________。
③开始实验时,先点燃____(填“A” 或“G”)处的酒精灯。
④请写出BCl3水解的化学方程式__________________________。
⑤硼酸是一元弱酸,其钠盐化学式为Na [B(OH)4],则硼酸在水中电离方程式是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学蚀刻法是指用化学药品在一些固体材料表面腐蚀出图案的方法。下列蚀刻方法可行的是( )
A. 用氢氟酸蚀刻玻璃
B. 用浓HNO3蚀刻水晶
C. 用FeCl2溶液蚀刻铜板
D. 用Na2CO3溶液蚀刻大理石
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应A+B═C+D为放热反应,对该反应的下列说法中正确的为( )
A. A的能量一定高于C B. B的能量一定高于D
C. A和B的总能量一定高于C和D的总能量 D. 该反应为放热反应,故不必加热就一定能发生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1) 常温下,向 1 L 0.1 mol·L-1 的的醋酸溶液中加入0.1 mol醋酸钠固体,则醋酸的电离平衡向______(填“正”或“逆”)反应方向移动;溶液中c (CH3COO-)·c(H+) / c (CH3COOH) 的值 __________(填“增大”、“减小”或“不变”)。
(2)常温时,测得0.1 mol·L-1 Na2A 溶液的pH=7。
① H2A在水溶液中的电离方程式为 ______________________ 。
② 该温度下,将0.01 mol·L-1 H2A溶液稀释20倍后,溶液的pH= _______ 。
③ 体积相等、pH=1的盐酸与H2A溶液分别与足量的Zn反应,产生的氢气 _________ 。(填序号)
A 、盐酸多 B、 H2A多 C、一样多 D、无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法不正确的是
A. 某有机物化学式为C3H6O2,其核磁共振氢谱有三个峰,其峰的面积比为3:2:1,则该有机物的结构简式一定是CH3CH2COOH
B. 除去乙酸乙酯中的乙酸和乙醇杂质,可加入足量的饱和纯碱溶液,通过分液即得乙酸乙酯
C. 除去乙醇中的少量水,加入新制生石灰,经蒸馏即得乙醇
D. 有机物 ![]() 的系统名称为3-甲基-1-戊烯
的系统名称为3-甲基-1-戊烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂除去溶液中的NaCl和Na2SO4,从而得到纯净的NaNO3溶液。相应的实验过程可用下图表示: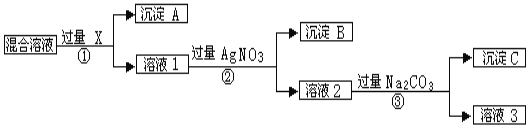
请回答下列问题:
(1)写出实验流程中下列物质的化学式:
试剂X_____________,沉淀A____________,沉淀B______________;
(2)上述实验流程中加入过量的Na2CO3的目的是____________________________。
(3)按此实验方案得到的溶液3中肯定含有__________(填化学式)杂质;为了解决这个问题,可以向溶液3中加入适量的___________(填化学式),之后若要获得固体NaNO3需进行的实验操作是__________________________(填操作名称)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com