
| A、氯乙烷与浓硫酸混和加热到170℃可发生消去反应生成乙烯 |
| B、苯与浓硝酸、浓硫酸的混和物加热到100~110℃时,因浓硝酸挥发和分解而得不到硝化产物 |
| C、将苯酚、40%的甲醛溶液和少量浓盐酸混和,水浴加热数分钟即可生成酚醛树脂 |
| D、酯化反应通常需要在浓硫酸存在下进行,浓硫酸此时既是催化剂又是吸水剂 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、2molC |
| B、2 molA、1 molB和1 molHe(不参加反应) |
| C、1 molB和1 molC |
| D、2 molA、2 molB和3 molC |
查看答案和解析>>
科目:高中化学 来源: 题型:
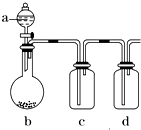 有几个实验小组的同学,利用如图装置进行“一器多用”的实验探究(a中盛放的液体均匀慢速滴下;b中盛放的药品足量;若在c、d中盛装液体,则长导管均浸入液面以下),每组同学设想在a、b、c、d中分别盛放不同物质,来制取某种气体并检验其性质.
有几个实验小组的同学,利用如图装置进行“一器多用”的实验探究(a中盛放的液体均匀慢速滴下;b中盛放的药品足量;若在c、d中盛装液体,则长导管均浸入液面以下),每组同学设想在a、b、c、d中分别盛放不同物质,来制取某种气体并检验其性质.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、食物中的主要成分能与酸反应的是碱性食物 |
| B、食物中的主要成分能与碱反应的是酸性食物 |
| C、食物在遇到甲基橙变红的是酸性食物,遇到酚酞变红的是碱性食物 |
| D、食物的酸碱性应当看食物在体内代谢完全后剩余物质的酸碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v (A)=0.3 mol?L-1?min-1 |
| B、v (B)=0.6 mol?L-1?min-1 |
| C、v (C)=0.5 mol?L-1?min-1 |
| D、v (A)=0.01 mol?L-1?s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
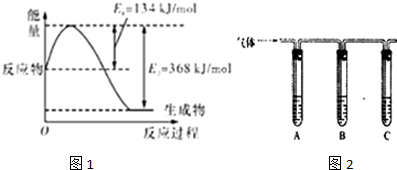
| 所加试剂 | 预期现象和结论 |
| 试管A中加足量 试管B中加1%品红溶液; 试管C中加 | 若 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com