
某绝热恒容容器中充入2mol/L NO2,发生反应2NO2 N2O4 △H=﹣56.9kJ/mol下列分析不正确的是( )
N2O4 △H=﹣56.9kJ/mol下列分析不正确的是( )
A. 5s时NO2的转化率为75%
B. 0﹣3s时v(NO2)增大是由于体系温度升高
C. 3s时化学反应处于平衡状态
D. 9s时再充入N2O4,平衡后K较第一次平衡时大
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016届甘肃省高三上学期期中联考化学试卷(解析版) 题型:选择题
CuSO4是一种重要的化工原料,其有关制备途径及性质如下图所示。下列说法不正确的是

A.相对于途径①,途径②更好地体现了绿色化学思想
B.Y可以是葡萄糖溶液
C.CuSO4在1100℃分解所得混合气体X一定有O2
D.途径①所用混酸中H2SO4与HNO3物质的量之比最好为3:1
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三上学期期中考试化学试卷(解析版) 题型:填空题
I.某化学反应的反应物和产物如下:Al + NaNO3 + H2O→Al(OH)3 + N2↑+ NaAlO2
(1)该反应中被还原的元素是 ,氧化产物是 。
(2)若反应过程中转移10mol 电子,则生成标准状况下N2的体积为 L。
(3)配平该反应的化学方程式,并用单线桥法标出电子转移的方向和数目。
Al + NaNO3 + H2O — Al(OH)3 + N2↑+ NaAlO2
II.已知食盐固体和SO3在高温下发生反应,生成等体积气体A(黄绿色)和漂白性气体B及硫酸钠。
(1)写出该反应的化学方程式为 。
(2)将上述反应产生的A和B的混合气体通入品红溶液,溶液不褪色。请用化学方程式表示其原因________________________________________。
(3)若将上述反应产生的A和B的混合气体先通过足量C溶液,再通入品红溶液,溶液褪色。C溶液可能是 (填序号)。
① 饱和食盐水 ② 饱和NaHSO3溶液 ③ 饱和Na2SO4溶液 ④ KMnO4溶液 ⑤ NaOH溶液
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江哈尔滨师大附中高三上学期期中考试化学试卷(解析版) 题型:选择题
下列有关仪器的使用正确的是
A.将固体药品放在蒸发皿中进行高温焙烧
B.六水氯化钙可用作食品干燥剂
C.向试管中滴加液体时胶头滴管一定应悬于试管口的正上方
D.冷凝管中冷却水的流向一定是下口进水、上口出水
查看答案和解析>>
科目:高中化学 来源:2016届贵州遵义航天高中高三上学期第三次模拟理综化学试卷(解析版) 题型:填空题
A、B、C、D、E、F、G为前四周期元素。A、B最外层电子排布可表示为asa、bsbbpb(a≠b);C元素对应单质是空气中含量最多的物质;D的最外层电子数是内层电子数的3倍;E与D同主族,且位于D的下一周期;F与E同周期,且是本周期中电负性最大的元素:基态G原子核外电子填充在7个能级中,且价层电子均为单电子。
(1)元素B、C、D的第一电离能由大到小的顺序为 (用元素符号表示)。
(2) ED3分子的空间构型为________,中心原子的杂化方式为________________________。
(3)四种分子①BA4②ED3③A2D④CA3键角由大到小排列的顺序是 (填序号)。
(4) CA3分子可以与A+离子结合成CA4+离子,这个过程中发生改变的是________(填序号)。
a.微粒的空间构型 b.C原子的杂化类型
c.A-C-A的键角 d.微粒的电子数
(5) EBC-的等电子体中属于分子的有 (填化学式),EBC-的电子式为 。
(6)G的价层电子排布式为________,化合物[G(CA3)6]F3的中心离子的配位数为 。
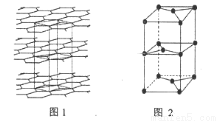
(7)B的某种单质的片层与层状结构如图1所示,其中层间距离为hcm.图2为从层状结构中取出的晶胞。试回答:
①在B的该种单质的片层结构中,B原子数、B-B键数、六元环数之比为 。
②若B的该种单质中B-B键长为a cm,则B的该种单质的密度为 g.cm-3。
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上学期期中考试化学试卷(解析版) 题型:选择题
甲~庚元素在周期表中的相对位置如下表,己的最高氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数。下列判断正确的是( )
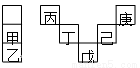
A.丙与戊的原子序数相差27
B.气态氢化物的稳定性:庚<己<戊
C.丁的最高价氧化物可用于制造光导纤维
D.常温下,甲和乙的单质均能与水剧烈反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林实验中学高二上学期期中考试化学试卷(解析版) 题型:选择题
某学生的实验报告所列出的下列数据中合理的是( )
A.用10mL量筒量取7.13mL稀盐酸
B.用托盘天平称量25.20g NaCl
C.用广泛pH试纸测得某溶液的pH为2.3
D.用25mL滴定管做中和滴定实验时,用去某浓度的碱溶液21.70mL
查看答案和解析>>
科目:高中化学 来源:2016届宁夏六盘山高级中学高三上学期期中考试化学试卷(解析版) 题型:选择题
下列实验操作正确且能达到相应实验目的的是
实验目的 | 实验操作 | |
A | 称取2.0 g NaOH固体 | 先在托盘上各放1张滤纸,然后在右盘上添加2 g砝码, 左盘上添加NaOH固体 |
B | 配制FeCl3溶液 | 将FeCl3固体溶于适量蒸馏水 |
C | 检验溶液中是否含NH4+ | 取少量试液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体 |
D | 验证铁的吸氧腐蚀 | 将铁钉放入试管中,用盐酸浸没 |
查看答案和解析>>
科目:高中化学 来源:2016届内蒙古鄂尔多斯市西部四校高三上学期期中联考化学试卷(解析版) 题型:填空题
某无色溶液,由Na+、Ag+、Ba2+、Al3+、AlO2-、MnO4-、CO32-、SO42-、SiO32-中的若干种组成(不考虑水的电离)。取该溶液进行如下实验:
Ⅰ.取适量溶液,加入过量的盐酸,有气体生成,并得到无色溶液;
Ⅱ.在Ⅰ所得溶液中加入过量的NH4HCO3溶液,有气体生成,同时析出白色沉淀甲;
Ⅲ.在Ⅱ所得溶液中加入过量的Ba(OH)2溶液,加热,也有气体生成,同时析出白色沉淀乙。
请回答下列问题:
(1)由实验Ⅰ可知原溶液中一定不含有的离子是__________;一定含有的离子是______。
(2)由实验Ⅱ可知原溶液中还一定含有的离子是________;生成甲的离子方程式为______________。
(3)实验Ⅲ中生成白色沉淀乙的离子方程式为_____________________。
(4)原溶液中还可能存在的离子是________;检验该离子的方法是____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com