
I.某化学反应的反应物和产物如下:Al + NaNO3 + H2O→Al(OH)3 + N2↑+ NaAlO2
(1)该反应中被还原的元素是 ,氧化产物是 。
(2)若反应过程中转移10mol 电子,则生成标准状况下N2的体积为 L。
(3)配平该反应的化学方程式,并用单线桥法标出电子转移的方向和数目。
Al + NaNO3 + H2O — Al(OH)3 + N2↑+ NaAlO2
II.已知食盐固体和SO3在高温下发生反应,生成等体积气体A(黄绿色)和漂白性气体B及硫酸钠。
(1)写出该反应的化学方程式为 。
(2)将上述反应产生的A和B的混合气体通入品红溶液,溶液不褪色。请用化学方程式表示其原因________________________________________。
(3)若将上述反应产生的A和B的混合气体先通过足量C溶液,再通入品红溶液,溶液褪色。C溶液可能是 (填序号)。
① 饱和食盐水 ② 饱和NaHSO3溶液 ③ 饱和Na2SO4溶液 ④ KMnO4溶液 ⑤ NaOH溶液
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016届山东省济宁市高三上学期期中考试化学试卷(解析版) 题型:选择题
一定条件下,下列各组物质中,Y既能与X反应又能与Z反应的是( )
X | Y | Z | |
① | NaOH溶液 | Al | Fe2O3 |
② | KOH溶液 | Br2 | Na2SO3溶液 |
③ | Na2CO3 | SiO2 | H2O |
④ | HCl | NaHCO3 | NaOH |
A.只有①③④ B.只有①②④ C.只有①②③ D.①②③④皆可
查看答案和解析>>
科目:高中化学 来源:2016届江苏省淮安市高三上学期10月阶段测化学试卷(解析版) 题型:实验题
在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙。下图所示A-E为实验室常见的仪器装置(部分固定夹持装置略去),请根据要求回答问题。
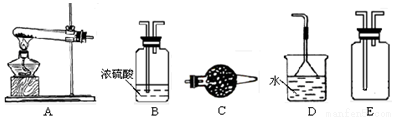
(1)实验空制取、收集干燥的NH3,需选用上述仪器装置中的 , 所用干燥剂的名称为 。
(2)向浓CaCl2溶液中通入NH3和CO2气体制纳米级碳酸钙时,应先通入的气体是 ,写出制纳米级碳酸钙的化学方程式: 。
(3)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级(1nm-100nm之间): 。
查看答案和解析>>
科目:高中化学 来源:2016届江西省南昌市高三上学期第四次考试化学试卷(解析版) 题型:实验题
碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂,在医药上也可用于治疗消化性溃疡出血。工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如下:
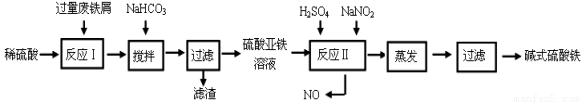
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
开始沉淀 | 2.3 | 7.5 | 3.4 | 完全沉淀 | 3.2 | 9.7 | 4.4 |
回答下列问题:
(1)加入少量NaHCO3的目的是调节pH在 范围内,使溶液中的 离子沉淀。
(2)反应Ⅱ中加入NaNO2,反应的离子方程式为 。
(3)在实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,若参与反应的O2有5.6 L(标准状况),则相当于节约NaNO2的物质的量为 。
(4)碱式硫酸铁溶于水后产生的Fe(OH)2+离子,Fe(OH)2+可部分水解生成Fe2(OH)42+ 聚合离子,该水解反应的离子方程式为 。
(5)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁。根据我国质量标准,产品中不得含有Fe2+及NO3-。为检验所得产品中是否含有Fe2+,应使用的试剂为 。
A.氯水 B.KSCN溶液 C.NaOH溶液 D.K3Fe(CN)6溶液
查看答案和解析>>
科目:高中化学 来源:2016届江西省南昌市高三上学期第三次考试化学试卷(解析版) 题型:选择题
在1L溶液中含有Fe(NO3)3和H2SO4两种溶质,其浓度分别为0.2mol/L和1.5mol/L,现向该溶液中加入39.2g铁粉使其充分反应,下列有关说法正确的是
A.反应后溶液中Fe3+物质的量为0.6mol
B.反应后产生13.44L H2(标准状况)
C.反应后溶液中Fe2+和Fe3+物质的量之和为0.8mol
D.由于氧化性Fe3+>H+,故反应中先没有气体产生后产生气体
查看答案和解析>>
科目:高中化学 来源:2016届江西上高第二中学高三12月月考理科综合化学试卷(解析版) 题型:填空题
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下:
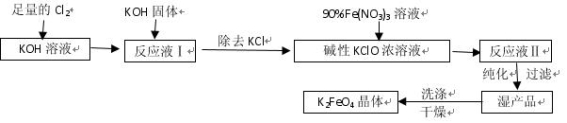
已知:① 2KOH + Cl2 = KCl + KClO + H2O(条件:温度较低)
② 6KOH + 3Cl2 = 5KCl + KClO3 + 3H2O(条件:温度较高)
(1)该生产工艺应在 (填“温度较高”或“温度较低”)情况下进行;
(2)写出工业上制取Cl2的化学方程式 ;
(3)在“反应液I”中加KOH固体的目的是 :
(4)加入硝酸铁溶液生成反应液Ⅱ的化学方程式:
(5)从“反应液Ⅱ”中分离出K2FeO4后,会有副产品 (写化学式),它们都是重要的化工产品,具体说出其中一种物质的用途 。
(6)将适量K2FeO4溶解于pH=4.74的溶液中,配制成c(FeO42-)=1.0 mmol·L-1的试样,将试样分别置于20℃、30℃、40℃和60℃的恒温水浴中,测定c(FeO42-)的变化,结果见图。该实验的目的是 ;发生反应的△H 0(填“>”、“<”或“=”)。

查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三第四次(12月)月考化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.pH=14的溶液中:K+、NH4+、NO3-、HCO3-
B.澄清透明的溶液:Cu2+、Mg2+、SO42-、Cl-
C.0.1mol·L-1Fe(NO3)2溶液中:H+、Ca2+、SCN-、Cl-
D.c(Fe2+)=1.0 mol·L-1溶液:H+、K+、Cl-、MnO4-
查看答案和解析>>
科目:高中化学 来源:2016届广西柳州铁路第一中学高三上学期10月月考理化学试卷(解析版) 题型:选择题
某绝热恒容容器中充入2mol/L NO2,发生反应2NO2 N2O4 △H=﹣56.9kJ/mol下列分析不正确的是( )
N2O4 △H=﹣56.9kJ/mol下列分析不正确的是( )
A. 5s时NO2的转化率为75%
B. 0﹣3s时v(NO2)增大是由于体系温度升高
C. 3s时化学反应处于平衡状态
D. 9s时再充入N2O4,平衡后K较第一次平衡时大
查看答案和解析>>
科目:高中化学 来源:2015-2016浙江宁波效实中学高二上期中考试化学试卷卷(解析版) 题型:简答题
氨气是重要化工产品之一。传统的工业合成氨技术的反应原理是:N2(g)+3H2(g) NH3(g)ΔH=-92.4 kJ/mol。在500 ℃、20 MPa时,将N2、H2置于一个固定容积的密闭容器中发生反应,反应过程中各种物质的量变化如图所示,回答下列问题:
NH3(g)ΔH=-92.4 kJ/mol。在500 ℃、20 MPa时,将N2、H2置于一个固定容积的密闭容器中发生反应,反应过程中各种物质的量变化如图所示,回答下列问题:
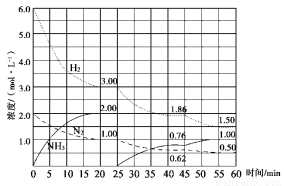
(1)计算反应在第一次平衡时的平衡常数K= 。(保留二位小数)
(2)产物NH3在5~10 min、25~30min和45~50 min时平均反应速率(平均反应速率分别以v1、v2、v3表示)从大到小排列次序为 。
(3)H2在三次平衡阶段的平衡转化率分别以α1、α2、α3表示,其中最小的是 。
(4)由第一次平衡到第二次平衡,平衡移动的方向是_______,采取的措施是________ 。
(5)请在下图中用实线表示25~60min 各阶段化学平衡常数K的变化图像。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com