
在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙。下图所示A-E为实验室常见的仪器装置(部分固定夹持装置略去),请根据要求回答问题。
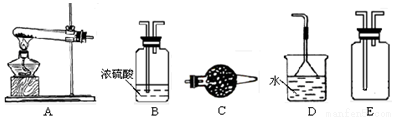
(1)实验空制取、收集干燥的NH3,需选用上述仪器装置中的 , 所用干燥剂的名称为 。
(2)向浓CaCl2溶液中通入NH3和CO2气体制纳米级碳酸钙时,应先通入的气体是 ,写出制纳米级碳酸钙的化学方程式: 。
(3)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级(1nm-100nm之间): 。
 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源:2016届四川省成都市高三上学期期中考试化学试卷(解析版) 题型:选择题
下列解释事实的化学方程式或离子方程式不正确的是
A.向AgCl悬浊液中加入KI溶液:AgCl(s)+I-(aq)=AgI(s)+Cl-(aq)
B.明矾净水:Al3++3H2O Al(OH)3+3H+
Al(OH)3+3H+
C.90℃时,测得纯水中Kw=3.8×10-13:H2O(l) H+(aq)+OH-(aq) △H<0
H+(aq)+OH-(aq) △H<0
D.用热的纯碱溶液可以清洗油污:CO32-+H2O HCO3-+OH-
HCO3-+OH-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高一上学期期中测试化学试卷(解析版) 题型:选择题
报道,科学家已成功合成了少量N4,有关N4的说法正确的是
A.N4和N2是互为同位素
B.N4的摩尔质量是56g
C.相同质量的N4和N2所含原子个数比为2:1
D.每个N4分子含有28个电子
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省高三上学期期中联考化学试卷(解析版) 题型:选择题
CuSO4是一种重要的化工原料,其有关制备途径及性质如下图所示。下列说法不正确的是

A.相对于途径①,途径②更好地体现了绿色化学思想
B.Y可以是葡萄糖溶液
C.CuSO4在1100℃分解所得混合气体X一定有O2
D.途径①所用混酸中H2SO4与HNO3物质的量之比最好为3:1
查看答案和解析>>
科目:高中化学 来源:2016届湖南省澧县、桃源、益阳三校高三上学期联考化学试卷(解析版) 题型:选择题
碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图),下列说法正确的是
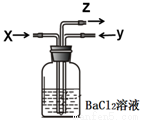
A.洗气瓶中产生的沉淀是BaCO3
B.Z导管出来的气体中无CO2
C.洗气瓶中产生的沉淀只有BaSO4
D.洗气瓶中产生的沉淀可能有BaSO3
查看答案和解析>>
科目:高中化学 来源:2016届江苏省淮安市高三上学期10月阶段测化学试卷(解析版) 题型:选择题
下列关于一部分单质和氧化物、酸、碱、盐分类的说法正确的是
①纯碱②硝酸铜③食盐④硝酸⑤盐酸⑥硫酸钠⑦硫酸⑧火碱⑨生石灰⑩氯气
A、含氧酸盐有①②③⑥
B、①和⑧是同一种物质
C、可以把⑥归类为: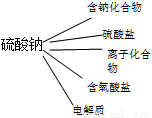
D、不能把⑦和⑧归为一类物质
查看答案和解析>>
科目:高中化学 来源:2016届辽宁师范大学附属中学高三上学期期中考试化学试卷(解析版) 题型:填空题
短周期元素A、B、C、D在周期表中的位置如图所示:B、D最外层电子数之和为12。回答下列问题:
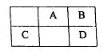
(1)与元素B、D处于同一主族的第2-5周期元素单质分别与H2反应生成1 mol气态氢化物对应的热量变化如下,其中能表示该主族第4周期元素的单质生成1 mol气态氢化物所对应的热量变化是_______(选填字母编号)。
a.吸收99.7kJ b.吸收29.7kJ c.放出20.6kJ d.放出241.8 kJ
(2)DB2通过下列工艺流程可制化工业原料H2DB4和清洁能源H2。

①查得:
化学键 | H-H | Br-Br | H-Br |
键能(kJ/mol) | 436 | 194 | 362 |
试写出通常条件下电解槽中发生总反应的热化学方程式: 。
②根据资料:
化学式 | Ag2SO4 | AgBr |
溶解度(g) | 0.796 | 8.4×10-6 |
为检验分离器的分离效果,取分离后的H2DB4溶液于试管,向其中逐滴加入AgNO3溶液至充分反应,若观察到 ,证明分离效果较好。
③在原电池中,负极发生的反应式为 。
④在电解过程中,电解槽阴极附近溶液pH (填“变大”、“变小”或“不变”)。
⑤将该工艺流程用总反应的化学方程式表示为: 。该生产工艺的优点有 (答一点即可)。
(3)溴及其化合物广泛应用于医药、农药、纤维、塑料阻燃剂等,回答下列问题:海水提溴过程中,向浓缩的海水中通入________,将其中的Br-氧化,再用空气吹出溴;然后用碳酸钠溶液吸收溴,溴歧化为Br-和BrO3-,其离子方程式为________________ 。
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三上学期期中考试化学试卷(解析版) 题型:填空题
I.某化学反应的反应物和产物如下:Al + NaNO3 + H2O→Al(OH)3 + N2↑+ NaAlO2
(1)该反应中被还原的元素是 ,氧化产物是 。
(2)若反应过程中转移10mol 电子,则生成标准状况下N2的体积为 L。
(3)配平该反应的化学方程式,并用单线桥法标出电子转移的方向和数目。
Al + NaNO3 + H2O — Al(OH)3 + N2↑+ NaAlO2
II.已知食盐固体和SO3在高温下发生反应,生成等体积气体A(黄绿色)和漂白性气体B及硫酸钠。
(1)写出该反应的化学方程式为 。
(2)将上述反应产生的A和B的混合气体通入品红溶液,溶液不褪色。请用化学方程式表示其原因________________________________________。
(3)若将上述反应产生的A和B的混合气体先通过足量C溶液,再通入品红溶液,溶液褪色。C溶液可能是 (填序号)。
① 饱和食盐水 ② 饱和NaHSO3溶液 ③ 饱和Na2SO4溶液 ④ KMnO4溶液 ⑤ NaOH溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林实验中学高二上学期期中考试化学试卷(解析版) 题型:选择题
某学生的实验报告所列出的下列数据中合理的是( )
A.用10mL量筒量取7.13mL稀盐酸
B.用托盘天平称量25.20g NaCl
C.用广泛pH试纸测得某溶液的pH为2.3
D.用25mL滴定管做中和滴定实验时,用去某浓度的碱溶液21.70mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com