
氨气是重要化工产品之一。传统的工业合成氨技术的反应原理是:N2(g)+3H2(g) NH3(g)ΔH=-92.4 kJ/mol。在500 ℃、20 MPa时,将N2、H2置于一个固定容积的密闭容器中发生反应,反应过程中各种物质的量变化如图所示,回答下列问题:
NH3(g)ΔH=-92.4 kJ/mol。在500 ℃、20 MPa时,将N2、H2置于一个固定容积的密闭容器中发生反应,反应过程中各种物质的量变化如图所示,回答下列问题:
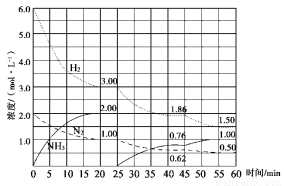
(1)计算反应在第一次平衡时的平衡常数K= 。(保留二位小数)
(2)产物NH3在5~10 min、25~30min和45~50 min时平均反应速率(平均反应速率分别以v1、v2、v3表示)从大到小排列次序为 。
(3)H2在三次平衡阶段的平衡转化率分别以α1、α2、α3表示,其中最小的是 。
(4)由第一次平衡到第二次平衡,平衡移动的方向是_______,采取的措施是________ 。
(5)请在下图中用实线表示25~60min 各阶段化学平衡常数K的变化图像。

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016届江西省高三上学期期中考试化学试卷(解析版) 题型:填空题
I.某化学反应的反应物和产物如下:Al + NaNO3 + H2O→Al(OH)3 + N2↑+ NaAlO2
(1)该反应中被还原的元素是 ,氧化产物是 。
(2)若反应过程中转移10mol 电子,则生成标准状况下N2的体积为 L。
(3)配平该反应的化学方程式,并用单线桥法标出电子转移的方向和数目。
Al + NaNO3 + H2O — Al(OH)3 + N2↑+ NaAlO2
II.已知食盐固体和SO3在高温下发生反应,生成等体积气体A(黄绿色)和漂白性气体B及硫酸钠。
(1)写出该反应的化学方程式为 。
(2)将上述反应产生的A和B的混合气体通入品红溶液,溶液不褪色。请用化学方程式表示其原因________________________________________。
(3)若将上述反应产生的A和B的混合气体先通过足量C溶液,再通入品红溶液,溶液褪色。C溶液可能是 (填序号)。
① 饱和食盐水 ② 饱和NaHSO3溶液 ③ 饱和Na2SO4溶液 ④ KMnO4溶液 ⑤ NaOH溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林实验中学高二上学期期中考试化学试卷(解析版) 题型:选择题
某学生的实验报告所列出的下列数据中合理的是( )
A.用10mL量筒量取7.13mL稀盐酸
B.用托盘天平称量25.20g NaCl
C.用广泛pH试纸测得某溶液的pH为2.3
D.用25mL滴定管做中和滴定实验时,用去某浓度的碱溶液21.70mL
查看答案和解析>>
科目:高中化学 来源:2016届宁夏六盘山高级中学高三上学期期中考试化学试卷(解析版) 题型:选择题
下列实验操作正确且能达到相应实验目的的是
实验目的 | 实验操作 | |
A | 称取2.0 g NaOH固体 | 先在托盘上各放1张滤纸,然后在右盘上添加2 g砝码, 左盘上添加NaOH固体 |
B | 配制FeCl3溶液 | 将FeCl3固体溶于适量蒸馏水 |
C | 检验溶液中是否含NH4+ | 取少量试液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体 |
D | 验证铁的吸氧腐蚀 | 将铁钉放入试管中,用盐酸浸没 |
查看答案和解析>>
科目:高中化学 来源:2015-2016浙江宁波效实中学高一上期中考试化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.容量瓶和量筒上均标有温度,且量筒和容量瓶均无“0”刻度
B.用丁达尔现象可鉴别蛋白质溶液、葡萄糖溶液和淀粉溶液
C.用洁净玻璃棒蘸取少量溶液,放在酒精灯上灼烧,透过蓝色钴玻璃观察K的焰色
D.检验某溶液是否含有SO42-时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸
查看答案和解析>>
科目:高中化学 来源:2015-2016浙江宁波效实中学高二上期中考试化学试卷卷(解析版) 题型:选择题
室温下向10mL pH=3的醋酸溶液中加水稀释后,下列说法正确的是
A.溶液中所有粒子的浓度都减少
B.溶液中 不变
不变
C.醋酸的电离程度增大,c(H+)亦增大
D.再加入10mL pH=11的NaOH溶液,混合液pH=7
查看答案和解析>>
科目:高中化学 来源:2015-2016宁夏回族自治银川一中高一上期中考试化学试卷(解析版) 题型:选择题
下列电离方程式错误的是
A.KNO3 = K+ + NO3-
B.NaHSO4 = Na+ + H+ + SO42-
C.BaCl2 = Ba2+ + Cl2-
D.Na2SO4 = 2Na+ + SO42-
查看答案和解析>>
科目:高中化学 来源:2016届内蒙古鄂尔多斯市西部四校高三上学期期中联考化学试卷(解析版) 题型:填空题
某无色溶液,由Na+、Ag+、Ba2+、Al3+、AlO2-、MnO4-、CO32-、SO42-、SiO32-中的若干种组成(不考虑水的电离)。取该溶液进行如下实验:
Ⅰ.取适量溶液,加入过量的盐酸,有气体生成,并得到无色溶液;
Ⅱ.在Ⅰ所得溶液中加入过量的NH4HCO3溶液,有气体生成,同时析出白色沉淀甲;
Ⅲ.在Ⅱ所得溶液中加入过量的Ba(OH)2溶液,加热,也有气体生成,同时析出白色沉淀乙。
请回答下列问题:
(1)由实验Ⅰ可知原溶液中一定不含有的离子是__________;一定含有的离子是______。
(2)由实验Ⅱ可知原溶液中还一定含有的离子是________;生成甲的离子方程式为______________。
(3)实验Ⅲ中生成白色沉淀乙的离子方程式为_____________________。
(4)原溶液中还可能存在的离子是________;检验该离子的方法是____________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高二上学期期中测试化学试卷(解析版) 题型:选择题
为提纯下列物质(括号内的物质为杂质),所用的除杂试剂和分离方法都正确的是
选项 | A | B | C | D |
被提纯物质 | 酒精(水) | 乙醇(乙酸) | 乙烷(乙烯) | 溴苯(溴) |
除杂试剂 | 生石灰 | 氢氧化钠溶液 | 酸性高锰酸钾溶液 | KI溶液 |
分离方法 | 蒸馏 | 分液 | 洗气 | 分液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com