
【题目】下列解释事实的方程式,不正确的是
A.铁粉与硫粉混合加热反应:Fe + S![]() FeS
FeS
B.红热的铜丝与硫蒸气化合:Cu + S ![]() CuS
CuS
C.镁条在氮气中燃烧:3Mg+N2 ![]() Mg3N2
Mg3N2
D.红热的木炭与浓硫酸反应:C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
科目:高中化学 来源: 题型:
【题目】将4molA和2molB在2L的密闭容器内混合,并在一定条件下发生如下反应:2A(s)+B(g)2C(g),若经2s后测得C的浓度为0.6mol·L-1,现有下列几种说法:①用物质A表示的反应的平均速率为0.3mol·L-1·s-1②用物质B表示的反应的平均速率为0.6mol·L-1·s-1③2s时物质A的转化率为30%④2s时物质B的浓度为0.7mol·L-1其中正确的是( )
A. ①③B. ①④C. ②③D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属材料、无机非金属材料、有机高分子材料是人类使用的三大类基础材料,它们以各自的特点满足着人类多方面的需要。
(1)金属材料中,有一类贮氢合金能够结合氢气形成金属化合物,并在一定条件下分解释放出氢气,该贮运原理属于_______变化,钢铁是制造轮船的主要金属材料,船身外通常装上一定数目比铁更活泼的金属块以防止腐蚀,该金属块可以选择_______(选填“铜块”、“锌块”、“铅块”);
(2)无机非金属材料中,用于电子工业的高纯碳酸钙、高纯氧化钙生产流程如下:

请回答下列问题:
①硝酸钙与碳酸铵在溶液中反应,其基本反应类型为_______;
②实验室常采用_______操作进行沉淀分离;
③生产高纯碳酸钙时,选择“220℃恒温干燥”而不选择“灼烧”的原因是_______;
④高纯氧化钙生产过程中,“干燥”的主要目的是为了防止______(用化学方程式表示);
(3)有机高分子材料“玉米塑料”,因其可降解被广泛用来替代一次性泡沫塑料,“玉米塑料”的使用可减少_______污染,20世纪30年代,尼龙因其抽成细丝极像蚕丝而被推向世界,生活中可采用______方法区分尼龙和蚕丝。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】十九大 报告提出要“打赢蓝天保卫战”,意味着对大气污染防治比以前更高。二氧化硫-空气质子交换膜燃料电池将化学能转变成电能的同时, 实现了制硫酸、发电、环保三位一体的结合,降低了成本提高了效益, 其理原如图所示。下列说法错误的是
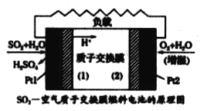
A.Ptl 电极附近发生的反应为:SO2+ 2H2O-2e- =SO42-+4H+
B.该电池放电时电子从Pt l电极经过外电路流到Pt2电极
C.Pt2电极附近发生的反应为O2+4e- =2O2-
D.相同条件下,放电过程中消耗的 SO2和O2的体积比为 2 : 1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是元素周期表的一部分,A、B、C均为短周期元素,A、C两种元素的原子核外电子数之和等于B的质子数,B的原子核内质子数和中子数相等。回答:
![]()
(1)写出元素符号:A_________;C___________。
(2)B的最高价氧化物对应水化物的化学式为_____。
(3)A的单质的电子式为______; A的氢化物的水溶液与其最高价氧化物的水化物反应的化学方程式为___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】稀土元素包括钪、钇和镧系(含Ce、Eu )共17种元素, 是重要的战略资源,我省稀土资源非常丰富.某彩色电视机显示屏生产过程中产生大量的废荧光粉末含 ( Eu2O3、SiO2、Fe2O3、CeO2、MnO 等物质).某课题组以此粉末为原料, 设计如下工艺流程对资源进行回收,得到较为纯净的CeO2和Eu2O3 (氧化铕).
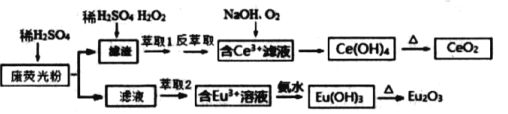
已知:CeO2 不溶于桸硫酸,也不溶于NaOH 溶液,Eu2O3可溶于稀硫酸
(1)往滤渣中加稀硫酸和H2O2进行酸浸,反应的离子方程式____________ 。为了提高酸浸率,可以适当提高反应温度,但温度偏高浸出率反而会减小,其原因是________________________________。
(2)有机物HR能将Ce3+从水溶液中萃取出来.该过程可表示为:Ce3+(水层)+3HR(有机层)![]() CeR3(有机层)+3H+(水层)。向 CeR3(有机层)中加入稀硫酸进行反萃取能获得较纯的含Ce3+水溶液,从平衡角度解释其原因:________________________。
CeR3(有机层)+3H+(水层)。向 CeR3(有机层)中加入稀硫酸进行反萃取能获得较纯的含Ce3+水溶液,从平衡角度解释其原因:________________________。
(3)流程中由含 Ce3+滤液生成Ce(OH)4的离子方程式____________________。
(4)取上述流程中得到的Ce(OH)4 产品 0.52 g, 加硫酸溶解后,用浓度为 0.1000molL-1FeSO4标准溶液滴定至终点时,铈被还原为Ce3+ , 消耗 24.00 mL 标准溶液。该产品中 Ce(OH)4的质量分数为___________。
(5)已知含 Ce3+溶液也可以先加碱调 pH后再通入氧气氧化可得到Ce(OH)4。298K 时,Ksp[Ce(OH)3]=5×10-20,若溶液中c(Ce3+)=0.05molL-1, 加碱调节pH 到_____时Ce3+开始沉淀(忽略加碱过程中溶液体积变化).
(6)萃取剂对金属离子的萃取率与 pH的关系如图所示.流程中为了用萃取剂除去金属杂质离子,进行萃取2 最适宜的pH 是_______(填选项序号).其原因是 _____。
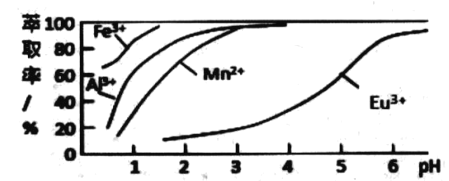
A. 2.0 左右 B . 3.0 左右 C. 5.0 左右
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化钡(Ba3N2)是一种重要的化学试剂。高温下,向氢化钡(BaH2)中通入氮气反应生成氮化钡。可用如图装置制备氮化钡。已知:Ba3N2遇水反应;BaH2在潮湿空气中能自燃,遇水反应。下列说法不正确的是( )
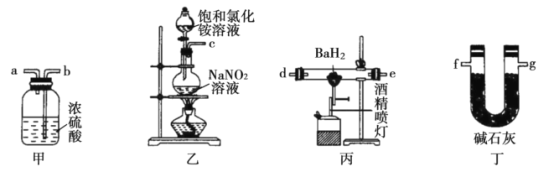
A.在实验室中可以用装置乙制备氯气
B.实验时,先点燃装置丙中的酒精喷灯,后点燃装置乙中的酒精灯
C.气流从左向右的字母连接顺序为c→b→a→d→e→g→f
D.装置甲中的浓硫酸和装置丁中的碱石灰作用相同,均可防止水蒸气进入装置丙中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化铬(Cr2O3)的性质独特,在冶金、颜料等领域有着不可替代的地位。一种利用淀粉水热还原铬酸钠制备氧化铬的工艺流程如图:
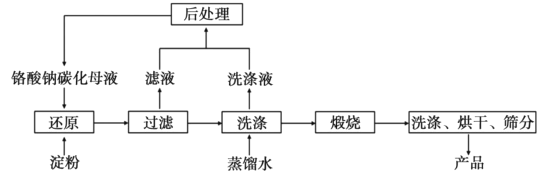
已知:①向含少量Na2CO3的铬酸钠碱性溶液中通入CO2可制得不同碳化率的铬酸钠碳化母液。
②“还原”反应剧烈放热,可制得Cr(OH)3浆料。
(1)该工艺中“还原”反应最初使用的是蔗糖或甲醛,后来改用价格低廉的淀粉。请写出甲醛(HCHO)与铬酸钠(Na2CrO4)溶液反应的离子方程式__。
(2)将混合均匀的料液加入反应釜,密闭搅拌,恒温发生“还原”反应,下列有关说法错误的是__(填标号)。
A.该反应一定无需加热即可进行
B.必要时可使用冷却水进行温度控制
C.铬酸钠可适当过量,使淀粉充分反应
D.应建造废水回收池,回收含铬废水
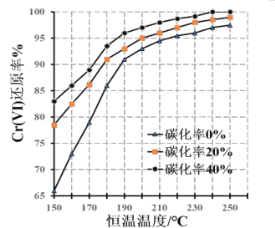
(3)测得反应完成后在不同恒温温度、不同碳化率下Cr(Ⅵ)还原率如图。实际生产过程中Cr(Ⅵ)还原率可高达99.5%以上,“还原”阶段采用的最佳反应条件为_、__。
(4)滤液中所含溶质为__。该水热法制备氧化铬工艺的优点有__、__(写出两条即可)。
(5)由水热法制备的氢氧化铬为无定型氢氧化铬[2Cr(OH)3H2O]。将洗涤并干燥后的氢氧化铬滤饼充分煅烧,失去质量与固体残留质量比为_。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.某同学做如下实验,以探究反应中的能量变化。
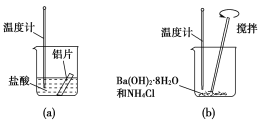
(1)在实验中发现反应后(a)中温度升高,由此可以判断(a)中反应是________热反应;(b)中温度降低,由此可以判断(b)中反应是________热反应。
(2)根据能量守恒定律,(b)中反应物的总能量应该________生成物的总能量。
II.某学习小组依据氧化还原反应原理:2Ag++Cu=Cu2++2Ag设计成的原电池如右图所示。
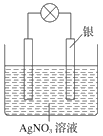
(3) 从能量转化角度分析,上述原电池将化学能转化为_________ ;
(4) 负极的电极材料为_____________;
(5) 正极发生的电极反应__________________________________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com