
����Ŀ����4molA��2molB��2L���ܱ������ڻ�ϣ�����һ�������·������·�Ӧ��2A��s��+B��g��2C��g��������2s����C��Ũ��Ϊ0.6mol��L-1���������м���˵������������A��ʾ�ķ�Ӧ��ƽ������Ϊ0.3mol��L-1��s-1��������B��ʾ�ķ�Ӧ��ƽ������Ϊ0.6mol��L-1��s-1��2sʱ����A��ת����Ϊ30%��2sʱ����B��Ũ��Ϊ0.7mol��L-1������ȷ���ǣ� ��
A. �٢�B. �٢�C. �ڢ�D. �ۢ�
���𰸡�D
��������
��������ʽ�����㣺B��Ũ��Ϊ![]() =1mol/L
=1mol/L
2A��s��+B��g��2C��g��
��ʼ��mol/L���� 1 0
�仯��mol/L���� 0.3 0.6
2sʱ��mol/L���� 0.7 0.6
��AΪ���壬���ڹ����Ũ���ڷ�Ӧ�в��ı䣬���Բ����ù�����������ʾ��Ӧ���ʣ��ʢٴ���
��2s�ڣ�������B��ʾ�ķ�Ӧ��ƽ������Ϊv��B��=![]() =0.15molL-1s-1���ʢڴ���
=0.15molL-1s-1���ʢڴ���
��2sʱ����A��ת����Ϊ��=![]() ��100%=30%���ʢ���ȷ��
��100%=30%���ʢ���ȷ��
��2sʱ����B��Ũ��Ϊ0.7molL-1���ʢ���ȷ��
������ȷ��Ϊ�ۢܡ�
��ѡD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����º����£���l molX��2 molY�����ܱ������з�����Ӧ��X(s)+2Y(g)![]() 2Z(g)��10 min��ﵽƽ��״̬������˵����ȷ����
2Z(g)��10 min��ﵽƽ��״̬������˵����ȷ����
A. ƽ��ǰ��������ѹǿ�淴Ӧ���ж���С
B. ƽ���������Y��Z�����ʵ���֮��һ��Ϊ1:1
C. 10 min�������¶ȣ�Y�ķ�Ӧ���ʲ���
D. ����Z�����ʵ���һ��С��2 moI
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z�����ڱ������ڵ���Ԫ�أ�X��Yͬ���ڣ�Y��Zͬ���壬��ԭ�ӵ�����������֮��Ϊ14��������֮��Ϊ28������Ԫ��Ϊ�� ��
A.N��P��OB.N��C��SiC.C.B��Mg��AlD.C��N��P
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��ӦA2��B2===2AB�������仯��ͼ��ʾ��������˵����ȷ���ǣ� ��
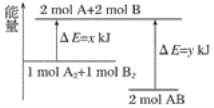
A. �÷�Ӧ�����������ķ�Ӧ
B. 1molA��A����1molB��B�������ܷų�xkJ������
C. 2molA��B��������Ҫ����ykJ������
D. 2molAB������������1molA2��1molB2��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʳ�е�����Ҫ������ʳ���У������������Ҫ�ĵ�ζƷ��Ҳ�DZ�֤����ˮ��ƽ�������Ҫ���ʡ���ȱ��֢���������������ʳ�����ˡ�����ʧˮ���ؼ��ᡢ���⾷�Ρ����ġ���к��ͷʹ����ʳ�г������������ƽ����¸�Ѫѹ�������漰������ָ���ǣ� ��
A.�Ƶ���B.ʳ��C.������D.̼������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£���Ӧ2N2O5![]() 4NO2+O2��ʼʱc(N2O5)=0.0408mol��L-1����1 min����c(N2O5)=0.030mol��L-1����÷�Ӧ�ķ�Ӧ����Ϊ
4NO2+O2��ʼʱc(N2O5)=0.0408mol��L-1����1 min����c(N2O5)=0.030mol��L-1����÷�Ӧ�ķ�Ӧ����Ϊ
A. v(N2O5)=1.08��10-4 molL-1s-1 B. v(N2O5)= 1.8��10-1 molL-1min
C. v(O2)=9.0��10-5 molL-1s-1 D. 2 v(NO2)= v(N2O5)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������к��е����ʣ�������Ϊ���ʣ��������ü��ȵķ�����ȥ���ǣ� ��
A.CaCO3��CaO��B.Cu��CuO��
C.Na2CO3��NaHCO3��D.NaHCO3��Na2CO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʽΪC4H10O����������Ʒ�Ӧ�ų��������л�����
A. 4�� B. 5�� C. 6�� D. 7��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����ͼ������ȼ�ϵ�ع���ʾ��ͼ��
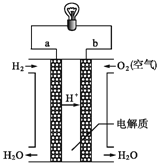
д������ȼ�ϵ�صĵ缫��Ӧʽ��
������______________________________��������__________________________________��
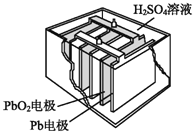
��2��������������Դ����Ǧ���ء���ṹ��ͼ��ʾ���ŵ�ʱ�ĵ�ط�Ӧ���£�PbO2+Pb+2H2SO4=2PbSO4+2H2O��д�������ĵ缫��Ӧʽ��_____________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com