
【题目】(1)下图是氢氧燃料电池构造示意图。
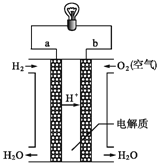
写出氢氧燃料电池的电极反应式:
负极:______________________________,正极:__________________________________。
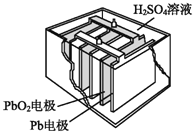
(2)汽车的启动电源常用铅蓄电池。其结构如图所示,放电时的电池反应如下:PbO2+Pb+2H2SO4=2PbSO4+2H2O。写出正极的电极反应式:_____________________。
【答案】H2—2e—=2H+ O2+4H++4e—=2H2O PbO2+4H++SO42—+2e—=PbSO4+2H2O
【解析】
(1)燃料电池中,一般燃料在负极发生反应,O2在正极发生反应;注意电解质溶液的酸碱性。
(2)原电池的正极发生还原反应。
(1)氢氧燃料电池中,H2在负极发生反应,电解质溶液为酸性,则H2+2e=2H+;O2在正极得到电子,和溶液中的H+结合生成水,方程式为O2+4e-+4H+=2H2O;
(2)正极发生的反应为还原反应,得到电子,化合价降低,分析化合价,得电子的为PbO2,生成PbSO4。方程式为PbO2+4H++SO42—+2e—=PbSO4+2H2O。


科目:高中化学 来源: 题型:
【题目】将4molA和2molB在2L的密闭容器内混合,并在一定条件下发生如下反应:2A(s)+B(g)2C(g),若经2s后测得C的浓度为0.6mol·L-1,现有下列几种说法:①用物质A表示的反应的平均速率为0.3mol·L-1·s-1②用物质B表示的反应的平均速率为0.6mol·L-1·s-1③2s时物质A的转化率为30%④2s时物质B的浓度为0.7mol·L-1其中正确的是( )
A. ①③B. ①④C. ②③D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤块的主要成分是MgCl2,此外还含Fe3+、Fe2+和Mn2+等离子。若以它为原料按下图所示工艺流程进行生产,可制得轻质氧化镁。
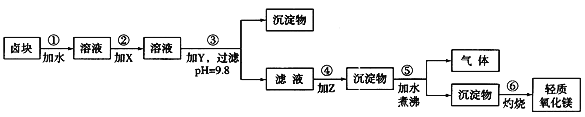
若要求产品尽量不含杂质,而且生产成本较低,请根据表1和表2提供的资料,填写空白:
表1 生成氢氧化物沉淀的pH
物质 | 开始沉淀 | 沉淀完全 |
Fe(OH)3 | 2.7 | 3.7 |
Fe(OH)2 | 7.6 | 9.6﹡ |
Mn(OH)2 | 8.3 | 9.8 |
Mg(OH)2 | 9.6 | 11.1 |
﹡Fe2+氢氧化物呈絮状,不易从溶液中除去,所以,常将它氧化为Fe3+,生成Fe(OH)3沉淀除去
表2 原料价格表
物质 | 价格/(元·吨-1) |
漂液(含25.2%NaClO) | 450 |
双氧水(含30%H2O2) | 2400 |
烧碱(含98%NaOH) | 2100 |
纯碱(含99.5%Na2CO3) | 600 |
(1)在步骤②中加入的试剂X,最佳的选择是____________,其作用是_________________;
(2)在步骤③中加入的试剂应是_______________________;之所以要控制pH=9.8,其目的是___________________________________________________________。
(3)在步骤④中加入的试剂Z应是________________;/p>
(4)在步骤⑤中发生反应的化学方程式是_____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某单烯烃与氢气的加成产物为(CH3)2CHCH2CH3,下列相关说法正确的是( )
A. 该产物的名称是1,1—二甲基丙烷
B. 原单烯烃只可能有3种不同结构
C. 1 mol加成产物燃烧消耗6.5 mol氧气
D. 原烯烃与分子式是C3H6的烃一定互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为周期表中短周期的一部分,W、X、Y、Z四种元素最外层电子数之和为24。下列说法正确的是
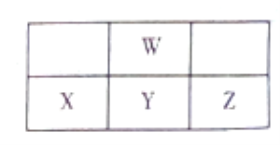
A. X、Y、Z的含氧酸的酸性依次增强
B. W元素形成的单核阴离子还原性强于X
C. Y、W形成的化合物一定能使酸性KMnO4溶液褪色
D. W与氢元素形成的化合物中可能含有非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有8种元素的性质、数据如下表所列,它们属于第二或第三周期。
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
原子半径(10-10m) | 0.74 | 1.60 | 1.86 | 1.10 | 0.99 | 1.52 | 0.75 | 1.43 |
最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
-2 | -3 | -1 | -3 |
回答下列问题:
(1)⑥的单质在空气中加热,生成物的电子式为_______________。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是___________。
(3)比较①和⑦的氢化物的稳定性(用化学式表示)_______________________________。
(4)写出实验室制备⑤的单质的离子方程式:________________________________。
(5)写出⑧的单质跟③的最高价氧化物的水化物的溶液反应的离子方程式:___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】老鼠能在含饱和多氟碳化物的溶液内部获得氧气,像鱼儿一样在水中游动,另有实验表示,把狗身上的70%的血液,换成由25%的多氟碳化物和75%的水混合成的乳液后仍可存活,科学家预测多氟碳化物可能成为血液的替代品.全氟丙烷(C3F8)是一种常见的多氟碳化物,下列对该物质的叙述中正确的是
A. 全氟丙烷的电子式为 B. 原子半径C比F的小
B. 原子半径C比F的小
C. 全氟丙烷分子中的化学键只有共价键 D. 全氟丙烷分子中碳链成直线型
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛酸钡(BaTiO3)在工业上有重要用途,主要用于制作电子陶瓷、PTC热敏电阻、电容器等多种电子元件。以下是生产钛酸钡的一种工艺流程图:
![]()
已知:①草酸氧化钛钡晶体的化学式为BaTiO(C2O4)2·4H2O;
(1)BaTiO3中Ti元素的化合价为:__________。
(2)用盐酸酸浸时发生反应的离子方程式为: ________________________________。
(3)流程中通过过滤得到草酸氧化钛钡晶体后,为提高产品质量需对晶体洗涤。
①过滤操作中使用的玻璃仪器有__________________________________________。
②如何证明晶体已洗净?_________________________________________。
(4)某兴趣小组取19.70gBaCO3模拟上述工艺流程制备BaTiO3,得产品13.98g,BaTiO3的产率为:________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com