
����Ŀ�����ᱵ(BaTiO3)�ڹ�ҵ������Ҫ��;����Ҫ�������������մɡ�PTC�������衢�������ȶ��ֵ���Ԫ�����������������ᱵ��һ�ֹ�������ͼ:
![]()
��֪:�ٲ��������ѱ�����Ļ�ѧʽΪBaTiO(C2O4)2��4H2O��
(1)BaTiO3��TiԪ�صĻ��ϼ�Ϊ:__________��
(2)���������ʱ������Ӧ�����ӷ���ʽΪ: ________________________________��
(3)������ͨ�����˵õ����������ѱ������Ϊ��߲�Ʒ������Ծ���ϴ�ӡ�
�ٹ��˲�����ʹ�õIJ���������__________________________________________��
�����֤��������ϴ��?_________________________________________��
(4)ij��ȤС��ȡ19.70gBaCO3ģ���������������Ʊ�BaTiO3���ò�Ʒ13.98g��BaTiO3�IJ���Ϊ:________��
���𰸡�+4 BaCO3 + 2H+ = Ba2+ + CO2 ��+ H2O©���� �ձ��� ������ȡ���һ��ϴ��Һ�������Թ��У� �μ�ϡ HNO3 �ữ�� AgNO3 ��Һ�� ���ް�ɫ���������� ˵����ϴ��60%
��������
̼�ᱵ�����ᷴӦ�����Ȼ�����Ȼ���Ȼ��������Ȼ�̼�����ᷴӦ����BaTiO��C2O4��2��4H2O��ͬʱ�õ�ΪHCl��HCl��ѭ�����ã��������ˡ�ϴ�ӡ�������յõ�BaTiO3��
(1)�ɻ��ϼ۴����͵���0��BaTiO3��TiԪ�صĻ��ϼ�Ϊx:2+x-3��2=0,x=+4��(2)���������ʱ̼�ᱵ�����ᷴӦ�����Ȼ�����������̼��ˮ��������Ӧ�����ӷ���ʽΪ:BaCO3 + 2H+ = Ba2+ + CO2 ��+ H2O ��(3)�ٹ��˲�����ʹ�õIJ���������©�����ձ�������������֤��������ϴ����ȡ���һ��ϴ��Һ�������Թ��У��μ�ϡHNO3 �ữ�� AgNO3 ��Һ�����ް�ɫ����������˵����ϴ����(4)��������۲����� BaTiO3 Ħ������ 233.192 g��mol-1 ��m(BaTiO3)= 233.192 g��mol-1��19.70g/197 g��mol-1=23.32g,�ò�Ʒ13.98g��BaTiO3�IJ���Ϊ:13.98g/23.32g��100%=60%.


 ͬ����ϰǿ����չϵ�д�
ͬ����ϰǿ����չϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����ͼ������ȼ�ϵ�ع���ʾ��ͼ��
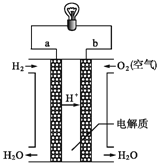
д������ȼ�ϵ�صĵ缫��Ӧʽ��
������______________________________��������__________________________________��
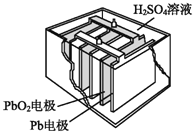
��2��������������Դ����Ǧ���ء���ṹ��ͼ��ʾ���ŵ�ʱ�ĵ�ط�Ӧ���£�PbO2+Pb+2H2SO4=2PbSO4+2H2O��д�������ĵ缫��Ӧʽ��_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1������Ԫ�����ڱ����Է�չ���ڰ����ڣ����ҵ������չ���ԭ�������ܼ����ڰ�����ӦΪ_____��Ԫ�ء�
��2����֪N-N��N=N��N��N����֮��Ϊ1.00:2.17:4.90,��C-C��C=C��C��C����֮��Ϊ1.00:1.77:2.34.�������Щ����������Ӳ��������ӳɷ�Ӧ����Ȳ�������ӳɷ�Ӧ?___
��3����ͼ�����־�����ͬ����ʽ���л�������ǻ�������Ͷ��ǻ�������Ľṹ��ʽ����֪���ķе����ܴ����ж��ǻ�������е�ϸߣ���δ�����ĽǶ������ͣ�_______
���ǻ������� ���ǻ�������
���ǻ�������
��4�����Ӿ�����ʳ�Σ��ܴ࣬��������ԭ�Ӿ�����ʯӢ��ͬ���ܴ࣬Ҳ��������Ȼ��ʳ�κ�ʯӢ��Ħ��Ӳ��ȴ����Ӧ��ν��ͣ�____________________________________
��5����ͼ�����ǽ����ơ�����п���⡢���ʯ������ʾ��ͼ��

i����ͼ�ĵ⾧���е���ӵ�������____�ֲ�ͬȡ����ƽ����_______��ԭ�ӡ�
ii������п������������Ϊ��a=266.49 pm��b=266.49 pm��c=494.68 pm����=90��,��=90�㣬��=120�㣬��þ����ĵ����Ϊ ___________cm2.����ֻ��ʽ�����㣩��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Է�������Ϊ M ����̬������V L����״����������m g ˮ�У� �õ���������Ϊ w�����ʵ���Ũ��Ϊc mol/L���ܶ�Ϊ��g/mL ����Һ������˵����ȷ���ǣ� ��
A. ��Һ�ܶ�![]() B. ���ʵ���Ũ��
B. ���ʵ���Ũ��![]()
C. ��Һ����������![]() D. ��Է�������
D. ��Է�������![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У���ȷ���ǣ� ��
A. 14C��� 14������
B. 1H��2H��3H��ͬһ�ֺ���
C. ��������Һ��c��H+����С���ɽ���Ϊǿ�������
D. ���ݷ�ɢ�ʿ�����С���ɽ���ɢϵ��Ϊ��Һ���������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ�������Դ����������ȡ�봢��������Դ����������о��ȵ㡣
��1����700��ʱ�����ݻ�Ϊ2L���ܱ������г���һ������CO��H2O��������Ӧ��CO(g)+H2O(g)![]() CO2(g)+H2(g)����Ӧ�����вⶨ�IJ������ݼ��±�������t2 > t1��:
CO2(g)+H2(g)����Ӧ�����вⶨ�IJ������ݼ��±�������t2 > t1��:
��Ӧʱ��/min | 0 | t1 | t2 |
n(CO)/mol | 1.20 | 0.80 | 0.80 |
�ٷ�Ӧ��t1min�ڵ�ƽ�����ʣ�v(H2)��____mol��L��1��min��1��
��t2ʱ�̣��÷�Ӧ������Ӧ����___�淴Ӧ���ʣ���������������С������������������
��2������ȼ�ϵ�ؿ���ʹ���ں���ɻ��ϣ��䷴Ӧԭ��ʾ��ͼ��ͼ��
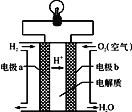
�ٸõ�ع���ʱ��____��ת��Ϊ____�ܡ�
��д���õ�ع���ʱ���ܷ�Ӧ����ʽ________��
�۵缫b�Ϸ���______��Ӧ����������������ԭ������
�������·�У����������ķ���Ϊ________��
��3��þ���Ͻ�Mg17Al10����һ��DZ�ڵ�������ϣ�������������£���һ����ѧ�����ȵ�Mg��Al������һ���¶���������á��úϽ���һ����������ȫ����ķ�Ӧ����ʽΪMg17Al10��17H2��17MgH2��10Al���õ��Ļ����Y��17MgH2��10Al����һ�������¿��ͷų�������
��þ���Ͻ���۵�Ƚ���þ���۵�______����������������������
����6.0 mol��L-1 HCl��Һ�У������Y����ȫ�ͷų�H2��1 mol Mg17Al10��ȫ�����õ��Ļ����Y����������������ȫ��Ӧ���ͷų�H2�����ʵ���Ϊ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й����ʵ�ת����ϵ��ͼ��ʾ������������ͷ�Ӧ��������ȥ����D��F��G��H��Ϊ�������壬����D��ʹʪ��ĺ�ɫʯ����ֽ������G�ʻ���ɫ��H�ڿ����к�����ߣ�C��Ħ������Ϊ32g��mol��1��EΪ�����Լ
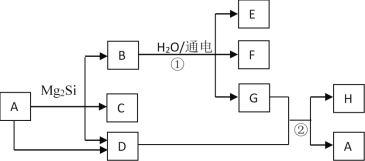
��1��C�Ļ�ѧʽΪ_________��
��2��A�ĵ���ʽΪ_________��
��3��д����Ӧ�ٵ����ӷ���ʽ_______________��
��4��д����Ӧ�ڵĻ�ѧ����ʽ________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NH3��һ����Ҫ�Ļ���ԭ�ϣ������Ʊ�һϵ������(����ͼ)������˵����ȷ���ǣ� ��

A. NH4Cl��NaHCO3���dz��õĻ���
B. NH4Cl��HNO3��Na2CO3����ʱ���ֽ�
C. NH3��NO2��һ�������¿ɷ���������ԭ��Ӧ
D. ͼ�����漰���������ʾ�����Ca(OH)2������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���Ũ����������У���ȷ����
A. Ũ���������ˮ�ԣ������ʹ����̿��
B. Ũ�����ڳ����¿�Ѹ����ͭƬ��Ӧ�ų�������������
C. Ũ������һ�ָ�������ܹ����ﰱ��������������
D. Ũ�����ڳ������ܹ�ʹ�������Ƚ����γ�����Ĥ���ۻ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com