
【题目】合成涤纶的流程图如下所示。
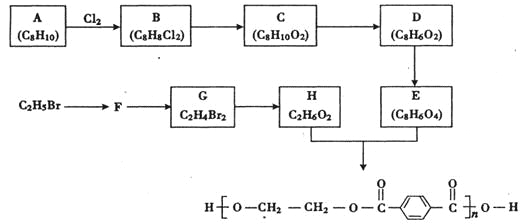
回答下列问题:
(1)A的名称为 ;
(2) F的结构简式是 ;
(3) C→D的反应类型是 ;F→G的反应类型为 ;
(4)E与H反应的化学方程式为 :
(5)E有多种同分异构体,符合下列条件的同分异构体有 种,其中在核磁共振氢谱中出现四组峰的是 (写出结构简式)。
①芳香族化合物;②红外光谱显示含有羧基;③能发生银镜反应;④能发生水解反应
(6) A也能一步转化生成E:![]() .试剂a可以用 溶液。
.试剂a可以用 溶液。
【答案】(15分)(1)对二甲苯(1分)(2)H2C=CH2(1分)(3)氧化反应(1分)加成反应(1分)
(4)![]()
![]()
(5)6(2分)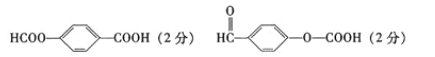
(6)酸性高锰酸钾溶液(2分)
【解析】
试题根据流程图可知,溴乙烷发生消去反应生成F,即F是乙烯。乙烯和单质溴发生加成反应生成G,即G是1,2-二溴乙烷,结构简式是CH2BrCH2Br。根据H的化学式可知,G生成H的反应是卤代烃的水解反应,即H是乙二醇,结构简式是HOCH2CH2OH。H和E发生反应生成高分子化合物,且该反应是缩聚反应,因此根据高分子化合物的结构简式可知,E应该是对苯二甲酸,结构简式是![]() 。D比E少2个氧原子,因此D生成E的反应是氧化反应,即D是对苯二甲醛,结构简式是
。D比E少2个氧原子,因此D生成E的反应是氧化反应,即D是对苯二甲醛,结构简式是![]() 。C比D多4个氢原子,因此C是对苯二甲醇,结构简式是
。C比D多4个氢原子,因此C是对苯二甲醇,结构简式是![]() 。B是卤代烃,生成C是水解反应,则B的结构简式是
。B是卤代烃,生成C是水解反应,则B的结构简式是![]() 。A和氯气反应生成B,则A是对二甲苯,结构简式是
。A和氯气反应生成B,则A是对二甲苯,结构简式是![]() 。
。
(1)根据以上分析可知,A的名称是对二甲苯。
(2)F是乙烯,其结构简式是H2C=CH2。
(3)根据以上分析可知,C→D的反应类型是氧化反应;F→G的反应类型为加成反应。
(4)E与H反应是缩聚反应,其化学方程式为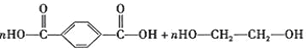
![]()
![]() 。
。
(5)①芳香族化合物,说明含有苯环;②红外光谱显示含有羧基;③能发生银镜反应,说明含有醛基;④能发生水解反应,说明还含有酯基。又因为在核磁共振氢谱中出现四组峰的是,说明2个取代基应该是对位的,则可能的结构简式是![]() 或
或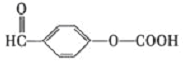 。
。
(6)对二甲苯要一步氧化生成对苯二甲酸,所以需要加入强氧化剂酸性高锰酸钾溶液。


 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为原子序数依次增大的四种短周期主族元素,A、B、C、D、E为上述四种元素中的两种或三种所组成的化合物,其中A、C、E为有机物。已知A的相对分子质量为28,B分子中含有18个电子,D分子中含有10个电子,五种化合物间的转化关系如下图所示。下列说法正确的是
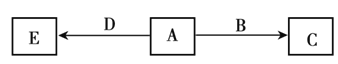
A.W是所在周期中原子半径最大的元素
B.Y的最高价氧化物的水化物为弱酸
C.X、Y、Z组成的分子中只含有极性键
D.X、Y组成的化合物的沸点一定比X、Z组成的化合物的沸点低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】保龄球与竹签可以用来制作有机分子球棍模型,保龄球代表有机分子中的原子,且保龄球个数和大小分别代表有机分子中的原子个数和类型;竹签代表有机分子中原子间结合的化学键,并以竹签的数目和类型代表化学键的数目和类型,下列关于用保龄球和竹签制作分子球棍模型的判断,正确的是( )
A. 甲烷的球棍模型需要用五个保龄球和五根竹签制作
B. 甲烷球棍模型中,较大的保龄球代表甲烷分子中的氢原子
C. 甲烷的球棍模型中,五个保龄球的球心不在同一平面上
D. 制作乙烯的模型时,需要用到六根完全相同的竹签
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室电解Na2SO4溶液的装置,下列叙述错误的是( )
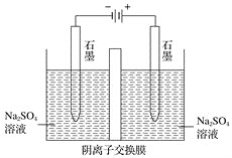
A.阴极:2H++2e-=H2↑,阳极:4OH--4e-=2H2O+O2↑
B.电解一段时间后,阴极区显碱性,阳极区显酸性
C.电解过程中,Na+、H+向阴极定向移动,SO42-、OH-向阳极定向移动
D.电解后,撤掉阴离子交换膜充分混合,Na2SO4溶液的浓度比电解前增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是生产生活中的常见有机物的分子式、结构式、结构简式或名称有关说法正确的是
①![]() ②
②![]() ③
③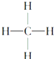 ④
④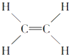 ⑤CH3CH2OH
⑤CH3CH2OH
⑥C6H12O6⑦CH3COOH ⑧硬脂酸甘油酯 ⑨蛋白质 ⑩聚乙烯
A. 能跟溴的四氯化碳溶液发生加成反应并使之褪色的有①②④⑩
B. 投入钠能产生H2的是⑤⑦⑧⑨
C. 属于高分子材料的是⑧⑨⑩
D. 含碳量最高、有毒、常温下为液体且点燃时有浓烟的是①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH=2的A、B两种酸溶液各1mL,分别加水稀释到1000mL,其溶液的pH与体积(V)的关系如图所示,则下列说法正确的是( )
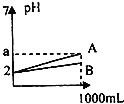
A.A、B两种酸溶液物质的量浓度一定相等
B.若a=5,则A是强酸,B是弱酸
C.稀释后A酸溶液的酸性比B酸溶液强
D.若a<5,则A.B都是弱酸且A的酸性>B
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学模拟工业上用离子交换膜法制烧碱的方法,可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。
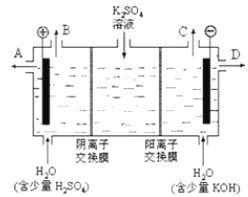
(1)该电解槽的阳极反应为________________________,此时通过阴离子交换膜的离子数________(填“大于”、“小于”或“等于”)通过阳离子交换膜的离子数。
(2) 制得的氢氧化钾溶液从出口________(填写“A”、“B”、“C”、“D”)导出,制得的氧气从出口________ (填写“A”、“B”、“C”、“D”)导出。
(3)通电开始后,阴极附近溶液pH会增大,请简述原因_______________________________ 。
(4)若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,则电池正极的电极反应为___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米磷化钻常用于制作特种钻玻璃,制备磷化钻的常用流程如图:
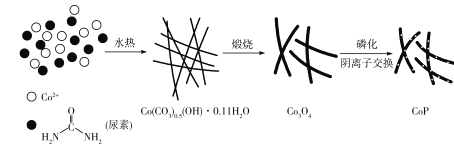
(1)基态P原子的电子排布式为___。P在元素周期表中位于___区。
(2)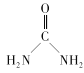 中碳原子的杂化类型是___C、N、O三种元素的第一电离能由大到小的顺序是___(用元素符号表示),电负性由大到小的顺序为___。
中碳原子的杂化类型是___C、N、O三种元素的第一电离能由大到小的顺序是___(用元素符号表示),电负性由大到小的顺序为___。
(3)CO32-中C的价层电子对数为___,其空间构型为___。
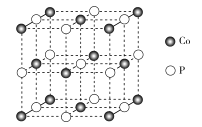
(4)磷化钴的晶胞结构如图所示,最近且相邻两个钴原子的距离为n pm。设NA为阿伏加德罗常数的值, 则其晶胞密度为___g.cm-3(列出计算式即可)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com