
【题目】在一定体积的密闭容器中,进行如下化学反应:
CO(g)+H2O(g) ![]() CO2(g)+H2(g),其化学平衡常数K和温度t的关系如表:
CO2(g)+H2(g),其化学平衡常数K和温度t的关系如表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K= , 该反应为反应(选填“吸热”、“放热”).
(2)能判断该反应是否达到化学平衡状态的依据是;
A.容器中压强不变
B.混合气体中c(CO)不变
C.v逆(H2)=v正(H2O)
D.c(CO2)=c(CO)
(3)830℃时,容器中的反应已达到平衡.在其他条件不变的情况下,在此温度下,若该容器中含有1molCO2、1.2molH2、0.75molCO、1.5molH2O,这状态(是或否)处于平衡状态?若不是,反应向哪个方向进行? . (选填“向正反应方向”、“向逆反应方向”).
(4)若830℃时,向容器中充入lmolCO、5molH2O,反应达到平衡后,CO的转化率为 .
【答案】
(1)![]() ;放热
;放热
(2)BC
(3)否;向逆反应方向
(4)83.3%(或83%,或5/6)
【解析】解:(1)化学平衡常数K等于生成物浓度幂之积与反应物浓度幂之积的比,但不包含固体和纯液体,所以该反应化学平衡常数K= ![]() ;升高温度平衡向吸热方向移动,根据表中数据知,升高温度化学平衡常数减小,说明平衡逆向移动,则正反应是放热反应,
;升高温度平衡向吸热方向移动,根据表中数据知,升高温度化学平衡常数减小,说明平衡逆向移动,则正反应是放热反应,
所以答案是: ![]() ;放热;(2)A.该反应前后气体物质的量不变,所以反应是否达到平衡状态容器中压强都不变,所以不能判断平衡状态,故错误;
;放热;(2)A.该反应前后气体物质的量不变,所以反应是否达到平衡状态容器中压强都不变,所以不能判断平衡状态,故错误;
B.混合气体中c(CO)不变时,正逆反应速率相等,反应达到平衡状态,故正确;
C.v逆(H2)=v正(H2O)=v正(H2),正逆反应速率相等,反应达到平衡状态,故正确;
D.c(CO2)=c(CO)时该反应可能达到平衡状态也可能没有达到平衡状态,与反应物初始量及转化率有关,所以不能判断平衡状态,故错误;
故选BC;(3)因为该反应中各气体计量数都是1,所以化学平衡常数也等于生成物物质的量之积与反应物物质的量之积的比,830℃时,化学平衡常数K=1.0,若该容器中含有1molCO2、1.2molH2、0.75molCO、1.5molH2O,该体系中浓度商= ![]() =1.07>1,该反应没有达到平衡状态,要使反应达到平衡状态,应该向逆反应方向移动,
=1.07>1,该反应没有达到平衡状态,要使反应达到平衡状态,应该向逆反应方向移动,
所以答案是:否;向逆反应方向;(4)该温度下化学平衡常数K为1.0,设参加反应的n(CO)=xmol,根据方程式知,参加反应的n(H2O)=n(H2)=n(CO2)=n(CO)=xmol,K= ![]() ,x=
,x= ![]() ,
,
转化率= ![]() ×100%=
×100%= ![]() =.83.3%(或83%,或5/6),
=.83.3%(或83%,或5/6),
所以答案是:83.3%(或83%,或5/6).
【考点精析】根据题目的已知条件,利用化学平衡状态本质及特征和化学平衡的计算的相关知识可以得到问题的答案,需要掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效);反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%.


科目:高中化学 来源: 题型:
【题目】有关药品的保存和使用不正确的是( )
A.溴水盛于带磨砂玻璃塞的细口瓶中
B.硫酸铜粉末、氯化钙等药品贮存于干燥器中
C.白磷需浸入水中密封保存
D.用碳酸钠滴定盐酸时,Na2CO3液应盛于酸式滴定管中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于电解NaCl水溶液的说法正确的是 ( )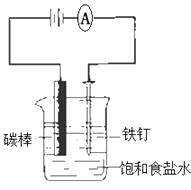
①电解产物为Cl2和Na
②电解过程中,碳棒一极产生黄绿色气体
③电解一段时间后,在碳棒附近的溶液中滴加酚酞溶液,溶液呈红色
④电解一段时间后,在铁钉附近的溶液中滴加酚酞溶液,溶液呈红色
A.①③
B.①④
C.②③
D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高氯酸是一种酸性极强的无机含氧酸,可用于制备高氯酸盐、人造金刚石提纯等方面.
查阅资料得到以下有关高氯酸的信息:
名称 | 分子式 | 外观 | 沸点 |
高氯酸 | HClO4 | 无色液体 | 130℃ |
工业上生产高氯酸的同时还生产了亚氯酸钠,工业流程如图:
(1)操作①的名称是 .
(2)Ca(ClO)2、ClO2、NaClO、NaClO2等含氯化合物都是常用的消毒剂和漂白剂是因为它们都具有
(3)反应器Ⅰ中投料时需加入过量浓硫酸,请简述目的 .
(4)反应器Ⅱ中发生反应的离子方程式为 .
(5)某学习小组模拟工业流程图中的蒸馏过程,有液体流出时立即收集产品以获得HClO4纯品.请评价这一操作是否合理并说明理由 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按照物质的组成和性质进行分类,HNO3应属于( )
①酸 ②氧化物 ③无氧酸 ④有氧酸 ⑤化合物 ⑥混合物 ⑦纯净物 ⑧一元酸
A. ①④⑤⑦⑧ B. ②③④⑤ C. ③④⑤⑦ D. ②⑤⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知化学反应A2(g)+B2(g)═2AB(g)的能量变化如图所示,判断下列叙述中正确的是( ) 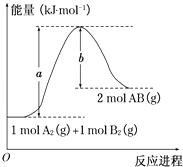
A.每生成2分子AB吸收b kJ热量
B.该反应热△H=+(a﹣b)kJmol﹣1
C.该反应中反应物的总能量高于生成物的总能量
D.断裂1 mol A﹣A和1 mol B﹣B键,放出a kJ能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有含少量NaCl、Na2SO4、Na2CO3等杂质的NaNO3溶液,用适当的试剂除去杂质,得到纯净的NaNO3固体的实验流程如图所示。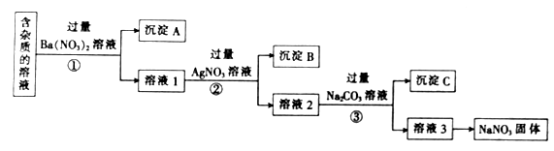
(1)沉淀A的主要成分是(填化学式)。
(2)②中反应的化学方程式是。
(3)①②③中均进行的分离操作是。
(4)实验室用上述实验获得的NaNO3固体配制480 mL 0.40 mol.L-1NaNO3溶液。
①配制溶液前要先计算,需称取NaNO3固体g。
②某同学转移溶液的操作如图所示,图中仪器的名称是烧杯和,该同学操作中的错误是。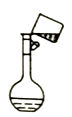
③若用胶头滴管定容时,不小心加水超过了刻度线,则应该采取的处理方法是。
④下列操作中,可能造成所配制溶液的浓度偏低的是(填字母)。
a.没有洗涤烧杯和玻璃棒
b.定容时,俯视刻度线
c.洗涤后的容量瓶中残留少量蒸馏水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸橙花酯是一种食用香料,其结构简式如图,关于该有机物的叙述中不正确的是( ) 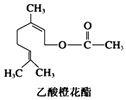
A.分子式为C12H20O2
B.1 mol该有机物水解时只能消耗1 mol NaOH
C.1mol该有机物可消耗3molH2
D.不能发生银镜反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com