
【题目】某化学研究小组设计如下图装置制备纯净的氯化铁。

资料:
①氯化铁遇水能发生剧烈反应生成Fe(OH)3;
②CCl4难溶于水,密度大于水,且Cl2在CCl4中的溶解度远大于水中的溶解度。
回答下列问题:
(1)试剂X的作用是__________________,试剂Y是__________________。
(2)实验过程中,A、E两处有酒精灯,应先点燃___________(填“A”或“E”)处;实验完毕后,关闭旋塞K,熄灭酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是______________,B的作用是______________________。
(3)用量简量取20mLG中溶液。倒入密封性良好的分液漏斗中,然后再注入10mL CCl4,盖好玻璃塞,振荡、静置、分液,分别取上层液、下层液滴在有色布条上,能使有色布条褪色的是__________(填“上层液”或“下层液”)。
(4)写出装置A中反应的离子方程式:_____________________________。实验结束后,测得装置E中的铁丝网质量增加mg,则理论上装置A中反应转移电子的物质的量为_________mol(用含m的式子回答)。
(5)有同学认为上述装置存在不足,用该装置制取的氯化铁中还含有其他杂质(不考虑铁),建议进行改进,请提出你的改进办法_____________________________。
【答案】 除去氯气中的HCl杂质 浓硫酸 A 瓶中液面下降,长颈漏斗内液面上升 贮存少量Cl2,避免Cl2污染环境 下层液 MnO2+ 4H++ 2Cl-![]() Mn2+ +Cl2↑+2H2O
Mn2+ +Cl2↑+2H2O ![]() 在F与G之间连接一个盛有浓硫酸的洗气瓶
在F与G之间连接一个盛有浓硫酸的洗气瓶
【解析】该实验的目的是制备纯净的氯化铁,由于氯化铁遇水能发生剧烈反应生成Fe(OH)3,所以该实验成功的关键是反应装置绝对干燥。观察装置,A装置产生Cl2,通过浓盐酸和二氧化锰加热制得的氯气中还有HCl气体和水蒸气,则Cl2进入E装置前应把这些杂质除去,所以C装置的目的是除去Cl2中的HCl,D装置的目的是除去Cl2中的水蒸气,纯净的Cl2进入E装置与铁在加热条件下反应生成氯化铁,多余的Cl2进入F装置,最后通入水中,进行尾气处理。
(1)A装置产生的Cl2中还有HCl气体和水蒸气杂质,则Cl2进入E装置前应把这些杂质除去,所以试剂X的目的是除去Cl2中的HCl,试剂Y的目的是除去Cl2中的水蒸气,试剂Y则为浓硫酸。
(2)实验过程中,A、E两处有酒精灯,应先点燃A,先产生Cl2,使Cl2充满整个装置;实验完毕后,关闭旋塞K,熄灭酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时Cl2进入B中,在饱和食盐水中溶解度很小,B瓶内压强增大,产生的现象是瓶中液面下降,长颈漏斗内液面上升;则B的作用是储存少量Cl2,避免Cl2污染环境;
(3)用量简量取20mLG中溶液,G中的溶液为氯水,注入10mL CCl4,盖好玻璃塞,振荡、静置、分液,因为CCl4难溶于水,密度大于水,且Cl2在CCl4中的溶解度远大于水中的溶解度。所以得到的上层液为水,下层是Cl2的CCl4中的溶液。分别取上层液、下层液滴在有色布条上,能使有色布条褪色的是下层液;
(4)装置A中反应的离子方程式:MnO2+ 4H++ 2Cl-![]() Mn2+ +Cl2↑+2H2O ;实验结束后,测得装置E中的铁丝网质量增加mg,增重即为Cl的质量,n(Cl)=
Mn2+ +Cl2↑+2H2O ;实验结束后,测得装置E中的铁丝网质量增加mg,增重即为Cl的质量,n(Cl)= ![]() ,氯由0价降到-1价,故转移电子的物质的量为
,氯由0价降到-1价,故转移电子的物质的量为![]()
(5)该实验成功的关键是反应装置绝对干燥,所以该装置的不足是E装置右边没有干燥装置,所以改进办法是在F与G之间连接一个盛有浓硫酸的洗气瓶。


科目:高中化学 来源: 题型:
【题目】某研究性学习小组对过量炭粉与氧化铁反应的气体产物成分进行研究.
(1)提出假设 ①该反应的气体产物是CO2 .
②该反应的气体产物是CO.
③该反应的气体产物是 .
(2)设计方案如图所示,将一定量的氧化铁在隔绝空气的条件下与过量炭粉完全反应,测定参加反应的碳元素与氧元素的质量比.
查阅资料
氮气不与碳、氧化铁发生反应.实验室可以用氯化铵饱和溶液和亚硝酸钠(NaNO2)饱和溶液混合加热反应制得氮气.请写出该反应的离子方程式: .
(3)实验步骤①按图连接装置,并检查装置的气密性,称取3.20g氧化铁、2.00g碳粉混合均匀,放入48.48g的硬质玻璃管中;
②加热前,先通一段时间纯净干燥的氮气;
③停止通入N2后,夹紧弹簧夹,加热一段时间,澄清石灰水(足量)变浑浊;
④待反应结束,再缓缓通入一段时间的氮气.冷却至室温,称得硬质玻璃管和固体总质量为52.24g;
⑤过滤出石灰水中的沉淀,洗涤、烘干后称得质量为2.00g.
步骤②、④中都分别通入N2 , 其作用分别为 .
(4)数据处理试根据实验数据分析,写出该实验中氧化铁与碳发生反应的化学方程式: .
(5)实验优化 学习小组有同学认为应对实验装置进一步完善.①甲同学认为:应将澄清石灰水换成Ba(OH)2溶液,其理由是 .
②从环境保护的角度,请你再提出一个优化方案将此实验装置进一步完善: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不能用胶体的知识解释的现象是( )
A. 向FeCl3溶液中加入NaOH溶液,出现红褐色沉淀
B. 石膏点豆腐
C. 一支钢笔使用两种不同牌号的墨水,易出现堵塞
D. 江河入海处,易形成沙洲
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A的相对分子质量184.5,其结构如图1所示,(﹣R﹣代表某种烷基),A在一定条件下还有如图2所示的反应关系,D不能发生银镜反应.
(1)C中含有的官能团为 , E→F的反应类型为;
(2)写出A的结构简式;
(3)写出C→E的化学方程式;
(4)H的同分异构体很多,其中属于酯类,含苯环,且水解产物中含有乙酸的同分异构体有种
(5)G显酸性,M(B),M(G)分别表示B、G的相对分子质量,试求:M(G)﹣M(B)= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生活与生产都离不开化学,下列说法不正确的是( )
A.用碳酸钠溶液可以洗涤油污
B.用pH试纸可以测定土壤的酸碱性
C.用明矾可以对自来水杀菌病毒
D.含氟牙膏可以有效防止龋齿
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中药在世界医学界越来越受到关注.中药药剂砒霜(主要成分As2O3)可用于治疗急性白血病,为此,砷及其化合物的提取再次引起关注.
(1)As的原子结构示意图为 ![]() ,则其在周期表中的位置是 .
,则其在周期表中的位置是 .
(2)N元素非金属性比As强,下列说法正确的是 . ①NH3的热稳定性比AsH3差
②HNO3的酸性比H3AsO4强
③N的原子半径比As的原子半径小
(3)根据如图写出As2O5分解为As2O3的热化学方程式 . 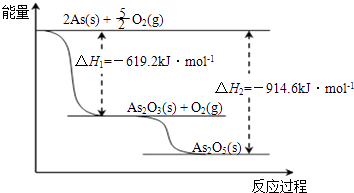
(4)查文献得知,可以从硫化砷(As2S3)废渣中提取As2O3 , 提取的工艺流程简图如下: 
①As2S3、Na3AsS3中的S均为﹣2价,碱浸过程中发生的反应(填“是”或“不是”)氧化还原反应.
②过程Ⅲ的系列操作包括 .
③写出过程Ⅲ的离子方程式 ,
过程Ⅲ中,酸性越强,As2O3的产率越高,请解释其原因 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com