
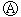 为
为 直流电源,
直流电源,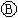 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸,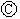 为电镀槽.接通电路后发现
为电镀槽.接通电路后发现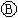 上的c点显红色.为实现铁上镀铜,接通
上的c点显红色.为实现铁上镀铜,接通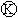 后,使c、d两点短路.
后,使c、d两点短路.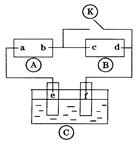
| A.a为直流电源的负极 |
| B.c极发生的反应为O2+4e-+2H2O=4OH- |
| C.f电极为铁板 |
| D.电解质溶液不能用CuCl2溶液 |
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案科目:高中化学 来源:不详 题型:单选题
| A.若电键K与N连接,铁被保护不会腐蚀 |
| B.若电键K与N连接,正极反应式是4OH- -4e-=2H2O+O2↑ |
| C.若电键K与M连接,将石墨棒换成铜棒,铁棒上立即有铜生成 |
| D.若电键K与M连接,当两极共产生22.4 L(标准状况)气体时,生成了1 molNaOH |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 资源。试回答下列问题:
资源。试回答下列问题: 和 三种溶液。
和 三种溶液。 将海水变成蒸汽,蒸汽经过冷却而得高纯度淡水,由此可判断蒸馏法是 (填“物理变化”、
将海水变成蒸汽,蒸汽经过冷却而得高纯度淡水,由此可判断蒸馏法是 (填“物理变化”、 “化学变化”),蒸馏法所用的主要玻璃仪器有________________________(写三种)。
“化学变化”),蒸馏法所用的主要玻璃仪器有________________________(写三种)。 NaOH+H2+Cl2(未配平)。利用电解所得气体制36.5%的浓盐酸100t,最少需要消耗食盐 t 。
NaOH+H2+Cl2(未配平)。利用电解所得气体制36.5%的浓盐酸100t,最少需要消耗食盐 t 。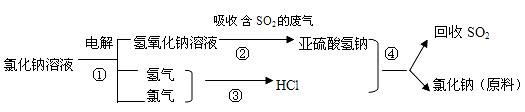
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用铜片连接电源的正极,另一电极用铂片 |
| B.用碳棒连接电源的正极,另一电极用铜片 |
| C.用氢氧化钠溶液吸收阴极产物 |
| D.用带火星的木条检验阳极产物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题


查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电解过程中有0.02mol电子转移 |
| B.阳极产物只有氯气 |
| C.在标准状况下,阳极产生的气体体积为0.448L |
| D.电解后溶液的pH =12 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电解过程中,阴阳两极产生的气体体积相同(同温同压时) |
| B.电解后的溶液中c(NaOH)=1mol/L |
| C.电解过程中,转移电子的物质的量约为8mol |
| D.原溶液中含有117g NaCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com