
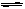 Ca2+(aq)+2OH-(aq),Ksp=4.7×10-6 mol3/L3,下列措施可使Ksp增大的是( )
Ca2+(aq)+2OH-(aq),Ksp=4.7×10-6 mol3/L3,下列措施可使Ksp增大的是( )| A.升高温度 | B.降低温度 |
| C.加入适量CaO固体 | D.加入适量Na2CO3固体 |
科目:高中化学 来源:不详 题型:单选题
| A.同温度下,CuS的溶解度大于FeS的溶解度 |
| B.同温度下,向饱和FeS溶液中加入少量Na2S固体后,Ksp(FeS)变小 |
| C.向含有等物质的量的FeCl2和CuCl2的混合溶液中逐滴加入Na2S溶液,最先出现的沉淀是FeS |
| D.除去工业废水中的Cu2+,可以选用FeS做沉淀剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
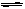 Ba2+(aq)+2OH-(aq)。向此种悬浊液中加入少量的氢氧化钡粉末,下列叙述正确的是 ( )
Ba2+(aq)+2OH-(aq)。向此种悬浊液中加入少量的氢氧化钡粉末,下列叙述正确的是 ( )| A.溶液中钡离子数减小 | B.溶液中C(Ba2+)减小 |
| C.溶液中C(OH-)增大 | D.PH减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1.0mol·L-1 Na2CO3 | B.加入2.0mol·L-1 NaOH |
| C.0.10mol·L-1CaCl2 | D.降低溶液的PH值 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.AgCl在饱和NaCl溶液中的KSP比在纯水中的KSP小 |
| B.向AgCl的悬浊液中加入NaBr溶液,白色沉淀转化为淡黄色,说明KSP(AgCl)<KSP(AgBr) |
| C.将0.001mol?L-1 AgNO3溶液滴入0.001mol?L-1 KCl和0.001mol?L-1 K2CrO4混合溶液中,先产生Ag2CrO4沉淀 |
| D.向AgCl的悬浊液中滴加浓氨水,沉淀溶解,说明AgCl的溶解平衡向右移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.难溶电解质在溶液中存在沉淀溶解平衡,且是一种动态平衡 |
| B.Ksp只与难溶电解质的性质与温度有关,而与沉淀的量和溶液中离子的浓度无关 |
| C.Ksp反映了物质在水中的溶解能力,可直接根据Ksp的大小比较电解质在水中溶解能力的大小 |
| D.可通过Q和Ksp的相对大小,来判断沉淀溶解平衡的移动方向 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com