
【题目】用50 mL 0.5 mol/L的盐酸与50 mL 0.5 mol/L的NaOH 溶液在下图所示的装置中进行中和热测定实验,下列说法不正确的是
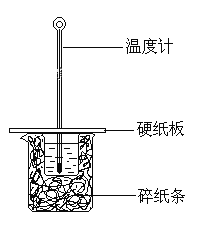
A.图中实验装置缺少环形玻璃搅拌棒,烧杯间填满碎纸条的主要作用是固定小烧杯
B.稀溶液中:H+ (aq) + OH— (aq) = H2O (l) ΔH=-57.3kJ·mol-1 ,若将含0.5 mol H2SO4的稀溶液与含1 mol NaOH的稀溶液混合,放出的热量为57.3kJ
C.进行中和热测定实验时,需要测出反应前盐酸和NaOH溶液的温度及反应后溶液的最高温度
D.若改用55 mL 0.50 mol/L的盐酸跟50 mL0.5 mol/L的NaOH溶液进行实验,从理论上说所求中和热相等。
【答案】A
【解析】
A. 根据图示结构可知图中实验装置缺少环形玻璃搅拌棒,烧杯间填满碎纸条的主要作用是保温,减少热量的散失,故A错误;
B. 稀溶液中:H+ (aq) + OH— (aq) = H2O (l) ΔH=-57.3kJ·mol-1 ,0.5 mol H2SO4的稀溶液中含有1molH+,1 mol NaOH的稀溶液中含有1molOH-,恰好完全反应生成1molH2O,放出的热量为57.3kJ,故B正确;
C. 进行中和热测定实验时,通过温度差及比热容可以计算出反应放出的热量,故C正确;
D. 若改用55 mL 0.50 mol/L的盐酸跟50 mL0.5 mol/L的NaOH溶液进行实验,过量的盐酸不参加反应,从理论上说所求中和热不变,故D正确;
故选A。


科目:高中化学 来源: 题型:
【题目】将2 mol N2(g)和1 mol H2(g)置于2L密闭容器中,在一定温度下发生反应:N2(g)+3H2(g)![]() 2NH3(g) H<0,其他条件不变时,改变某一条件对上述反应的影响,得出下列关系图:
2NH3(g) H<0,其他条件不变时,改变某一条件对上述反应的影响,得出下列关系图:


下列说法正确的是
A.图Ⅰ研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高
B.图Ⅱ研究的是压强对反应的影响,且乙的压强较高
C.图Ⅱ研究的是温度对反应的影响,且乙的温度较高
D.图Ⅲ研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+3B(g) ![]() 2C(g)+2D(g)在四种不同情况下的反应速率分别为
2C(g)+2D(g)在四种不同情况下的反应速率分别为
①v(A)=0.45 mol·L-1·min-1 ②v(B)=0.6 mol·L-1·s-1 ③v(C)=0.4 mol·L-1·s-1 ④v(D)=0.45 mol·L-1·s-1,该反应进行的快慢顺序为
A. ④>③=②>① B. ④<③=②<① C. ①>②>③>④ D. ④>③>②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数,下列说法正确的是( )
A. 标准状况下,11.2L的己烷所含的分子数为0.5NA
B. 28g乙烯所含共用电子对数目为4NA
C. 1mol羟基所含电子数为7 NA
D. 现有乙烯、丙烯的混合气体共14g,其原子数为3 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结晶玫瑰是具有玫瑰香气的香料,可由下列方法合成(部分反应物及反应条件未标出)

已知: ![]() (-R表示烃基)
(-R表示烃基)
(1)A是苯的一种同系物,相同条件下,其蒸气对氢气的相对密度是46,则A的名称是__________。
(2)反应②所需药品及反应条件是_________________。
(3)C的核磁共振氢谱峰面积之比是_________。
(4)C有多种同分异构体,其中属于芳香族化合物的有________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们利用原电池原理制作了多种电池,以满足日常生活、生产和科学技术等方面的需要。请根据题中提供的信息,回答下列问题。
(1)铅蓄电池在放电时的电池反应为Pb+PbO2+2H2SO4==2PbSO4+2H2O,则其正极上的电极反应为___________。
(2)FeCl3溶液腐蚀印刷电路铜板时发生反应:2FeCl3+Cu==2FeCl2+ CuCl2。若将此反应设计成原电池,则负极所用的电极材料为_____;电极反应式:_________。
(3)用Fe做阳极,KOH溶液做电解质溶液,进行电解,在阳极得到FeO![]() ,写出阳极的电极反应式____________________________________
,写出阳极的电极反应式____________________________________
(4)已知甲醇燃料电池的工作原理如下图所示。该电池工作时,b口通入的物质为_____,该电池正极上的电极反应式为 _______________;当6.4g甲醇(CH3OH)完全反应生成CO2时,有____mol电子发生转移。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数用![]() 表示,下列叙述正确的是
表示,下列叙述正确的是![]()
①![]() 含有电子数为
含有电子数为![]()
②![]() 中含有的
中含有的![]() 键总数目为
键总数目为![]()
③![]()
![]() 与
与![]() 完全反应时转移电子数为
完全反应时转移电子数为![]()
④![]() 硅晶体中含有
硅晶体中含有![]() 个
个![]() 键
键
⑤![]() 通入足量氢氧化钠溶液中充分反应,转移的电子数等于
通入足量氢氧化钠溶液中充分反应,转移的电子数等于![]()
⑥![]() ,
,![]()
![]() 溶液中,
溶液中,![]() 和
和![]() 离子数的总和是
离子数的总和是![]()
⑦在常温常压下,![]() 铁与
铁与![]()
![]() 充分反应,转移的电子数为
充分反应,转移的电子数为![]()
⑧![]() 和
和![]() 的混合物共
的混合物共![]() ,其中所含原子数一定为
,其中所含原子数一定为![]() .
.
A.①②③⑤⑧B.②④⑥⑦⑧C.①③⑤⑥⑦D.①②④⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Mn和Bi形成的晶体薄膜是一种金属间化合物![]() 晶胞结构如图
晶胞结构如图![]() ,有关说法正确的( )
,有关说法正确的( )
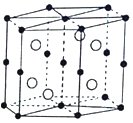
A.锰价电子排布为![]()
B.Bi是d区金属
C.该合金堆积方式是简单立方
D.该晶体的化学式为MnBi
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A.元素的第一电离能越大,其金属性越强
B.原子核外的 M层上的 s能级和 p能级都填满了电子,而 d轨道上尚未排有电子的两种原子,其对应元素不一定位于同一周期
C.元素电负性越大的原子,失电子能力越强
D.金属单质跟酸反应的难易,只跟该金属元素的第一电离能有关
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com