
【题目】某物质(X)是有机合成中重要中间体,下列关于它的说法正确的是( )
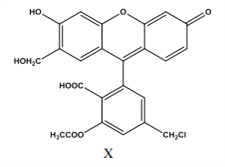
A. 1 mol X 与与足量的 NaOH 溶液反应, 最多消耗 6mol NaOH
B. 1 mol X 最多能与 10mol 氢气反应,且生成物中无手性碳原子
C. 1mol X 与足量的浓溴水反应,最多消耗 2mol Br2
D. X 分子式为 C24H17O8Cl,是芳香族化合物
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】如图所示是298 K时,N2与H2反应过程中能量变化的曲线图,下列叙述正确的是

A. 该反应的热化学方程式为:N2+3H2![]() 2NH3 △H=-92 kJ/mol
2NH3 △H=-92 kJ/mol
B. a曲线是加入催化剂时的能量变化曲线
C. 加入催化剂,该化学反应的反应热不改变
D. 在温度、体积一定的条件下,通入1 mol N2和3 mol H2反应后放出的热量为92kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于合金性质的说法中,错误的是( )
A. 合金的硬度一般比其各成分金属的硬度高
B. 合金的熔点一般比其各成分金属的熔点低
C. 合金的物理性质一般与其各成分金属的的物理性质不同
D. 合金的化学性质一般与其各成分金属的的化学性质不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烯烃在一定条件下发生氧化反应,碳碳双键断裂,如:R1CH═CHR2,被氧化为![]() 和
和![]() ;
; 被氧化为
被氧化为 和
和 ,由此推断分子式为C5H10的烯烃的氧化产物有( )
,由此推断分子式为C5H10的烯烃的氧化产物有( )
A.5种 B.6种 C.7种 D.8种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列条件一定能使反应速率加快的是:①增加反应物的物质的量 ②升高温度 ③缩小反应容器的体积 ④加入生成物 ⑤加入催化剂( )
A. 全部 B. ①②⑤ C. ② D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C三种不含结晶水的固体物质的溶解度曲线如图,下列说法中不正确的是

A. t1℃时,A的饱和溶液65 g中含有溶剂50 g
B. 将t1℃ A、B、C三种物质的饱和溶液升温至t2℃ 时,溶液中溶质的质量分数是A=B>C
C. A中含少量C时可用降温结晶法提纯A
D. 25%的A溶液降温至t1℃时会有晶体析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲酸乙酯(C9H10O2)稍有水果气味,用于配制香水香精和人造精油,大量用于食品工业中,也可用作有机合成中间体、溶剂等。其制备方法为: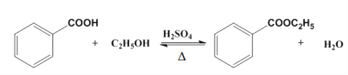
已知:
颜色、状态 | 沸点(℃) | 密度(g·cm-3) | 相对分子质量 | |
苯甲酸* | 白色片状晶体 | 249 | 1.2659 | 122 |
苯甲酸乙酯 | 无色澄清液体 | 212.6 | 1.05 | 150 |
乙醇 | 无色澄清液体 | 78.3 | 0.7893 | 46 |
环己烷 | 无色澄清液体 | 80.8 | 0.7318 | 84 |
*苯甲酸在 100℃会迅速升华。
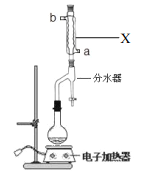
实验步骤如下:
①在 100mL 圆底烧瓶中加入 12.20g 苯甲酸、25mL乙醇(过量)、20mL 环己烷,以及 4mL浓硫酸,混合均匀并加入沸石,按右图所示装好仪器,并在分水器中预先加入水,使水面略低于分水器的支管口,控制温度在 65~70℃加热回流 2h。反应时环己烷-乙醇-水会形成“共沸物”(沸点62.6℃)蒸馏出来。在反应过程中,通过分水器下部的旋塞分出生成的水,注意保持分水器中水层液面原来的高度,使油层尽量回到圆底烧瓶中。
②反应结束,打开旋塞放出分水器中液体后,关闭旋塞。继续加热,至分水器中收集到的液体不再明显增加,停止加热。
③将烧瓶内反应液倒入盛有适量水的烧杯中,分批加入Na2CO3至溶液呈中性。
④用分液漏斗分出有机层,水层用 25mL 乙醚萃取分液,然后合并至有机层。加入氯化钙,对粗产物进行蒸馏,低温蒸出乙醚后,继续升温,接收 210—213℃的馏分。
⑤检验合格,测得产品体积为 11.43mL。
回答下列问题:
(1)装置 X 的作用是_________;进水口为_________(a或者b)。
(2)步骤①中使用分水器不断分离除去水的目的是_________。
(3)步骤②中应控制馏分的温度在_________。
A.65~70℃ B.78~80℃ C.85~90℃ D.215~220℃
(4)若 Na2CO3加入不足,在步骤④蒸馏时,蒸馏烧瓶中可见到白烟生成,产生该现象的原因是_________。
(5)该实验的产率为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 用系统命名法命名有机物![]() 和
和 ,主链碳原子数均为7个
,主链碳原子数均为7个
B. 某烃的分子式为C10H14,它不能使溴水褪色,但可使酸性KMnO4溶液褪色,且分子结构中只有一个烷基,符合条件的烃有4种
C. 碳原子数小于或等于8的单烯烃中,与HBr加成产物只有一种结构,符合条件的单烯烃有6种
D. 经测定C3H7OH和C6H12组成的混合物中氧的质量分数为8%,则此混合物中碳的质量分数是78%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组设计出如图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化。

(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c,其目的是_____________________。
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2 mL浓硝酸,c中反应的化学方程式是______________________________________________。
(3)下表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是____________。
方案 | 反应物 |
甲 | Cu、浓HNO3 |
乙 | Cu、稀HNO3 |
丙 | Cu、O2、稀HNO3 |
(4)该小组还用上述装置进行实验证明酸性:HCl>H2CO3>H2SiO3,则分液漏斗a中加入的试剂是____________,c中加入的试剂是____________,d中加入的试剂是____________,实验现象为____________________________________________。有同学认为,该实验装置仍不能证明上述结论,改进的措施是_________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com