
����Ŀ����һ�������ȵĹ̶��ݻ����ܱ������У��������淴ӦmA(g)+nB(g)![]() pC(g)+qD(g)����m��n��p��qΪ������������Ϊ�㣩ʱ����Ӧ�ﵽƽ��ı�־��
pC(g)+qD(g)����m��n��p��qΪ������������Ϊ�㣩ʱ����Ӧ�ﵽƽ��ı�־��
����ϵ��ѹǿ���ٸı� ����ϵ���¶Ȳ��ٸı� ������ֵ�Ũ�Ȳ��ڸı�
������������������ٸı� ����Ӧ����v(A)��v(B)��v(C)��v(D)=m��n��p��q
����λʱ����m molA�ϼ���Ӧ��ͬʱp molCҲ�ϼ���Ӧ
A���ۢܢݢ� B���ڢۢܢ� C���٢ۢܢ� D���٢ۢܢ�
���𰸡�B
��������
���������������÷�Ӧ��һ����Ӧǰ�������������Ŀ��淴Ӧ������ϵ��ѹǿʼ�ղ��䣬���Բ��ܸ���ѹǿ�жϷ�Ӧ�Ƿ�ﵽƽ��״̬����������ϵ���¶Ȳ��ٸı䣬���淴Ӧ������ȣ������ܾݴ��жϸ÷�Ӧ�ﵽƽ��״̬����ȷ��������ֵ����ʵ���Ũ�Ȳ��ٸı䣬�÷�Ӧ�ﵽƽ��״̬����ȷ�������÷�Ӧ�ﵽƽ��״̬������ֵ������������ٸı䣬��ȷ��������Ӧ����vA��vB��vC��vD=m��n��p��q�����ܾݴ��жϸ÷�Ӧ�Ƿ�ﵽƽ��״̬����������λʱ����m mol A�ϼ���Ӧ��Ч��pmol C�γɣ�ͬʱpmol CҲ�ϼ���Ӧ����ȷ����ѡB��


 99��1������ĩ��ѵ��ϵ�д�
99��1������ĩ��ѵ��ϵ�д� ��ǿ��У��ĩ���100��ϵ�д�
��ǿ��У��ĩ���100��ϵ�д� �óɼ�1��1��ĩ���100��ϵ�д�
�óɼ�1��1��ĩ���100��ϵ�д� ��״Ԫ���źþ�ϵ�д�
��״Ԫ���źþ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������Ӻ�������ȡ�������ͼ���£�

(1)ָ����ȡ��Ĺ������йص�ʵ��������ƣ�
��________________����____________________��
(2)���պ���ʱ������Ҫ���ż��⣬����Ҫ�õ��������� (������������ѡ��������������������ĸ��д�ڿհ״�)��
A�ձ� B���� C������ D������ E�ƾ��� F������
(3)��ȡ��Ĺ����У��ɹ�ѡ����л��ܼ���_____ ___(����ĸ���)��(���ᡢ���;�������ˮ)
A���ױ����ƾ� B�����Ȼ�̼���� C�����͡����� D�����͡�����
(4)���������������ʱ���������� ��ۼ���
(5)������л�����Һ����ȡ��ͻ����л��ܼ�������Ҫ�������۲�����ʵ��װ�ã�ָ���������
�� ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A��������ȼ����Ϊ��H=-285.5kJmol��1������ˮ���Ȼ�ѧ����ʽΪ2H2O ��l��![]() 2H2��g��+O2��g�� ��H=+285.5kJmol��1
2H2��g��+O2��g�� ��H=+285.5kJmol��1
B����ӦSO2��g��+2H2S��g��=3S��s��+2H2O��l���ڳ��������Է����У���÷�Ӧ����H��0
C��500����30MPa�£���0.5molN2��1.5molH2�����ܱյ������г�ַ�Ӧ����NH3��g��������19.3kJ�����Ȼ�ѧ����ʽΪ��N2��g��+3H2��g��![]() 2NH3��g����H=-38.6kJmol��1
2NH3��g����H=-38.6kJmol��1
D����C��ʯī��s��=C�����ʯ��s����H=+1.90kJmol��1��֪�����ʯ��ʯī�ȶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ����ȷ������ ��
A��Cu����ϡHNO3��Cu��2 H����NO![]() ===Cu2����NO2����H2O
===Cu2����NO2����H2O
B����ʯī�缫��ⱥ��ʳ��ˮ��2 Cl����2 H2O ![]() 2 OH����H2����Cl2��
2 OH����H2����Cl2��
C��(NH4)2Fe(SO4)2��Һ�����NaOH��Һ��Ӧ��Fe(OH)2��Fe2����2OH��===Fe(OH)2��
D����Fe(NO3)3��Һ�м��������HI��Һ��2 Fe3����2 I��===2 Fe2����I2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������谷��C3H6N6����һ����Ҫ�Ļ���ԭ�ϣ������ڣ� ��
A.����
B.�����
C.���
D.����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������Ҫ0.1 mol��L��1 NaOH��Һ450 mL��0.5 mol��L��1������Һ500 mL��������������Һ����������ش��������⣺

��1������ͼ��ʾ��������������Һ�϶�����Ҫ����____________________(����ĸ)��
������������Һ�����õ��IJ���������__________________(����������)��
�������й�����ƿʹ��˵������ȷ������ ��
a������ƿʹ��ǰһ��Ҫ����Ƿ�©Һ�������Ϊװˮ����ƿ���������۲��Ƿ�©ҹ����������������ת180����������۲��Ƿ�©ҹ��
b��������Ϊ��Ӧ��������������Һ�����������ǿ������������������Һ��
c�����ܽ������Ũ��Һֱ��������ƿ���ܽ��ϡ�ͣ����ܼ���������ȵ�Һ�� ��
d��������ƿ������Һ������ʱ���ӿ̶��ߣ�������ҺŨ��ƫС��
(2)������NaOH��Һʱ��
�ٸ��ݼ�����������ƽ��ȡNaOH������Ϊ________g��
����NaOH��Һ��ת��������ƿʱ����������������������ҺŨ��___________(�>������<������)0.1 mol��L��1��
����NaOH�����ܽ��������������ƿ��ϴ���ձ�����������ϴ��Һ��������ƿ�����ݣ���������ҺŨ��___________(�>������<������) 0.1 mol��L��1��
(3)������������Һʱ��
��������������Ϊ98%���ܶ�Ϊ1.84 g��cm��3��Ũ��������Ϊ__________(����������һλС��)mL��
�����ʵ������15 mL��50 mL��100 mL��Ͳ��Ӧѡ��___________mL��Ͳ��ã�
�����ƹ������������ձ��н�Ũ�������ϡ�ͣ�ϡ��ʱ����������__________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ҵ�����Ҫ���л�����ԭ�ϣ�������ϩ����ֱ��ˮ�Ϸ�����ˮ�Ϸ��������ش��������⣺
��1�����ˮ�Ϸ���ָ�Ƚ���ϩ��Ũ���ᷴӦ����������������C2H5OSO3H������ˮ�������Ҵ���д����Ӧ��Ӧ�Ļ�ѧ����ʽ ��
��2����֪��
�״���ˮ��Ӧ 2CH3OH��g���TCH3OCH3��g�� + H2O��g����H1=��23.9kJmol��1
�״���ϩ����Ӧ 2CH3OH��g���TC2H4��g�� + 2H2O��g����H2=��29.1kJmol��1
�Ҵ��칹����Ӧ C2H5OH��g���TCH3OCH3��g����H3=" +" 50.7kJmol��1
����ϩ����ֱ��ˮ�Ϸ�ӦC2H4��g�� + H2O��g���TC2H5OH��g������H= kJmol��1������ˮ�Ϸ���ȣ�����ֱ��ˮ�Ϸ����ŵ��� ��
��3������ֱ��ˮ�Ϸ�����ϩ��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ������![]() ��
��![]() =1��1��
=1��1��
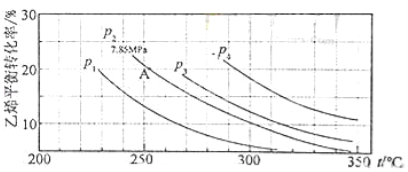
����ʽ������ϩˮ�����Ҵ���Ӧ��ͼ��A���ƽ�ⳣ��Kp= ��
��A����ѹΪ7.85MPa,��ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�����������
��ͼ��ѹǿ��P1��P2��P3��P4����С˳��Ϊ �������� ��
������ֱ��ˮ�Ϸ������õĹ�������Ϊ������/������Ϊ��������Ӧ�¶�290����ѹǿ6.9MPa��![]() ��
��![]() =0.6��1����ϩ��ת����Ϊ5%����Ҫ��һ�������ϩת���ʣ����˿����ʵ��ı䷴Ӧ�¶Ⱥ�ѹǿ�⣬�����Բ�ȡ�Ĵ�ʩ�� �� ��
=0.6��1����ϩ��ת����Ϊ5%����Ҫ��һ�������ϩת���ʣ����˿����ʵ��ı䷴Ӧ�¶Ⱥ�ѹǿ�⣬�����Բ�ȡ�Ĵ�ʩ�� �� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������£�X������Y��Ӧ������Z��Ӧ���Ҷ����ڸ��ֽⷴӦ����
ѡ�� | X | Y | Z |
A | Cu | HNO3 | Fe(NO3)3 |
B | FeCl3 | Zn | NaHCO3 |
C | O2 | NH3 | SO2 |
D | NH4Al(SO4)2 | Ba(NO3)2 | NaOH |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�����������������ڷ�Ӧ�����������ǣ� ��
A��̼������ȷֽ� B���Ҵ�ȼ�� C������������������Ӧ D������������ˮ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com