
【题目】三聚氰胺(C3H6N6)是一种重要的化工原料,它属于( )
A.单质
B.混合物
C.有机物
D.无机物
 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】下列有关性质的比较,不能用元素周期律解释的是
A. 金属性:Na>Mg B. 酸性:H2SO4>H2SiO3
C. 稳定性:HCl> HBr D. 同浓度溶液的碱性:Na2CO3> NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中既能跟稀硫酸反应, 又能跟氢氧化钠溶液反应的化合物是( )
①Al ②Al2O3 ③Al(OH)3 ④AlCl3 ⑤NaHCO3
A.①③④ B.②③⑤ C.②③④ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作.不正确的是
A. 给试管、烧杯、蒸发皿和烧瓶加热时都要垫上石棉网
B. 酒精灯内盛酒精不得超过容积的![]()
C. 往试管里装粉末状药品.可以用纸槽
D. 酒精灯不慎碰翻着火,应立即用湿布盖灭
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】

(1)该浓盐酸中HCl的物质的量浓度为__________mol·L-1。
(2)某学生欲用该浓盐酸和蒸馏水配制成1mol·L-1的稀盐酸。现实验室仅需要这种盐酸220mL,试回答下列问题:
①经计算需要______mL浓盐酸,在量取时宜选用下列量筒中的______。
A.5mL |
B.10mL |
C.25mL |
D.50mL |
②在量取浓盐酸后,进行了下列操作:
a等稀释的盐酸的温度与室温一致后,沿玻璃棒注入容量瓶中。
b往容量瓶中小心加蒸馏水至液面离容量瓶刻度线1~2cm时,改用胶头滴管加蒸馏水,使溶液的液面与瓶颈的刻度标线相切。
c在盛盐酸的烧杯中注入蒸馏水,并用玻璃棒搅动,使其混合均匀。
d用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是(填序号)____________。若量取的是浓硫酸,简述第c步实验的操作过程。
③在上述配制过程中,用量筒量取浓盐酸时仰视观察凹液面,其配制的稀盐酸浓度________(填“偏高”、“偏低”或“无影响”,下同)。若定容后把容量瓶倒置摇匀,发现液面低于刻度线,又加水至刻度线,则配制的稀盐酸浓度________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个不传热的固定容积的密闭容器中,发生可逆反应mA(g)+nB(g)![]() pC(g)+qD(g),当m、n、p、q为任意整数(不为零)时,反应达到平衡的标志是
pC(g)+qD(g),当m、n、p、q为任意整数(不为零)时,反应达到平衡的标志是
①体系的压强不再改变 ②体系的温度不再改变 ③各组分的浓度不在改变
④各组分质量分数不再改变 ⑤反应速率v(A):v(B):v(C):v(D)=m:n:p:q
⑥单位时间内m molA断键反应,同时p molC也断键反应
A.③④⑤⑥ B.②③④⑥ C.①③④⑤ D.①③④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烷、乙烯、乙炔共同具有的性质是( )
A.都难溶于水,且密度比水小
B.能够使溴水和酸性KMnO4溶液褪色
C.分子中各原子都处在同一平面内
D.都能发生聚合反应生成高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌是一种过渡金属,外观呈现银白色,在现代工业中对于电池制造上有不可磨灭的地位。现代炼锌的方法可分为火法和湿法两大类.硫酸铅是生产锌的副产品。
(1)火法炼锌是将闪锌矿(主要含ZnS)通过浮选、焙烧使它转化为氧化锌,再把氧化锌和焦炭混合,在鼓风炉中加热至1473-1573K,使锌蒸馏出来。将闪锌矿焙烧使它转化为氧化锌的主要化学反应方程式为。
(2)某含锌矿的主要成分为ZnS(还含少量FeS等其他成分),以其为原料冶炼锌的工艺流程如图所示:
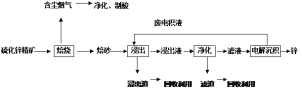
回答下列问题:
①焙烧过程中产生的含尘烟气可净化制酸,该酸可用于后续的_______操作。
②浸出液“净化”过程中加入的主要物质为锌粉,其作用是。
③改进的锌冶炼工艺,采用了“氧压酸浸”的全湿法流程,既省略了易导致空气污染的焙烧过程,又可获得一种有工业价值的非金属单质。“氧压酸浸”中发生的主要反应的离子方程式为________
(3)工业冶炼锌的过程中,会产生铅浮渣(主要成分是PbO、Pb,还含有少量Ag、Zn、CaO和其他不溶于硝酸的杂质),某科研小组研究利用铅浮渣生产硫酸铅的流程如下:
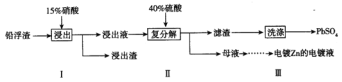
已知:25℃时,Ksp(CaSO4)=4.9×10-5,KSP(PbSO4)=1.6×10-8。
①已知步骤Ⅰ有NO气体产生,浸出液中含量最多的阳离子是Pb2+。写出Pb参加反应的化学方程式_____________________。
②步骤Ⅰ需控制Pb的用量并使Pb稍有剩余,目的是使Ag留在浸出渣中,产品PbSO4还需用Pb(NO3)2溶液多次洗涤,目的是除去附着在硫酸铅表面的微溶物硫酸钙。沉淀转化反应的离子方程式是___。
③母液中可循环利用的溶质的化学式是_____________(填一种物质)
(4)现向含Pb2+、Ca2+浓度均为0.10mol/L的混合溶液中滴加0.10mol/LSO42-溶液.当Pb2+沉淀完全时,溶液中Ca2+浓度为mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某密闭容器中加入 4 mol A、1.2 mol C 和一定量的 B 三种气体,一定条件 下发生反应,各物质的浓度随时间变化如甲图所示[已知 t0~t1 阶段保持恒温、恒容,且 c(B)未画出]。乙图为 t2 时刻后改变反应条件,反应速率随时间的变化情况,已知在 t2、t3、t4、t5 时刻各改变一种不同的条件,其中 t3 时刻为使用催化剂。
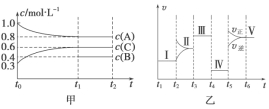
(1)若 t1=15 s,则 t0~t1 阶段的反应速率为 v(C)= 。
(2)t4 时刻改变的条件为 ,B 的起始物质的量为 。
(3)t5 时刻改变的条件为 ,该反应的逆反应为 (填“吸热反 应”或“放热反应”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com